2. 中昊晨光化工研究院有限公司, 四川 自贡 643201
2. Zhonghao Chenguang Research Institute of Chemical Industry Co Ltd, Zigong 643201, China
碳酸二苯酯(Diphenyl Carbonate, DPC)作为一种重要的有机化工中间体[1], 不仅可以用于合成异氰酸酯及农药、医药, 还可以替代光气合成聚碳酸酯.近十年来, 随着我国经济的高速发展, 国内对DPC的需求不断增加.
DPC的合成方法最初是采用苯酚与光气或氯甲酸甲酯反应, 但光气及氯甲酸甲酯均有剧毒, 存在严重的环境、安全问题[2].上世纪70年代以来, 苯酚氧化羰化法、苯酚电羰化法、尿素法、二氧化碳法以及酯交换法等多条非光气清洁生产工艺路线被开发[3-10].其中, 利用草酸二甲酯(Dimethyl Oxalate, DMO)或草酸二乙酯与苯酚先进行酯交换合成草酸二苯酯(Diphenyl Oxalate, DPO), 然后DPO再脱羰生成DPC的工艺路线备受关注.该路线不仅操作条件相对温和、产物易分离、DPO脱羰生成的CO可回收用于制备草酸烷基酯, 还成功地将C1化学和碳酸酯产业链有机结合, 顺利实现了“煤制乙二醇”产业链的拓展.
由于DPO脱羰制备DPC较易进行, 催化剂选择性几乎为100%, DPC收率可高达95.0%以上, 因而酯交换合成草酸二苯酯被认为是制约该工艺路线发展的瓶颈[11, 12].以“煤制乙二醇”中间体草酸二甲酯为例, 一般认为草酸二甲酯和苯酚酯交换过程分为两步:首先, 草酸二甲酯与苯酚生成甲基苯基草酸酯(Methyl Phenyl Oxalate, MPO); 其次, 甲基苯基草酸酯发生歧化或者进一步与苯酚酯交换生成草酸二苯酯, 有关反应方程式如下:
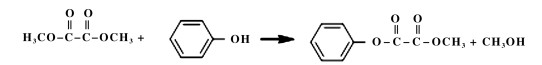
|
(1) |
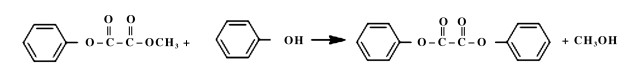
|
(2) |

|
(3) |
草酸二甲酯与苯酚酯交换合成草酸二苯酯可分为多相催化体系[3, 10, 13-34]和均相催化体系[3, 10, 35].其中, 负载型三氧化钼催化剂是研究较多的催化体系[13, 22-30, 33].马新宾课题组围绕MoO3/SiO2催化剂开展了一系列研究, 发现泥浆浸渍法制备的催化剂其性能虽然较传统浸渍法提高不明显, 但制备过程中无需高温焙烧且不产生废气、废液[23, 28].当将无定形TiO2覆盖在SiO2载体表面时, 新制备的MoO3/TiO2-SiO2催化剂由于活性物种分散更好且酸量更高, 致使其催化性能优于MoO3/SiO2[13, 24]; 此外, Sn助剂的加入也利于MoO3/SiO2性能的提升[15, 25].我们前期对比了传统浸渍法和热扩散法制备的MoO3/SiO2催化剂[33], 发现热扩散法制备的催化剂表面钼含量高且MoO3分散更好, 其酯交换性能优于传统浸渍法. Biradar等[30]在中性条件下采用溶胶-凝胶法制备MoO3/SiO2催化剂用于草酸二乙酯和苯酚酯交换反应, 也获得了较传统浸渍法更佳的催化性能.然而截止目前, 在碱性条件下采用溶胶-凝胶法制备MoO3/SiO2催化剂用于草酸烷基酯与苯酚酯交换合成草酸二苯酯尚未见诸报道.因此, 我们考察了碱性条件下MoO3/SiO2催化剂的制备及其催化草酸二甲酯与苯酚酯交换的反应性能.
1 实验部分 1.1 主要化学试剂草酸二甲酯、钼酸铵、硅酸四乙酯、1, 2-丙二醇(国药化学试剂有限公司); 苯酚(广东光华化学厂有限公司).
1.2 催化剂制备取适量氨水调节去离子水的pH值形成碱性溶液A, 其中pH分别为8.6、9.1及9.7.另取一定量硅酸四乙酯、乙醇、1, 2-丙二醇及钼酸铵形成溶液B.然后在搅拌条件下将B液逐滴加入到80 ℃预热的A液中, 滴加完毕, 继续搅拌、老化.将所得凝胶进行干燥、并于550 ℃焙烧5 h, 即得MoO3/SiO2催化剂.为了方便, 所有催化剂均标记为xMoO3/SiO2, 其中x代表MoO3的负载量(重量百分比).
1.3 催化性能评价及产物分析草酸二苯酯的合成在带有搅拌器和分馏柱的250 mL三颈烧瓶中进行.分别将一定量的苯酚、草酸二甲酯和催化剂按比例加入, 通惰性气体保护, 升温到反应温度.反应结束后的釜液和馏分用带有FID检测器的气相色谱进行分析, 色谱柱为SUPELCO 25316 SPBTM-5型(15 m×0.53 mm×0.5 μm), 采用程序升温法, 检测器温度和气化室温度均为270 ℃.
催化剂活性用苯酚转化率表示, 选择性用MPO、DPO的选择性及MPO与DPO总选择性(酯交换选择性)表示.
1.4 催化剂表征催化剂晶相分析在Philips X’pert pro MPD型X射线衍射仪上进行, Cu靶, Kα辐射源, 管电压40 kV, 管电流40 mA, 入射狭缝(1/6)°, 扫描速度2°/min, 扫描范围5°~80°.
红外在NICOLET 6700红外光谱仪(美国Thermo Scientific公司)上进行, 扫描波数范围为: 400~1600 cm-1.
样品的X射线光电子能谱在ESCALAB 250Xi型X射线电子能谱仪(美国Thermo Fischer)上进行测试.其中以Al Kα(hv = 1253.6 eV)为激发光源, 样品的荷电效应以C 1s (284.60 eV)为内标加以校正.
NH3-TPD表征在TP5080型全自动化学吸附仪(天津先权)上进行, 用高纯氮气400 ℃吹扫降至50 ℃, 在50 ℃化学吸附NH3至饱和, 再切换成氮气以10 ℃/min升温速率从50 ℃升温至800 ℃, 用热导检测NH3的脱附信号.催化剂的酸量根据NH3脱附峰面积进行计算.
2 结果与讨论 2.1 催化剂表征结果 2.1.1 催化剂的物相结构不同MoO3负载量的MoO3/SiO2催化剂(合成pH = 9.1)的XRD谱图如图 1a.当MoO3负载量为4%~12%(重量百分比), 仅在23.0°(JCPDS 43-0784)附近出现了无定形SiO2的特征衍射峰, 并未观察到MoO3的特征衍射峰, 表明Mo物种含量较低或以高分散形式存在于MoO3/SiO2催化剂.但当MoO3负载量为15%(重量百分比)时, 在2θ为12.8°, 23.3°, 27.4°, 33.7°附近出现了较弱的MoO3特征衍射峰(JCPDS 05-0508);继续增加MoO3负载量至18%(重量百分比)时, MoO3的衍射峰变得更加明显和尖锐, 表明MoO3晶粒尺寸增大.

|
图 1 不同MoO3负载量的MoO3/SiO2催化剂(pH = 9.1)及不同pH值条件下12% MoO3/SiO2催化剂的XRD谱图 Figure 1 XRD patterns of the MoO3/SiO2 catalysts with different MoO3 loadings synthesized at pH=9.1 (a) and the 12% MoO3/SiO2 catalysts synthesized at different pH values (b). |
不同pH值条件下合成的12%(重量百分比)MoO3/SiO2催化剂的XRD谱图示于图 1b. pH = 8.6及pH =9.7条件下合成的12%(重量百分比) MoO3/SiO2催化剂均在12.8°, 23.3°, 27.4°及33.7°附近出现了MoO3的特征衍射峰.而pH为9.1条件下合成的MoO3/SiO2催化剂并未观察到MoO3的特征衍射峰, 表明pH为9.1时, MoO3/SiO2催化剂中的MoO3以高分散形式存在.说明MoO3/SiO2催化剂制备过程中, 水解反应的pH值影响了Mo物种在催化剂表面的分散.
2.1.2 催化剂的FT-IR不同MoO3负载量的MoO3/SiO2催化剂的FT-IR光谱如图 2, 所有样品均呈现类似的吸收峰.在1098、800和463 cm-1附近出现的峰分别归属为硅氧四面体的反对称伸缩振动(νas(Si-O-Si))、硅氧四面体的对称伸缩振动(νs(Si—O—Si))、Si—O—Si键的弯曲振动[36].此外, 还在908 cm-1附近出现了Mo—O—Si键振动吸收峰[13], 表明MoO3/SiO2催化剂中活性物种与载体之间发生了相互作用力.

|
图 2 MoO3/SiO2催化剂的红外光谱图(pH = 9.1) Figure 2 FT-IR spectra of the MoO3/SiO2 catalysts synthesized at pH 9.1 |
为了获得催化剂表面元素的化学环境信息, 对MoO3/SiO2催化剂进行了XPS测试.不同pH值条件下制备的12%(重量百分比)MoO3/SiO2催化剂及15%(重量百分比)MoO3/SiO2(pH=9.1)催化剂的Mo 3d5/2、Mo 3d3/2轨道结合能分别为232.50~232.60 eV及235.60~235.70 eV, 表明Mo物种以MoO3形式存在.对于12%(重量百分比) MoO3/SiO2催化剂, 不同pH值条件制备的MoO3/SiO2催化剂表面Mo含量按以下顺序降低: pH = 9.1 > pH = 8.6 > pH = 9.7.结合图 1b的XRD结果, 表明pH=9.1时, 12%(重量百分比) MoO3/SiO2催化剂表面的Mo物种分散更好.说明催化剂制备过程中水解反应的pH值对催化剂表明Mo物种的分散有一定影响. pH值均为9.1时, 与12%(重量百分比) MoO3/SiO2催化剂相比, 15% (重量百分比)MoO3/SiO2催化剂表面Mo含量略微减小.结合图 1a的XRD结果, 这可能是由于较高的MoO3含量导致催化剂表面Mo物种发生聚集, 晶粒尺寸增加, 表面Mo物种分散变差.
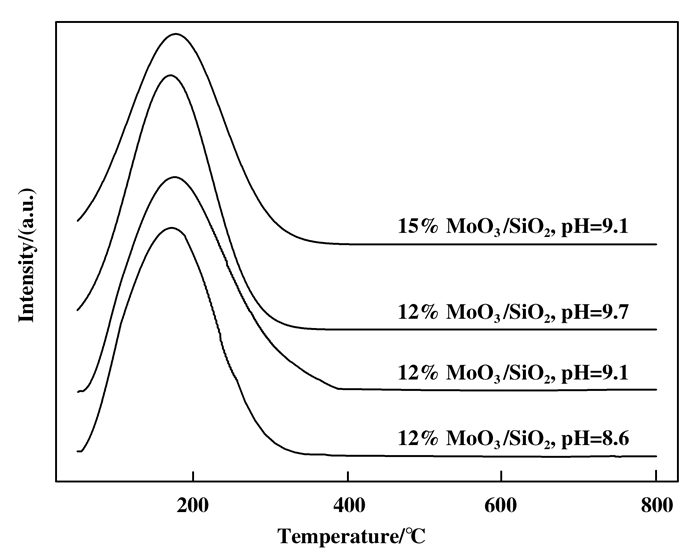
2.1.4 催化剂的NH3-TPD不同pH值条件下制备的12%(重量百分比)MoO3/SiO2催化剂的NH3-TPD如图 3, 三个催化剂均呈现一个氨的脱附峰, 其峰位置位于175 ℃附近, 归属为弱酸性中心[33].与pH=8.6及pH=9.7制备的MoO3/SiO2催化剂相比, pH=9.1制备的MoO3/SiO2催化剂脱附峰面积较大, 通过对脱附峰面积进行分析, pH=8.6、pH=9.1及pH=9.7的MoO3/SiO2催化剂的氨脱附量分别为0.088 mmol/g、0.095 mmol/g及0.079 mmol/g, 表明MoO3/SiO2催化剂制备过程中, 水解反应的pH值对催化剂的表面酸量有一定影响.此外, pH值均为9.1时, 与12%(重量百分比) MoO3/SiO2催化剂相比, 15%(重量百分比) MoO3/SiO2催化剂的氨脱附峰面积略微增加, 其氨脱附量为0.097 mmol/g.
|
图 3 MoO3/SiO2催化剂的NH3-TPD图 Figure 3 NH3-TPD profiles of the MoO3/SiO2 catalysts |
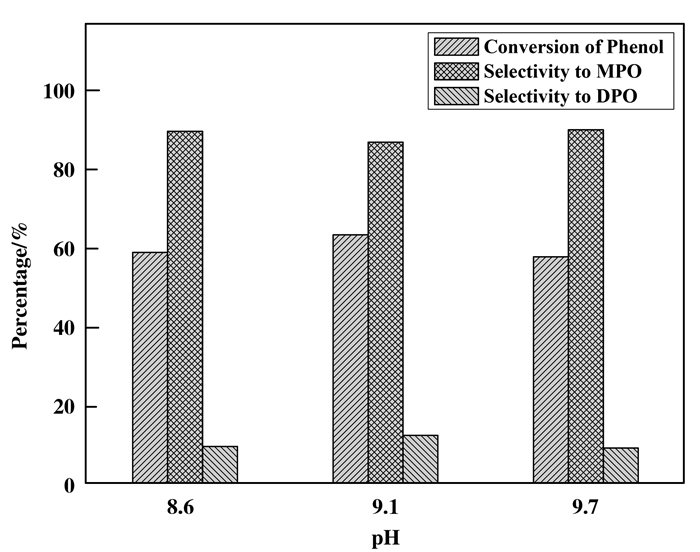
不同pH值条件下制备的12%(重量百分比)MoO3/SiO2催化剂反应性能见图 4.结果显示: pH=9.1时制备的12%(重量百分比)MoO3/SiO2催化剂的催化性能最好, 苯酚转化率达63.6%, MPO和DPO选择性分别为87.0%、12.9%.结合XRD、XPS和NH3-TPD表征结果, 这可能与该催化剂具有更高的酸量和表面Mo物种分散更好有关.此外, 由于所有MoO3/SiO2催化剂均只呈现弱酸中心.因此, 弱酸位是反应的活性中心.
|
图 4 pH值对MoO3/SiO2催化剂性能的影响 Figure 4 Effect of pH on the performance of 12%MoO3/SiO2 catalysts Reaction conditions: m(catalyst)=1.20 g, 0.20 mol DMO, 0.20 mol Phenol, T=180 ℃, t = 3 h |
pH= 9.1时, 不同负载量的MoO3/SiO2催化剂的酯交换活性见图 5.当MoO3负载量≤12%时, 随着MoO3负载量的增大, 苯酚转化率和DPO选择性逐渐增大, MPO则呈现相反的规律.当MoO3负载量为12%时, 苯酚的转化率达最大.继续增大MoO3负载量, 苯酚的转化率反而下降.根据XRD及XPS结果(图 1及表 1), 这可能是由于催化剂表面出现过多的MoO3晶体覆盖了原有的活性中心有关, 类似的现象已有报道[26, 33].
| 表 1 MoO3/SiO2催化剂的钼原子结合能及表面元素组成 Table 1 Binding energy of Mo 3d and surface elements composition of the MoO3/SiO2 catalysts |

|
图 5 MoO3负载量对MoO3/SiO2催化剂性能的影响 Figure 5 Effect of MoO3 loading on the performance of MoO3/SiO2 catalysts prepared at pH=9.1 Reaction conditions: 0.20 mol DMO, 0.20 mol Phenol, m(catalyst) = 1.20 g, T =180 ℃, t = 3 h |
综上所述, 当MoO3负载量为12%(重量百分比), pH为9.1时的MoO3/SiO2催化剂具有更高的催化性能.后续选用此催化剂进行酯交换工艺条件优化.
2.3 pH=9.1, 12%MoO3/SiO2催化酯交换反应优化 2.3.1 反应温度图 6为反应温度对酯交换反应的影响.可以看出, 当温度为160 ℃时, 苯酚的转化率较低.随着反应体系温度升高, 苯酚转化率和DPO选择性也逐渐增大, 而MPO选择性则呈相反趋势, 这说明提高反应体系温度有利于酯交换和歧化反应的进行, 这可能与酯交换反应、歧化反应均为吸热反应相关[33].当反应温度达180 ℃时, 苯酚和产物的收率达最大.因此, 较适宜的反应温度为180 ℃.

|
图 6 反应温度对酯交换反应的影响 Figure 6 Effect of Reaction Temperature on transesterification Reaction conditions: 0.20 mol DMO, 0.20 mol Phenol, m(catalyst) = 1.20 g, t = 3 h |
图 7为原料中DMO与苯酚摩尔比对酯交换反应的影响.当DMO与苯酚摩尔比为0.5时, 苯酚处于过量状态, 因此转化率相对较低, 仅为41.0%, 产物MPO和DPO的选择性分别约为79.6%和20.3%.随着DMO与苯酚摩尔比由1逐渐增加到2, 产物MPO和DPO的选择性变化相当小但苯酚转化率有明显提高, 表明草酸二甲酯过量有利于苯酚的转化; 继续增大摩尔比到2.5时, 苯酚转化率增加较小, 几乎达到平台.因此, 适宜的草酸二甲酯与苯酚摩尔比为2.此时, 苯酚转化率可达70.0%, MPO和DPO的选择性分别为88.4%和11.5%.

|
图 7 n(DMO)/n(Phenol)对酯交换反应的影响 Figure 7 Effect of n(DMO)/n(Phenol) on transesterification Reaction conditions: 0.20 mol Phenol, 1.20 g catalyst, T=180 ℃, t =3 h |
图 8为反应时间对酯交换反应的影响.可以看出, 随着反应时间的延长, 苯酚转化率先急剧增加然后逐渐变缓, 而MPO和DPO选择性均变化较小, 表明延长反应时间有利于酯交换的进行.但反应超过3 h后继续延长时间, 苯酚转化率增加幅度较小.因此, 较佳的反应时间为3 h.

|
图 8 反应时间对酯交换反应的影响 Figure 8 Effect of reaction time on transesterification Reaction conditions: 1.20 g catalyst, 0.20 mol Phenol, n(DMO)/n(Phenol)=2, T=180 ℃ |
催化剂制备过程中, 水解反应的pH值影响催化剂表面的Mo物种分散及表面酸量.钼和硅作用产生的弱酸位是反应的活性中心.当pH为9.1时制备的12%(重量百分比)MoO3/SiO2催化剂具有较佳的酯交换反应活性, 这可能是由于该催化剂表面有更高的Mo含量及更高的酸量.当12%(重量百分比) MoO3/SiO2催化剂为1.20 g, 0.20 mol Phenol, n(DMO)/n(Phenol)=2, T=180 ℃, t = 3 h时, 苯酚转化率可达70.0%, MPO和DPO选择性分别为88.4%和11.5%.
| [1] | Xu Ke-xun(徐克勋). Handbook of fine organic chemical raw materials and intermediates(精细有机化工原料及中间体手册)[M]. Beijing: Chem Ind Press(北京: 化学工业出版社), 1998. |
| [2] | Mei Fu-ming(梅付名), Li Guang-xing(李光兴), Mo Wan-ling(莫婉玲). Synthesis of diphenyl carbonate(碳酸二苯酯的合成工艺进展)[J]. Mod Chem Ind(现代化工), 1999, 19(5): 13–15. |
| [3] | Gong J L, Ma X B, Wang S P. Phosgene-free approaches to catalytic synthesis of diphenyl carbonate and its intermediates[J]. Appl Catal A Gen, 2007, 316(1): 1–21. DOI:10.1016/j.apcata.2006.09.006 |
| [4] | Murayama T, Hayashi T, Arai Y, et al. Direct synthesis of diphenyl carbonate by mediated electrocarbonylation of phenol at Pd2+ supported activated carbon anode[J]. Electrochim Acta, 2011, 56(7): 2926–2933. DOI:10.1016/j.electacta.2010.12.087 |
| [5] | Murayama T, Hayashi T, Kanega R, et al. Phosgene-free method for diphenyl carbonate synthesis at the Pd0/Ketjenblack anode[J]. J Phys Chem C, 2012, 116(19): 10607–10616. DOI:10.1021/jp300809s |
| [6] | Kanega R, Hayashi T, Yamanaka I. Pd(NHC) elctrocatalysis for phosgene-free synthesis of diphenyl carbonate[J]. Acs Catal, 2013, 3(3): 389–392. DOI:10.1021/cs300725j |
| [7] | HwangKuen-Yuan, Chen Yu Z, Chu Chio C, US[P]. 5591883, 1997. |
| [8] | Li Z H, Qin Z F. Synthesis of diphenyl carbonate from phenol and carbon dioxide in carbon tetrachloride with zinc halides as catalyst[J]. J Mol Catal A:Chem, 2007, 264(1/2): 255–259. |
| [9] | Li Zhen-huan(李振环), Qin Zhang-feng(秦张峰), Wang Jian-guo(王建国). Synthesis of diphenyl carbonate from phenol and carbon dioxide with mesoporous SiMCM-41 supported catalysts(介孔催化剂上苯酚和二氧化碳直接合成碳酸二苯酯)[J]. J Fuel Chem Technol(燃料化学学报), 2007, 35(6): 706–710. DOI:10.3969/j.issn.0253-2409.2007.06.012 |
| [10] | Huang S Y, Yan , Wang S P, et al. Recent advances in dialkyl carbonates synthesis and applications[J]. Chem Soc Rev, 2015, 44(10): 3079–3116. DOI:10.1039/C4CS00374H |
| [11] | Harada K, Sugise R, Kashiwagi K, et al, US[P]. 5892089, 1998. |
| [12] | Keigo N, Shuji T, Yuki N. US[P]. 5811573, 1998. |
| [13] | Liu Y, Ma X B, Wang S P, et al. The nature of surface acidity and reactivity of MoO3/SiO2 and MoO3/TiO2-SiO2 for transesterification of dimethyl oxalate with phenol:A comparative investigation[J]. Appl Catal B Environ, 2007, 77(1/2): 125–134. |
| [14] | Ma X B, Guo H L, Wang S P, et al. Transesterification of dimethyl oxalate with phenol over TS-1 catalyst[J]. Fuel Proce Technol, 2003, 83(1/3): 275–286. |
| [15] | Ma X B, Gong J L, Wang S P, et al. Characterization and reactivity of stannum modified titanium silicalite TS-1 catalysts for transesterification of dimethyl oxalate with phenol[J]. J Mol Catal A:Chem, 2005, 237(1/2): 1–8. |
| [16] | Shi Y, Wang Sh P, Ma X B. Microwave preparation of Ti-containing mesoporous materials. Application as catalysts for transesterification[J]. Chem Eng J, 2011, 166(2): 744–750. DOI:10.1016/j.cej.2010.11.081 |
| [17] | Wang S P, Shi Y, Ma X B. Microwave synthesis, cha-racterization and transesterification activities of Ti-MCM-41[J]. Micro Mes Mater, 2012, 156(1): 22–28. |
| [18] | Liu Y, Zhao G M, Liu G, et al. Cyclopentadienyl-functionalized mesoporous MCM-41 catalysts for the transesterification of dimethyl oxalate with phenol[J]. Catal Commun, 2008, 9(10): 2022–2025. DOI:10.1016/j.catcom.2008.03.042 |
| [19] | Liu G, Liu Y, Yang G, et al. Preparation of titania-silica mixed oxides by a sol-gel route in the presence of citric acid[J]. J Phys Chem C, 2009, 113(21): 9345–9351. DOI:10.1021/jp900577c |
| [20] | Ma X B, Wang S P, Gong J L, et al. A comparative study of supported TiO2 catalysts and activity in ester exchange between dimethyl oxalate and phenol[J]. J Mol Catal A:Chem, 2004, 222(1/2): 183–187. |
| [21] | Wang S P, Ma X B, Guo H L, et al. Characterization and catalytic activity of TiO2/SiO2 for transesterification of dimethyl oxalate with phenol[J]. J Mol Catal A:Chem, 2004, 214(2): 273–279. DOI:10.1016/j.molcata.2003.12.020 |
| [22] | Ma X B, Gong J L, Wang S P, et al. Reactivity and surface properties of silica supported molybdenum oxide ca-talysts for the transesterification of dimethyl oxalate with phenol[J]. Catal Commun, 2004, 5(3): 101–106. |
| [23] | Ma X B, Gong J L, Yang X, et al. A comparative study of supported MoO3 catalysts prepared by the new "slurry" impregnation method and by the conventional method:Their activity in transesterification of dimethyl oxalate and phenol[J]. Appl Catal A Gen, 2005, 280(2): 215–223. DOI:10.1016/j.apcata.2004.11.001 |
| [24] | Liu Y, Wang S P, Ma X B. Activity and surface properties of titanium oxide modified silica supported molybdenum oxide catalysts fortransesterification of dimethyl oxalate with phenol[J]. Ind Eng Chem Res, 2007, 46(4): 1045–1050. |
| [25] | Ma X B, Gong J L, Wang S P, et al. Characterization and reactivity of silica supported bimetallic molybdenum and stannic oxides for the transesterification of dimethyl oxalate with phenol[J]. J Mol Catal A:Chem, 2004, 218(2): 253–259. DOI:10.1016/j.molcata.2004.04.022 |
| [26] | Gong J L, Ma X B, Wang S P, et al. Transesterification of dimethyl oxalate with phenol over MoO3/SiO2 catalysts[J]. J Mol Catal A:Chem, 2004, 207(2): 215–220. DOI:10.1016/S1381-1169(03)00504-1 |
| [27] | Gong J L, Ma X B, Yang X, et al. Effect of Mo loading on transesterification activities of MoO3/γ-Al2O3 catalysts prepared by conventional and slurry impregnation methods[J]. Rea Kinet Catal Lett, 2005, 84(1): 79–86. |
| [28] | Gong J L, Ma X B, Yang X, et al. Comparative preparation of MoO3/SiO2 catalysts using conventional and slurry impregnation method and activity in transesterification of dimethy oxalate with phenol[J]. Catal Lett, 2005, 99(3/4): 187–191. |
| [29] | Kotbagi T, Nguyen D L, Lancelot C, et al. Transesterification of diethyl oxalate with phenol over solgel MoO3/TiO2 catalysts[J]. ChemSusChem, 2012, 5(8): 1467–1473. DOI:10.1002/cssc.v5.8 |
| [30] | Biradar A V, Umbarkar S B, Dongare M K. Transesterification of diethyl oxalate with phenol using MoO3/SiO2 catalyst[J]. Appl Catal A Gen, 2005, 285(1/2): 190–195. |
| [31] | Chen C X, Peng J S, Li B, et al. The catalytic activity of CuNi-containing hydrotalcites in the transesterification of dimethyl oxalate with phenol[J]. J Porous Mater, 2009, 16(2): 233–238. DOI:10.1007/s10934-008-9191-1 |
| [32] | Yuan X L, Zhang M, Chen X D, et al. Transesterification of dimethyl oxalate with phenol over nitrogen-doped nanoporous carbon materials[J]. Appl Catal A Gen, 2012, 439/440(1): 149–155. |
| [33] | Zhang F B, Yu X P, Ma F, et al. Transesterification of dimethyl oxalate with phenol over a MoO3/SiO2 catalyst prepared by thermal spreading[J]. Chin J Catal, 2014, 35(7): 1043–1053. DOI:10.1016/S1872-2067(14)60042-5 |
| [34] | Wang S P, Liu Y, Shi Y, et al. Dispersion and catalytic activity of MoO3 on TiO2-SiO2 binary oxide support[J]. AIChE, 2008, 54(3): 741–749. DOI:10.1002/(ISSN)1547-5905 |
| [35] | Zhang Fu-bao(张付宝), Wang Qing-yin(王庆印), Yang Xian-gui(杨先贵), et al. Organo-titanium compound catalysts for transesterification of dimethyl oxalate with phenol[J]. J Mol Catal(Chin)(分子催化), 2014, 28(1): 12–18. |
| [36] | Seyedmonir S R, Abdo S, Howe R F. A fourier transform infrared study of low-frequency vibrations in a supported molybdenum catalyst[J]. J Phys C, 1982, 86(8): 1233–1484. |
 2018, Vol. 32
2018, Vol. 32


