随着能源危机的加剧, 氢能作为新型能源被应用到生活的各个领域, 其生产技术受到越来越多的关注[1].生物乙醇蒸气重整(Ethanol Steam Reforming, ESR)是目前较为前沿的产氢方式, 为可再生能源生产氢气提供了环保路线[2].乙醇水蒸气重整(以下简称ESR)在制氢方面表现出诸多优点, 主要体现在以下方面: (1)氢含量高; (2)可用性好, 生产成本低[3]; (3)易于处理和运输; (4)无毒性[4].然而, ESR过程还涉及一系列重整和水煤气变换反应, 伴随有诸多副产物生成。因此, 催化剂的研究成为了亟待解决的关键, 尤其是研发具有高活性和高稳定性的非贵金属催化体系, 已在该催化领域中被重点关注.
Co基催化剂, 因其具有良好的C—C和C—H键断裂能力而被广泛使用[5], 但这类催化剂通常由于Co物种的烧结和焦碳沉积导致快速失活[6].研究表明, 选择合适的载体是提高催化剂稳定性的有效方法, 这也是目前研发钴基催化剂的主要挑战[7].为了提高Co基催化剂的性能, 采用引入其他活性金属对催化剂载体进行改性.据报道, 催化剂中的CeO2通过调节Ce4+和Ce3+价态之间的变化而表现出优异的储放氧功能[8].在晶格中释放出的流动氧可与含碳物质反应, 从而减少金属表面的积碳, 起到抑制催化剂失活的作用[9-10].
SBA-15分子筛因其具有水热稳定性高、孔径大、孔壁厚等特点已被广泛应用于催化领域. Co/SBA-15催化剂在ESR反应中有很好的发展前景[11], 但其活性金属Co在反应过程中易烧结产生积碳是目前需要解决的问题[5].通过在载体SBA-15骨架中引入金属Ce离子, 利用其储放氧的功能以及与活性组分间的协同作用来提高金属Co的分散度, 减少催化过程中积碳的产生, 从而提高催化活性和稳定性.对改性后的载体和催化剂进行了一系列表征及性能测试, 得出较为适宜的铈硅比(n(Si)/n(Ce)), 为ESR反应中Co基催化剂的制备提供了指导建议.
1 实验部分 1.1 实验试剂与表征乙聚环氧乙烷-聚环氧丙烷-聚环氧乙烷三嵌段共聚物(P123): AR, 美国Aldrich公司; 正硅酸乙酯(TEOS)、乙醇、盐酸: AR, 天津市科密欧化学试剂有限公司; 六水合硝酸钴Co(NO3)2·6H2O, 六水合硝酸铈Ce(NO3)3·6H2O: AR, 天津市光复科技发展公司.
XRD采用日本Rigaku公司的D/Max-2500型X射线衍射仪测定, 采用CuKα射线, 电压40 kV, 电流100 mA, 扫描范围为0.5°~80°, 扫描速度为8°/min.
N2吸附采用美国Micromeritics ASAP 2020型自动吸附仪测定, 样品测定前在真空条件下350 ℃处理4 h, 去除样品中杂质, 吸附剂为高纯氮, 液氮为冷凝剂, 比表面积计算应用BET方程, 由氮吸附等温线得出, 由BJH吸附方程计算得出孔径分布和孔容.
紫外-可见光光谱UV-Vis采用美国PE的漫反射光谱仪(LambdaBio40)测定, BaSO4作为本底, 扫描范围为200~800 nm, 扫描速度为100 nm/min.
红外光谱FT-IR采用Bruker公司所产的NICOLET Nexus型傅立叶变换红外光谱仪测定, 样品通过KBr压片处理, 扫描范围为400~4000 cm-1.
H2程序还原H2-TPR采用美国Micromeritics公司生产的2920型全自动化学吸附仪测定, 样品在400 ℃Ar气氛中预处理60 min, 后用流速为30 mL/min的5%的H2与Ar的混合气吹扫, 从100 ℃升高到1000 ℃, 升温速率为5 ℃/min.
热重-差热分析TG/DTA采用美国Perkin Elmerg公司的Diamond型号TG/DTA热重分析仪完成的.称取5~10 mg催化剂样品置于热天平上, 在空气氛围中程序升温至900 ℃, 升温速率以10 ℃/min进行.
1.2 实验过程 1.2.1 催化剂载体制备以三嵌段共聚物EO20PO70EO20(P123)为模板剂, 正硅酸乙酯为硅源, 采用水热晶化法分别合成SBA-15, Ce-SBA-15载体.
具体步骤:取2 g P123溶于60 g 2 mol/L的HCl溶液中, 并加入15 mL蒸馏水, 搅拌溶解后, 滴加4.18 g TEOS, 在40 ℃水浴中搅拌24 h, 装入聚四氟乙烯内衬的不锈钢反应中, 在100 ℃环境下水热处理48 h, 结束后经过滤、洗涤、干燥, 得到SBA-15粉末, 将样品在马弗炉中以2 ℃/min的速率升温到550 ℃, 在此温度下焙烧6 h, 得到SBA-15.
Ce-SBA-15的制备过程与上述方法相似, 不同的是在水热前加入(Ce(NO3)3·6H2O), 通过控制物质Si、Ce的量来制备不同的催化剂, 用摩尔比n(Si/Ce)来表示n(40)、n(20)、n(10), 随后用2 mol/L的NaOH溶液调节混合组分的水热环境, 使得溶液pH值为4, 接着完成后续步骤, 得到Ce-SBA-15.
1.2.2 Co/SBA-15、Co/Ce-SBA-15的制备分别以上述制得的催化剂为载体, 采用等体积浸渍法以硝酸钴(Co(NO3)2·6H2O)为钴源负载质量分数为7%的Co活性物质, 将样品烘干后, 在马弗炉里以同样的条件焙烧, 得到目标催化剂.
1.3 催化剂的评价催化剂作用于乙醇水蒸气重整制氢反应, 在实验室微型固定床反应装置中进行, 制备粒径0.450~0.280 mm, 堆比重为1.28 g/mL的催化剂0.3与1.5 g石英砂均匀混合放置于不锈钢管中的反应二段, 反应管的其它段路由石英砂填充, 反应前先用流量为35 mL/min的H2对催化剂在400 ℃条件下还原处理2 h, 随后体积比为3:1的水醇混合液通过恒流泵经汽化进入反应管内, 反应在质量空速为3.49 h-1, 反应温度为500 ℃的条件下进行, 测试反应中氢气选择性和乙醇转化率.反应气体产物的检测和分析通过GC950型气相色谱仪的TDX-01填充柱实现, 其中, H2和N2通过热导检测器(TCD)在线分析, 其他气体产物如CO、CH4、CO2等通过氢火焰检测器(FID)在线分析.液体产物通过GC-9890b型气相色谱离线分析.催化剂的催化性能主要通过两个参数来表示, 具体计算方法如下公式2-1和2-2所示.
(1) 乙醇的转化率
| $ {X_{EtOH}}\left( \% \right) = \frac{{{N_{EtOH, in}} - {N_{EtOH, out}}}}{{{N_{EtOH, in}}}} $ | (2-1) |
(2) 各产物选择性
| $ {S_i}\left( \% \right) = \frac{{{{\rm{n}}_{\left( {\rm{i}} \right)}}}}{{\sum {{\rm{n}}_{\left( {\rm{i}} \right)}}}} \times 100 $ | (2-2) |
式中X为乙醇的转化率; Si为各物质的选择性.
2 结果与讨论 2.1 XRD衍射峰由图 1可见, 在小角XRD谱图(A)中2θ=0.5°~5°均出现了3个明显衍射峰, 分别代表(100、110、200)晶面, 说明所合成的载体都具有SBA-15分子筛所特有的有序介孔结构[12], Ce-SBA-15载体样品的XRD谱图衍射峰的强度均略低于SBA-15的衍射峰强度, 这是由于Ce离子的引入导致介孔的有序度降低.金属离子掺杂后的衍射峰向低角度方向发生了部分移动, 随着金属量的增加, 移动角度增大, 这是因为金属Ce的进入, 使得SBA-15载体发生了骨架收缩[13].广角XRD谱图(B)显示出, 掺金属Ce后的载体与SBA-15样品谱图相似.所有样品在20°~30°区域均有无定形硅的衍射峰.在金属引入量低的载体中, Ce物种可能掺入到SBA-15的介孔骨架中, 也可能形成了高度分散且低于XRD的检测限度的微观晶粒, 随着金属物种Ce引入量的增多, 在载体Ce-SBA-15(10)谱图中出现氧化铈晶体的特征峰.

|
图 1 不同载体的XRD谱图 Fig.1 XRD patterns of supports a. SBA-15; b. Ce-SBA-15 (40); c. Ce-SBA-15 (20); d. Ce-SBA-15 (10) |
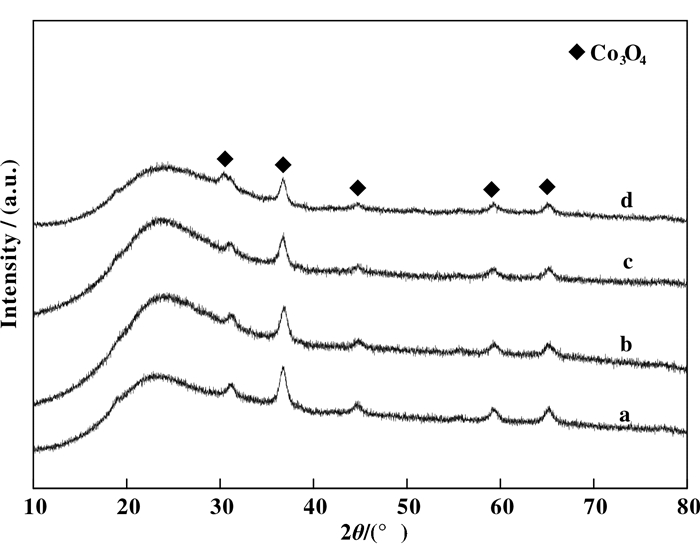
图 2是不同催化剂的广角XRD谱图, 由浸渍法制备的催化剂中均出现了Co3O4的特征峰, 说明Co金属以氧化物Co3O4的形式分散于载体表面[11, 14], 其中Co/Ce-SBA-15(10)催化剂谱图中没有体现出明显的氧化铈晶体特征峰, 这可能是由于表面的金属钴物种覆盖了载体表面存在的少许氧化铈, 检测出与其他催化剂相似的谱图. Co/Ce-SBA-15(40, 20, 10)催化剂中Co3O4的特征峰强度均低于Co/SBA-15的Co3O4的峰强度, 这归因于载体中Ce与Co的协同作用, 增大了Co物种分散度.
|
图 2 不同催化剂的广角XRD谱图 Fig.2 XRD patterns of catalysts a. Co/SBA-15; b. Co/Ce-SBA-15(40); c. Co/Ce-SBA-15(20); d. Co/Ce-SBA-15(10) |
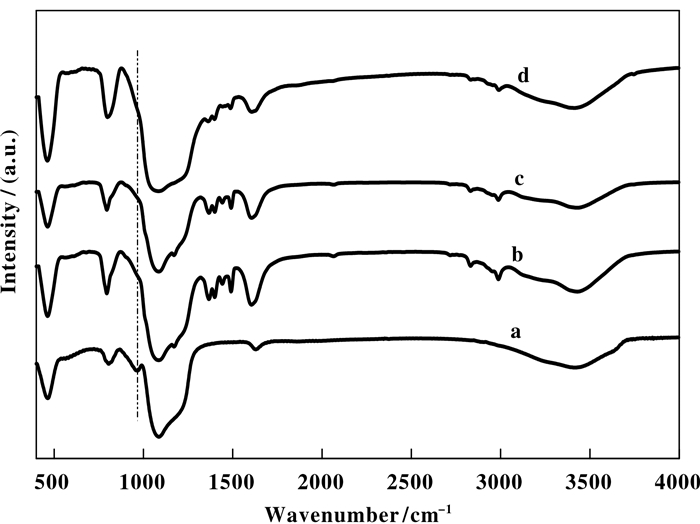
文献表明, SBA-15分子筛骨架震动谱带的吸收峰主要在400~1600 cm-1区域内表现出来, 其主要的对应关系为: 470 cm-1附近为Si-O弯曲振动, 800 cm-1附近为对称伸缩振动; 1090 cm-1附近为Si-O-Si的SiO4反对称伸缩振动[15].由图 3可知, 载体样品与文献报道相符.同时960 cm-1附近的吸收峰被认为是Si-OH的不对称伸缩振动引起的, 此处掺杂金属的分子筛SBA-15显示出的振动谱带有所减弱, 说明载体Ce-SBA-15中出现了Si-O-Ce的伸缩振动峰[16], 影响了Si-OH的振动, 可以侧面说明金属Ce离子成功进入载体骨架, 随着金属量的增加, 谱带减弱更为明显, 这可能是因为过多的金属引入使得部分金属在此载体表面形成富集, 这与XRD谱图结果相符.同时所有载体样品在3415 cm-1处表现出特征吸收峰, 这归因于SBA-15孔道内部硅醇基团(Si-O-H)的振动.
|
图 3 不同载体的FT-IR谱图 Fig.3 FT-IR spectra of supports a. SBA-15; b. Ce-SBA-15 (40); c. Ce-SBA-15 (20); d. Ce-SBA-15 (10) |
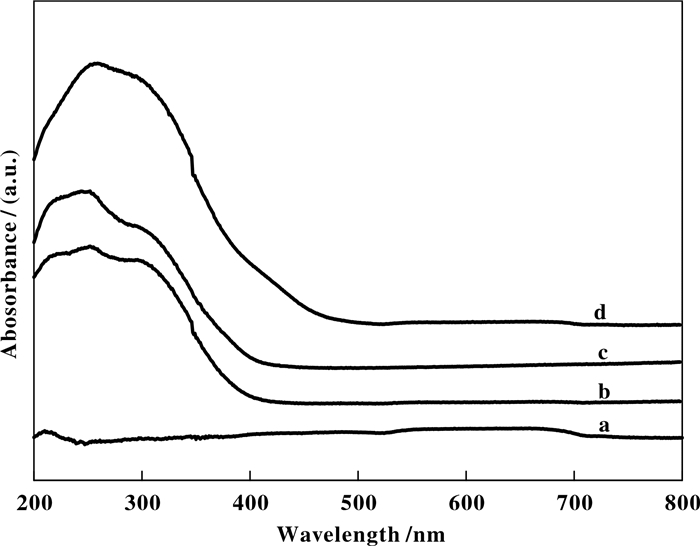
图 4可知, 在250、300 nm附近出现的特征吸收峰, 代表Ce3+、Ce4+与氧配体之间的电荷转移, 265 nm处的吸收峰是由于O2→Ce(Ⅲ)电荷转移跃迁引起的.随着引入金属量的增大, 载体Ce-SBA-15(10)表面可能会富集少量的CeO2, 在300 nm处出现的吸收峰, 这是由O2→Ce(Ⅳ)电荷转移跃迁引起的.这些结果表明金属Ce离子分别以Ce(Ⅲ), Ce(Ⅳ)形式存在于载体体相中[17].
|
图 4 不同载体的UV-Vis谱图 Fig.4 UV-Vis spectra of supports a. SBA-15; b. Ce-SBA-15 (40); c. Ce-SBA-15 (20); d. Ce-SBA-15 (10) |
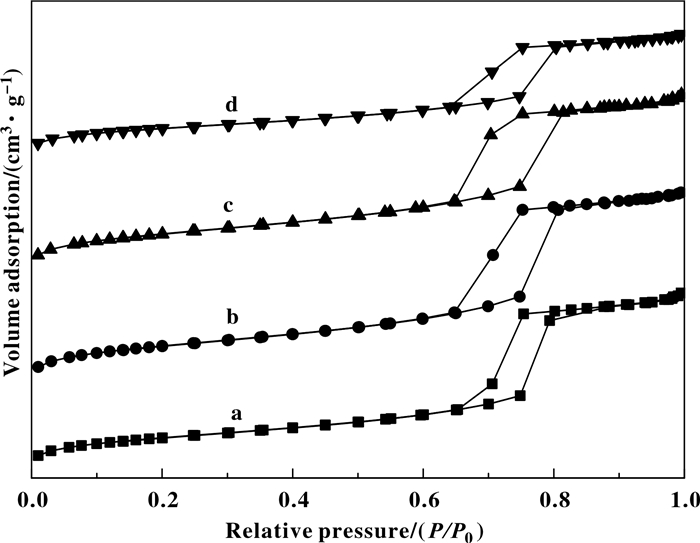
由图 5, 载体的氮吸附等温线均为Ⅳ型吸附曲线, 且有H1型滞后环出现, 说明合成的载体Ce-SBA-15基本保留SBA-15特有的规整孔道结构[18].在相对分压0.6~0.8范围内有急剧变化, 发生N2的毛细凝聚现象, 但随着掺杂金属量的增加, 曲线显示出的规整度有所降低, 这表明金属离子的引入对SBA-15孔结构造成一定的影响.与纯SBA-15相比, 载体Ce-SBA-15(40)和Ce-SBA-15(20)的比表面积和孔体积明显增大, 这是由于Ce的引入使得样品形成的Ce—O键要比原Si—O键的键长长, 导致比表面积增大, 这一现象符合以上键长理论, 说明金属Ce物种被引入到SBA-15分子筛的骨架上.但载体Ce-SBA-15(10)比表面积出现明显的减小, 这是因为引入金属量的增大, 部分金属进入载体的孔道内部或者聚集在载体表面, 造成一定程度的堵塞, 这与载体Ce-SBA-15(10)XRD谱图中出现的较为明显的CeO2衍射峰且孔径减小相一致.
|
图 5 不同载体的N2吸附/脱附曲线 Fig.5 N2 absorption/desorption isotherms of supports a. SBA-15; b. Ce-SBA-15 (40); c. Ce-SBA-15 (20); d. Ce-SBA-15 (10) |

|
图 6 不同载体的孔径分布曲线 Fig.6 pore size distributions of supports a. SBA-15; b. Ce-SBA-15 (40); c. Ce-SBA-15 (20); d. Ce-SBA-15 (10) |
| 表 1 不同载体和催化剂的孔结构性质 Table 1 The structure parameters of the catalyst support and catalyst |
图 7中曲线分别为载体Ce-SBA-15(20)和催化剂Co/SBA-15、Co/Ce-SBA-15(20)在100~900 ℃的氢气程序升温还原谱图, 通过物相还原峰位置, 判断金属物质在催化剂中存在的状态和位置.图中载体a中出现2个H2吸收峰, 分别在480、770 ℃左右, 其中较低温还原峰归属于分散在载体表面或者孔道里极少数Ce4+→Ce3+→Ce0的还原, 770 ℃左右的还原峰对应于载体骨架中Ce物种的还原, 这充分地说明Ce被引入到载体骨架中.纯负载型催化剂b中出现了2个H2吸收峰, 分别在300, 380 ℃左右, 这是由于负载后表面Co3O4的Co3+→Co2+→Co0逐步还原[19], 图中催化剂c中出现4个H2吸收峰, 分别在278、407、488、780 ℃左右, 其中前两个低温还原峰与b中Co3O4的还原峰对相对应, 剩余两个峰均与上述载体中Ce物种的还原峰相对应, 这表明催化剂的载体骨架中已经存在Ce物种, 各吸收峰显示出的温度偏差可能是由金属间的相互作用引起的.

|
图 7 载体和催化剂的H2-TPR谱图 Fig.7 H2-TPR profiles of support and catalyst a. Ce-SBA-15; b. Co/SBA-15; c. Co/Ce-SBA-15(20) |
图 8为不同催化剂在相同时间段内的产物选择性和乙醇转化率, 反应按照水醇体积比3:1的情况下在微型固定床反应器上模拟实验, 反应在质量空速为3.49 h-1, 反应温度为500 ℃, 反应时间为8 h, 发生主反应(Eq.1), 由反应可知, 产物中除了大量目标产物H2以外, 还有很多副产物的生成, 如CO、CO2、CH4和CH3CHO(Eq.2).从样品催化剂活性测试图明显的可以看出, 相比于Co/SBA-15催化剂, 载体骨架中掺有金属Ce的催化剂表现出良好的催化性能, 主要为更高的乙醇转化率, 更高的H2选择性以及更低的乙醛选择性, 其中Co/Ce-SBA-15(20)性能最佳.这是由于金属Ce的加入使Co/Ce-SBA-15催化剂载体相比Co/SBA-15催化剂载体有较大的比表面积, 使负载的活性金属物种Co在其载体表面的分散度大大提高, 促进了金属间的协同作用, 这更有利于催化性能的提高.

|
图 8 不同催化剂的8 h活性测试 Fig.8 ESR activity of the different catalysts with 8 hours |
掺杂金属Ce的催化剂Co/Ce-SBA-15表现出的催化性能与纯负载型Co/SBA-15催化剂的催化性能有着明显的差异, 乙醇转化率均有了显著的提高, 并伴随着副产物含量的变化, 由各产物选择性分布可反映出催化剂的性能, 其中Co/Ce-SBA-15(40、10)催化剂与Co/SBA-15相比, CO选择性有所提高, 这是因为在ESR反应中, CO的转化主要是由WGS(Water Gas Shift)(Eq.3)进行的[20], 金属Ce加入的过多或过少, 均有利于逆水煤气反应的进行, 消耗了H2和CO2.同时CH4转化率降低, 这也是由于Ce的加入减弱了甲烷化反应(Eq.4, Eq.5), 催化剂表现出的催化性能与前面表征相符.其中, Co/Ce-SBA-15(10)催化剂由于大量Ce金属的引入, 造成Ce金属不能很好地进入载体SBA-15骨架.其氧化物CeO2在催化剂表面的存在, 使得活性组分Co不能很好地分散于载体表面, 从而导致催化剂活性降低, 同时在反应副产物中检测到有少量乙烯生成, 这是因为CeO2具有调节催化剂表面酸碱性的作用, 其在催化剂表面的存在, 使得催化剂表面形成少许酸性位, 乙醇发生脱水反应, 产生乙烯(Eq.6).
样品Co/Ce-SBA-15(20)催化剂具有较高的催化活性, H2选择性可达75.5%, 乙醇转化率可达96.6%, CO2选择性也有明显的提高, 其他副产物选择性均有显著的降低趋势, 表明此催化剂作用下反应主要沿主反应方向进行.这归因于适量的Ce被引入到SBA-15骨架中, 提高了载体的比表面积, 并大大提高了活性组分Co的分散度, 可更好的作用于C—C、C—H键的断裂, 适量Ce的存在提高了WGS反应[21], 降低了CO选择性, 促进了CO2和H2的生成, 提高其选择性, 同时表面活性组分Co与Ce的协同作用, 加快了乙醛分解(Eq.7), 降低了乙醛选择性, 更有利于CO转化, 也加强了甲烷重整(Eq.4), 促进CH4的转化, 增加催化剂活性.
| $ {{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{5}}}{\rm{OH + 3}}{{\rm{H}}_{\rm{2}}}{\rm{O}} \to {\rm{2C}}{{\rm{O}}_{\rm{2}}}{\rm{ + 6}}{{\rm{H}}_{\rm{2}}} $ | (1) |
| $ {{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{5}}}{\rm{OH}} \to {\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{CHO + }}{{\rm{H}}_{\rm{2}}} $ | (2) |
| $ {\rm{CO + }}{{\rm{H}}_{\rm{2}}}{\rm{O}} \leftrightarrow {\rm{C}}{{\rm{O}}_{\rm{2}}}{\rm{ + }}{{\rm{H}}_2} $ | (3) |
| $ {\rm{CO + }}{{\rm{H}}_{\rm{2}}} \to {\rm{C}}{{\rm{H}}_{\rm{4}}}{\rm{ + }}{{\rm{H}}_{\rm{2}}}{\rm{O}} $ | (4) |
| $ {\rm{C}}{{\rm{O}}_{\rm{2}}}{\rm{ + }}{{\rm{H}}_{\rm{2}}} \leftrightarrow {\rm{C}}{{\rm{H}}_{\rm{4}}}{\rm{ + }}{{\rm{H}}_{\rm{2}}}{\rm{O}} $ | (5) |
| $ {\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{C}}{{\rm{H}}_{\rm{2}}}{\rm{OH}} \to {{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{4}}}{\rm{ + }}{{\rm{H}}_{\rm{2}}}{\rm{O}} $ | (6) |
| $ {\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{CHO}} \to {\rm{C}}{{\rm{H}}_{\rm{4}}}{\rm{ + CO}} $ | (7) |
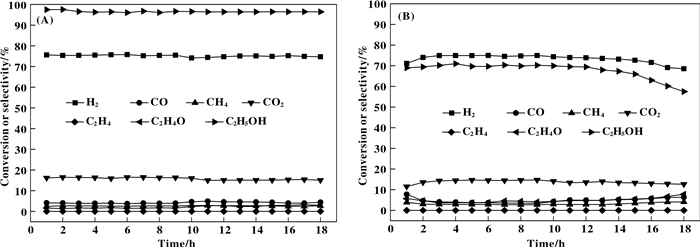
为了进一步研究所制备的催化剂的催化性能, 通过ESR反应在上述条件下对Co/Ce-SBA-15(20)和Co/SBA-15催化剂进行反应时间为18 h的稳定性测试.催化剂Co/Ce-SBA-15(20)的乙醇转化率和产物分布结果如图 9(A)所示, 乙醇转化率的初始值达到97.5%, 反应开始一段时间后转化率稳定在96.5%左右.在所有的产物选择性分布中, H2的选择性均保持在75%左右, 且CO2选择性高达16%.只观察到少量乙醛存在, 说明催化剂Co/Ce-SBA-15(20)在整个反应时间段内保持着长时间的稳定性以及最佳的反应性能.相比之下, Co/SBA-15催化剂的催化性能较差(图 9(B)).在相同的反应条件下, 乙醇转化率从初始的70.2%降至57.5%且CO2选择性由14.7%降到12.6%, 并伴随着数值相对较高的乙醛选择性7.79%, 这表明催化剂的断裂C—C键功能减弱.与此同时, H2的选择性由最佳的74.9%降至68.6%, CH4和CO有略微的升高, 催化剂的活性降低, 催化剂有了明显的失活现象[5].测试结果表明, 载体骨架中Ce金属的加入在一定程度上提高了催化剂的催化性能。突出表现为Ce的存在抑制了活性金属的烧结, 减少积碳的产生(见下文2.6.3), 体现了它储放氧的功能, 使得催化剂保持更好的稳定性.
|
图 9 催化剂在500 ℃条件下的稳定性测试 Fig.9 Catalysts stability testing under 500 ℃ reaction conditions (A) Co/Ce-SBA-15; (B) Co/SBA-15 |
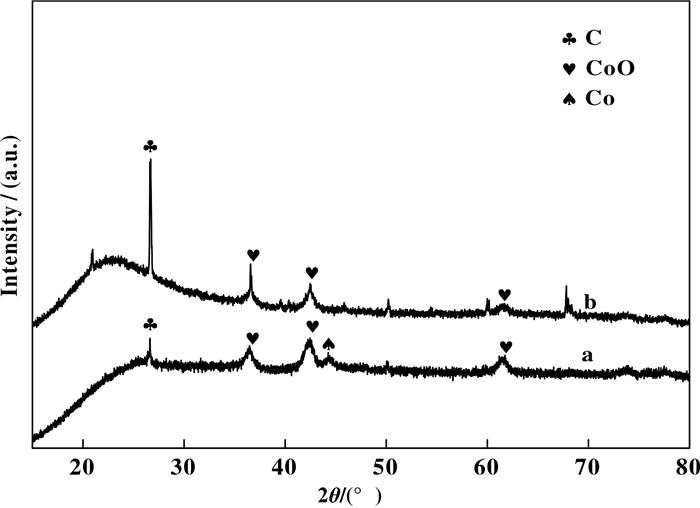
图 10是Co/Ce-SBA-15(20)和Co/SBA-15催化剂稳定性测试后的XRD谱图, Co/SBA-15催化剂谱图中显示出明显的C(2θ=26.7°)的特征衍射峰, 表明催化剂失活的主要原因是由于积碳的生成, 其覆盖在催化剂表面, 阻碍了反应物与活性组分的接触[22].而反应后的Co/Ce-SBA-15(20)催化剂谱图中并没有出现明显的C物质晶面, 这主要是骨架中的金属Ce充分发挥其储放氧的作用, 释放出氧组分, 与反应中生成的C物质结合生成相应的气体产物, 减少了积碳的生成.反应前的H2还原处理将催化剂中的Co3O4还原为CoO, 经计算可得反应后Co/SBA-15催化剂中的CoO平均晶粒尺寸为22.07 nm, Co/Ce-SBA-15(20)催化剂中的CoO平均晶粒尺寸为13.82 nm, 这说明金属Ce的加入降低了活性金属组分的烧结程度.
|
图 10 反应后催化剂的XRD谱图 Fig.10 XRD patterns of cataiysts Co/Ce-SBA-15 (a) and Co/SBA-15(b) after reaction |
图 11是Co/Ce-SBA-15(20)和Co/SBA-15催化剂18 h热稳定性测试后的TG-DTA测试结果, 各催化剂的主要失重量是由于催化剂表面的积碳分解氧化引起的, 如图所示, 不同积碳催化剂进行烧碳实验后显示出的差热峰存在稍许差异, 归纳起来, 这些失重峰出现在3个温度范围内.在100 ℃附近出现失重峰, 归于催化剂表面结晶水的去除[23]. Co/SBA-15在440 ℃附近出现第2个失重峰, 而Co/Ce-SBA-15在300 ℃附近出现第2个失重峰, 最后两者均在550 ℃附近出现第3个失重峰, 由文献可知[24], 反应性能较高的积碳燃烧放热峰出现在240~300 ℃之间, 次高的出现在300~500 ℃之间, 反应性能最差的出现在500~600 ℃之间.由此可得由于金属Ce的加入减少了低反应性能积碳的产生, 进一步提高了催化剂使用的可持续性.数据对比发现, Co/Ce-SBA-15(20)催化剂含碳量仅为5.6%, 而Co/SBA-15催化剂在相同反应时间内的含碳量达15.6%.这表明载体中金属Ce在去除积碳方面得到充分的发挥, 有效的抑制了积碳的形成, 使得催化剂展现出良好的稳定性和催化活性.

|
图 11 反应后催化剂的TG-DTA分布图 Fig.11 TG-DTA profiles of cataiysts Co/SBA-15 (a) and Co/Ce-SBA-15(b) after reaction |
金属改性后的SBA-15在乙醇水蒸气重整制氢中表现出良好的催化活性.
(1) 通过水热法合成的Ce-SBA-15催化剂载体, 各表征结果表明部分金属Ce进入分子筛骨架, 均匀地分布在分子筛中.
(2) 以Ce-SBA-15为载体的催化剂Co/Ce-SBA-15在反应中体现出良好的催化性能.其中主要是金属Ce的储放氧功能, 在反应中减少积碳的生成和降低活性物质烧结方面发挥了重要作用.同时在物料摩尔比n(Si/Ce)为20时, 适量的金属Ce与金属Co之间存在良好的协同作用, 大大提高了Co物种的分散度, 使得反应效果最佳, H2选择性可达75.5%, 乙醇转化率可达96.6%, 反应后积碳率仅为5.6%.
| [1] | He Jian-ping(贺建平), Zhang Lei(张磊), Chen Lin(陈琳), et al. Effect of CeO2 on Cu/Zn-Al catalysts derived from hydrotalcite precursor for methanol steam reforming(CeO2改性Cu/Zn-Al水滑石衍生催化剂对甲醇水蒸气重整制氢性能的影响)[J]. Chem J Chin Univer(高等学校化学学报), 2017, 38(10): 1822–1828. DOI:10.7503/cjcu20170158 |
| [2] | Martono E, Vohs J M. Support effects in cobalt-based ethanol steam reforming catalysts:Reaction of ethanol on Co/CeO2/YSZ (100) model catalysts[J]. J Catal, 2012, 291: 79–86. DOI:10.1016/j.jcat.2012.04.010 |
| [3] | Li Xing(李星), Li Bao-ru(李宝茹), Xie Xian-mei(谢鲜梅), et al. The preparation of modified montmorillonite catalyst and study on the catalytic properties for ethanol dehydration to ethylene(改性蒙脱土催化剂制备及催化低浓度乙醇脱水制乙烯研究)[J]. J Mol Catal(分子催化), 2018, 32(2): 107–116. |
| [4] | Ni M, Leung D Y C, Leung M K H. A review on reforming bio-ethanol for hydrogen production[J]. Int J Hydrogen Energ, 2007, 32(15): 3238–3247. DOI:10.1016/j.ijhydene.2007.04.038 |
| [5] | Mattos L V, Jacobs G, Davis B H, et al. Production of hydrogen from ethanol:Review of reaction mechanism and catalyst deactivation[J]. Chem Rev, 2012, 112(7): 4094–4123. DOI:10.1021/cr2000114 |
| [6] | Llorca J, Piscina P R, Dalmon J A, et al. CO-free hydrogen from steam-reforming of bioethanol over ZnO-supported cobalt catalysts:Effect of the metallic precursor[J]. Appl Catal B Environ, 2003, 43(4): 355–369. DOI:10.1016/S0926-3373(02)00326-0 |
| [7] | Wang H, Ye J L, Liu Y, et al. Steam reforming of ethanol over Co3O4/CeO2 catalysts prepared by different methods[J]. Catal Today, 2007, 129(3/4): 305–312. |
| [8] | Zeng Liang-peng(曾良鹏), Huang Fan(黄樊), Zhu Xing(祝星), et al. Chemical looping conversion of methane over CeO2-based and Co3O4-based Co3O4-CeO2 oxygen carriers:Controlling of product selectivity(铈基与钴基Co3O4-CeO2氧载体上甲烷化学链转化特性:产物选择性控制)[J]. Chem J Chin Univer(高等学校化学学报), 2017, 38(1): 115–125. |
| [9] | Wang Zhi-cai(王知彩), Yang Hong-bing(杨红兵), Gu Shun-ming(谷顺明), et al. Catalytic performance of CeO2 modified Ag-V2O5/TiO2on the oxidation demethylation of methylpyridine(CeO2改性Ag-V2O5/TiO2催化剂的甲基吡啶氧化脱甲基性能)[J]. J Mol Catal(分子催化), 2018, 32(2): 126–132. |
| [10] | Ferencz Z, Erdohelyi A, Baán K, et al. Effects of support and Rh additive on Co-based catalysts in the ethanol steam reforming reaction[J]. ACS Catal, 2014, 4(4): 1205–1218. DOI:10.1021/cs500045z |
| [11] | Xu X, Li J, Hao Z, et al. Characterization and catalytic performance of Co/SBA-15 supported gold catalysts for CO oxidation[J]. Mater Res Bull, 2006, 41(2): 406–413. DOI:10.1016/j.materresbull.2005.08.003 |
| [12] | Mu Z, Li J J, Tian H, et al. Synthesis of mesoporous Co/Ce-SBA-15 materials and their catalytic performance in the catalytic oxidation of benzene[J]. Mater Res Bull, 2008, 43(10): 2599–2606. DOI:10.1016/j.materresbull.2007.10.037 |
| [13] | Shen W, Dong X, Zhu Y, et al. Mesoporous CeO2 and CuO-loaded mesoporous CeO2:Synthesis, characterization, and CO catalytic oxidation property[J]. Micro Mes Mater, 2005, 85(1/2): 157–162. |
| [14] | Wang K, Li X, Ji S, et al. Effect of Cex Zr1-x O2 promoter on Ni-based SBA-15 catalyst for steam reforming of methane[J]. Energ Fuel, 2008, 23(1): 25–31. |
| [15] | Murkute A D, Jackson J E, Miller D J. Supported mesoporous solid base catalysts for condensation of carboxylic acids[J]. J Catal, 2011, 278(2): 189–199. DOI:10.1016/j.jcat.2010.12.001 |
| [16] | Handjani S, Marceau E, Blanchard J, et al. Influence of the support composition and acidity on the catalytic pro- perties of mesoporous SBA-15, Al-SBA-15, and Al2O3-supported Pt catalysts for cinnamaldehyde hydrogenation[J]. J Catal, 2011, 282(1): 228–236. DOI:10.1016/j.jcat.2011.06.017 |
| [17] | Dai Q, Wang X, Chen G, et al. Direct synthesis of cerium (Ⅲ)-incorporated SBA-15 mesoporous molecular sieves by two-step synthesis method[J]. Micro Mes Mater, 2007, 100(1/3): 268–275. |
| [18] | Naik B, Hazra S, Prasad V S, et al. Synthesis of Ag nanoparticles within the pores of SBA-15:an efficient catalyst for reduction of 4-nitrophenol[J]. Catal Commun, 2011, 12(12): 1104–1108. DOI:10.1016/j.catcom.2011.03.028 |
| [19] | Zhao M, Tamara L, Andrew T. SBA-15 supported Ni-Co bimetallic catalysts for enhanced hydrogen production during cellulose decomposition[J]. Appl Catal Benviron, 2010, 10(24): 1016–1025. |
| [20] | Carrasco J, López-Durán D, Liu Z, et al. In situ and theoretical studies for the dissociation of water on an active Ni/CeO2 catalyst:Importance of strong metal-support interactions for the cleavage of O-H bonds[J]. Angew Chem Int Edit, 2015, 54(13): 3917–3921. DOI:10.1002/anie.201410697 |
| [21] | Liu X, Park M, Kim M G, et al. Integrating NiCo alloys with their oxides as efficient bifunctional cathode catalysts for rechargeable zinc-air batteries[J]. Angew Chem Int Edit, 2015, 54(33): 9654–9658. DOI:10.1002/anie.v54.33 |
| [22] | Yishuang Wang, Mingqiang Chen, Zhonglian Yang, et al. Bimetallic Ni-M (M=Co, Cu and Zn) supported on attapulgite as catalysts for hydrogen production from glycerol steam reforming[J]. Appl Catal Agen, 2018, 2018(550): 214–227. |
| [23] | Quek X Y, Liu D, Cheo W N E, et al. Nickel-grafted TUD-1 mesoporous catalysts for carbon dioxide reforming of methane[J]. Appl Catal B:Environ, 2010, 95(3/4): 374–382. |
| [24] | Wang Hong(王红). The study on Co/CeO2catalysts for steam reforming of ethanol(用于乙醇水蒸气重整Co/CeO2催化剂的研究)[D]. Tianjin: Tianjin University(天津: 天津大学), 2007. |
 2019, Vol. 33
2019, Vol. 33


