2. 河南师范大学 环境学院, 黄淮水环境与污染防治省部共建教育部重点实验室, 河南省环境污染控制重点实验室, 河南 新乡 453007
2. School of Environmental, Henan Normal University, Key Laboratory for Yellow River and Huaihe River Water Environment and Pollution Control, Ministry of Education, Henan Key Laboratory for Environmental Pollution Control, Xinxiang 453007, China
开发绿色、环境友好的有机合成技术已经成为了全球性的研究热点, 其中醇类化合物选择性氧化制醛是有机合成中的重要组成部分, 在实验室和工业上均有着至关重要的意义[1].近年来, g-C3N4由于其独特的电子结构、高的化学和热稳定性等诸多优点, 备受青睐[2].然而, g-C3N4半导体材料受到较小的比表面积、较窄的可见光响应范围和较高的光生电子-空穴复合率所限制, 仍需进一步的改进和完善.截至目前, 科学家们通过多种方法改进g-C3N4的光催化性能, 如微观结构调整、元素掺杂、半导体复合和贵金属负载等[3-11].贵金属金、铂、钯等作为催化剂可以改变化学反应速率, 由于它们的d电子轨道未被填满, 在其表面容易吸附反应物, 有利于参与产物的生成, 具有较高的催化活性[12-13].研究人员将负载贵金属催化剂用于有机合成中苯甲醇的选择性氧化反应并取得了较为理想的效果[14-18].例如, Wang等[14]通过浸渍-还原法将金、钯双金属纳米粒子负载在MgAl-LDH表面, 在可见光下将苯甲醇选择性氧化成苯甲醛.结果显示Au9-Pd1/LDH具有高效的光催化活性, 5 h内苯甲醇的转化率可达91.1%, 苯甲醛的选择性为99%. Ma等[15]采用浸渍法制备了不同银含量的Ag/SBA-15催化剂, 对苯甲醇在气相中选择性氧化制苯甲醛, 结果表明银纳米粒子的负载有效地提高了SBA-15催化剂的比表面积, 苯甲醇转化率和苯甲醛选择性分别达到了87%和95%.
通过硼氢化钠还原法制得Ag/g-C3N4、Pd/g-C3N4和Ag-Pd/g-C3N4光催化剂, 并在室温和水溶液中选择性氧化苯甲醇.在5 W LED(λ>400 nm)灯的照射下, 考察不同实验条件下对苯甲醇的转化率及选择性的影响.实验结果表明, Ag-Pd/g-C3N4光催化材料比纯的g-C3N4展现出了更加优异的光催化性能.
1 实验材料和方法 1.1 催化剂合成 1.1.1 块状g-C3N4的合成以二氰二胺为前驱体通过热聚合制备石墨相氮化碳(g-C3N4).将3.0 g二氰二胺放入石英舟, 在马弗炉中氮气氛围下以2.8 ℃ min-1的速率从室温升至550 ℃, 保持4 h.热聚合反应结束之后, 将石英舟取出, 自然冷却至室温, 然后将得到的黄色产品研磨均匀, 放入烘箱中60 ℃干燥过夜, 最终得到黄色粉末的块状g-C3N4[19].
1.1.2 Ag/g-C3N4、Pd/g-C3N4、Ag-Pd/g-C3N4光催化剂的合成Ag/g-C3N4、Pd/g-C3N4和Ag-Pd/g-C3N4光催化剂采用硼氢化钠还原法制备得到.具体操作如下:称取200 mg石墨相氮化碳(g-C3N4)溶解于20 mL去离子水中, 超声0.5 h, 然后分别加入1.7 mL浓度为2 mg/mL的硝酸银或1.77 mL浓度为2 mg/mL的氯化钯水溶液(Pd/g-C3N4), 或分别加入上述两种溶液(Ag-Pd/g-C3N4), 磁力搅拌2 h, 然后逐滴加入3 mL 0.5 mol/L的硼氢化钠水溶液, 离心之后用乙醇和水分别洗涤3次, 最后在80 ℃干燥12 h.
1.2 催化剂表征催化剂的微观形貌结构通过日本电子公司JEOL生产的JEM-2100型超高分辨透射电子显微镜进行观察.利用德国Brukeraxs布鲁克(Bruker)公司生产的, 型号为D8 Advance的X-射线衍射仪来对材料的晶体结构进行分析, 其中X-射线源为Cu Kα (λ = 0.154 06 nm), 加速电压和发射电流分别为35 kV和25 mA, 2θ扫描范围为10°~90°, 扫描速度0.02°/0.4 s.表面元素种类及元素状态通过赛默飞世尔科技公司生产, 型号为ESCALA260Xi, 辐射源为Al Kα射线的X射线光电子能谱进行分析.通过美国珀金埃尔默公司生产的型号为Lambd 950紫外可见近红外光谱仪测定材料的紫外-可见漫反射光谱, 以BaSO4为参比, 扫描光谱的范围为200~800 nm.苯甲醇和苯甲醛的浓度通过美国Waters公司生产的型号为Waters1525-2998的高效液相色谱仪进行检测, 其中色谱柱为C18(5 μm, 4.6×150 mm), 检测器为PDA检测器.
1.3 选择性氧化苯甲醇选择性氧化苯甲醇反应是在多通道光催化反应系统(PCX50B)进行.该仪器能够同时进行九组反应, 采用磁子悬浮搅拌以及底部光盘旋转照射的方式, 在进行多组实验的同时, 减少了因光照强度不均匀、搅拌不充分所带的误差.苯甲醇选择性氧化的具体过程如下:一定量的催化剂和0.1 g Na2CO3分散在含有50 mL苯甲醇(10 mg/L)溶液的反应瓶中, 超声混合均匀后固定在光催化反应装置上.室温下, 打开设备开关.在反应过程中, 在一定的间隔时间取出样品溶液离心, 取上清液过滤后用高效液相色谱仪测定苯甲醇和苯甲醛的浓度(注射体积: 20 μm, 流动相中的水:甲醇= 60:40, 柱温: 35 ℃, 运行时间: 10 min, 在211和250 nm的检测波长下分别检测苯甲醇和苯甲醛的浓度.
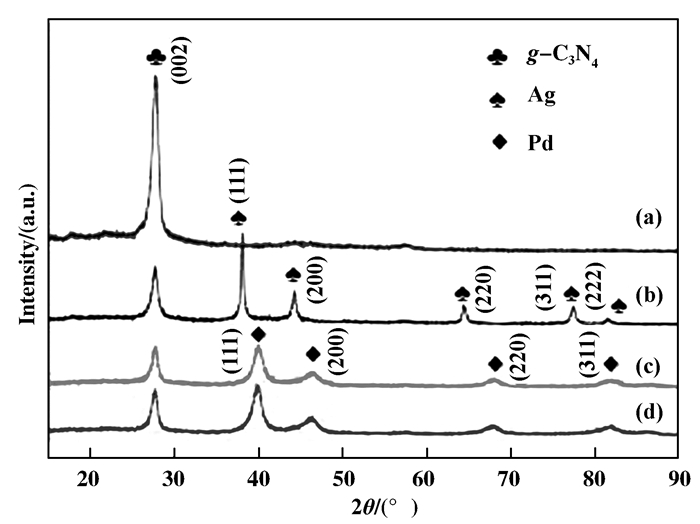
2 结果与讨论 2.1 XRD分析所制备样品的晶体结构和组成通过X射线衍射(XRD)来分析. 图 1是g-C3N4, Ag/g-C3N4, Pd/g-C3N4和Ag-Pd/g-C3N4复合材料的XRD图, 由图 1可看出, 所制备的Ag/g-C3N4和Pd/g-C3N4(图 1b、c)中银和钯的衍射数据分别与标准卡片银(JCPDS card No.04-0783和钯(JCPDS card No. 46-1043)相吻合[20-22]. Ag/g-C3N4复合材料在2θ等于38.4°、44.1°、63.9°、77.3°、81.4°处出现了较强的衍射峰, 分别对应于银的(111)、(200)、(220)、(311)、(222)晶面[23]. Pd/g-C3N4复合材料在2θ等于40.4°、46.4°、67.8°、82.1°处出现了较强的衍射峰, 分别对应于钯的(111)、(200)、(220)、(311)晶面[24].从图 1d中可以看出, AgPd特征衍射峰(111)(2θ=39.8°)位于Ag(111)(2θ=38.4°)和Pd (111)(2θ=40.4°)之间, 证明了双金属银钯纳米颗粒成功地负载在g-C3N4的表面上[18].
|
图 1 g-C3N4(a)、Ag/g-C3N4(b)、Pd/g-C3N4 (c)和Ag-Pd/g-C3N4(d)复合材料的XRD图谱 Fig.1 XRD patterns of g-C3N4(a)、Ag/g-C3N4(b)、Pd/g-C3N4(c)和Ag-Pd/g-C3N4(d) composites |
图 2是g-C3N4, Ag/g-C3N4, Pd/g-C3N4和Ag-Pd/g-C3N4复合材料的HR-TEM图, 图 2a是g-C3N4的HR-TEM图, 从图 2中可以看出g-C3N4呈表面光滑的块状结构.如图 2(b)和(c)所示, 银和钯纳米颗粒分别负载在g-C3N4的表面上.从图 2 (d)和(e)中可以看出, 在g-C3N4的表面同时负载着银和钯两种纳米颗粒, 可以清楚地观察到宽度为0.241和0.225 nm的晶格条纹, 分别对应于银晶体中的(200)和钯晶体中(111)晶面间距.通过EDS点扫能谱(图 2f)进一步说明Ag-Pd/g-C3N4复合材料有C、N、Ag和Pd元素存在, 其中, Ag-Pd/g-C3N4复合材料中C、N、Ag和Pd元素的质量百分数分别为22.718%、59.966%、9.132%和8.184%.

|
图 2 g-C3N4(a), Ag/g-C3N4(b), Pd/g-C3N4(c), Ag-Pd/g-C3N4(d) (e)的HR-TEM图以及Ag-Pd/g-C3N4(f)的EDS图 Fig.2 HR-TEM images of the g-C3N4(a), Ag/g-C3N4(b), Pd/g-C3N4(c), Ag-Pd/g-C3N4(d)(e) and EDS spectrum(f) |
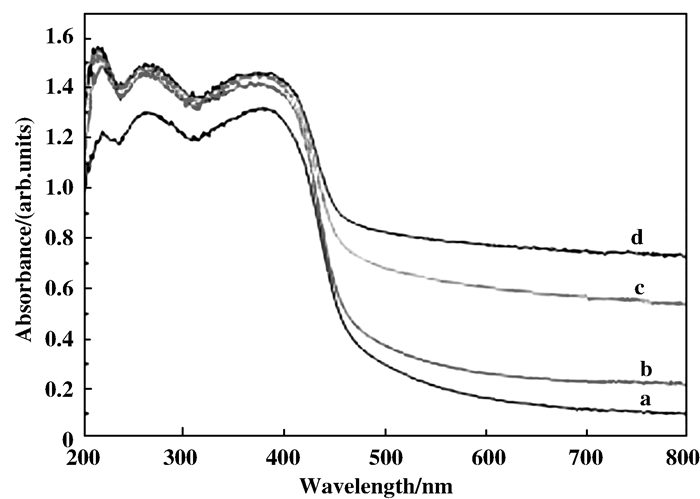
图 3为材料g-C3N4、Ag/g-C3N4、Pd/g-C3N4和Ag-Pd/g-C3N4的紫外可见漫反射光谱图.从图 3中可以看出, 所制备的复合材料样品在可见区均有吸收, 且负载Ag和Pd后, 材料在可见区的吸收明显增强, 共同负载的Ag-Pd/g-C3N4的吸收最强.从图 3可知, g-C3N4的最大吸收边在465 nm左右, Ag/g-C3N4、Pd/g-C3N4、Ag-Pd/g-C3N4的最大吸收边分别在472、480和495 nm, 半导体带隙宽度可以根据以下计算公式得到:
|
图 3 g-C3N4(a), Ag/g-C3N4(b), Pd/g-C3N4(c), Ag-Pd/g-C3N4(d)的紫外-可见漫反射光谱图 Fig.3 Ultraviolet - visible diffuse reflectance spectra of the g-C3N4(a), Ag/g-C3N4(b), Pd/g-C3N4(c), Ag-Pd/g-C3N4(d) |
| $ {\left( {\alpha hv} \right)^{n/2}} = A\left( {hv - Eg} \right) $ |
式中: α为吸收系数, hv为光子能量, Eg为禁带宽度, A是一个常值.指数n与半导体类型直接相关, 对于直接带隙半导体而言, n=1/2, 而对于间接带隙半导体, n=2.本实验中计算的g-C3N4为直接带隙半导体, 故n=1/2.通过(αhv)2对(hv)作图, 得到的图形直线部分延长至X轴, 交点处对应的值即为该半导体的禁带宽度.根据图 3, 可以估算出g-C3N4、Ag/g-C3N4、Pd/g-C3N4和Ag-Pd/g-C3N4的带隙值分别约为2.67、2.63、2.59和2.51 eV.Ag/g-C3N4、Pd/g-C3N4和Ag-Pd/g-C3N4在可见光区域对光的吸收明显增强, 而光吸收边发生了些许“红移”现象, 可能是负载银和钯纳米颗粒造成的.
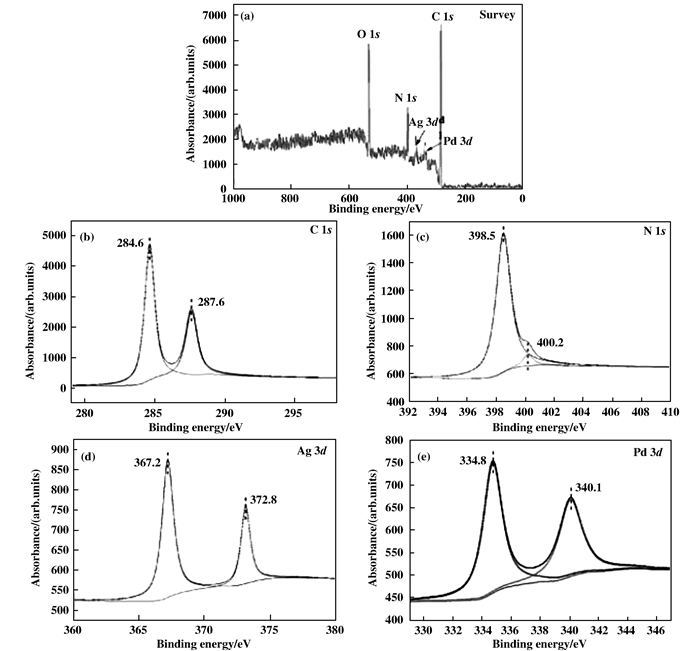
2.4 XPS分析为了进一步分析复合材料的元素组成和电子结构, 我们对Ag-Pd/g-C3N4复合材料进行了X射线光电子能谱测试. 图 4显示了Ag-Pd/g-C3N4复合材料的XPS全谱和复合物中每种元素的高分辨图谱.从图 4(a)可以看出, 结合能在291.08、403.08、540.08、376.08和347.08 eV的强峰分别对应C 1s、N 1s、O 1s、Ag 3d和Pd 3d的特征峰, 说明样品中含有C、N、O、Ag和Pd元素.并且, 在C 1s的图谱4(b)中, 结合能为284.6和287.6 eV处, 其中, 位于284.6 eV的峰归属于石墨相中C—C键, 287.6 eV对应于N—C=N中sp2杂化的C键的结合能[25-26].图 4(c)中元素N 1s的结合能位于398.5和400.2 eV处, 其中398.5 eV可归属于C=N—C结构中的N链接两个C元素的sp2键, 400.2 eV对应的是g-C3N4中N≡C的结合能[27].此外, 元素Ag 3d的高分辨图谱(如图 4(d))显示在367.2和372.8 eV处出现了特征信号峰, 分别对应于Ag 3d5/2和Ag 3d3/2的自旋轨道[28]. 图 4(e)是元素Pd 3d的特征信号峰, 位于334.8和340.1 eV处, 分别归属于Pd 3d5/2和Pd 3d3/2的自旋轨道[29].
|
图 4 Ag-Pd/g-C3N4复合材料的XPS图谱全谱(a), C 1s(b), N 1s(c), Ag 3d(d), Pd 3d(e)的高分辨谱图 Fig.4 XPS spectra of the Ag-Pd/g-C3N4 survey scan of Ag-Pd/g-C3N4 (a). High-resolution spectra of C 1s (b), N 1s (c), Ag 3d (d) and Pd 3d (e) |
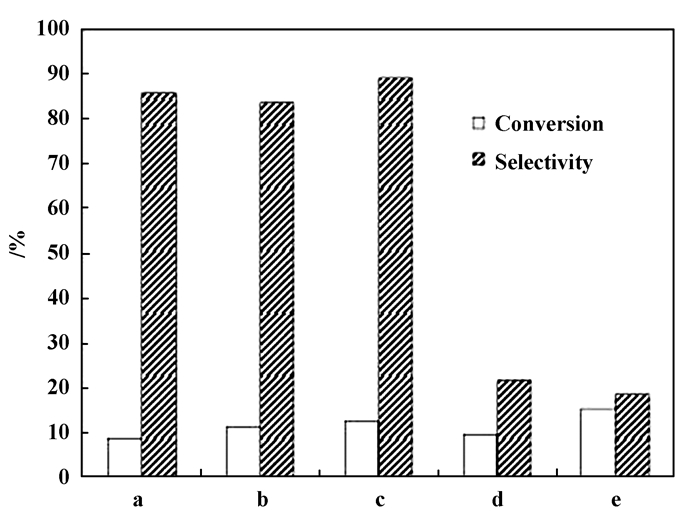
为了评估所制复合材料的催化活性, 使用苯甲醇水溶液为目标物, 在5 W LED(λ>400 nm)灯下进行了苯甲醇选择性氧化反应. 图 5分别是材料g-C3N4、Ag/g-C3N4、Pd/g-C3N4、Ag-Pd/g-C3N4在不通氧气和通氧气条件下对苯甲醇选择性氧化反应的结果.由图 5可知, 在不通氧气下, Pd/g-C3N4的苯甲醇转化率最高, 达到了12.4%.材料g-C3N4、Ag/g-C3N4、Pd/g-C3N4、Ag-Pd/g-C3N4对生成苯甲醛的选择性分别为76.9%、80.6%、77.8%和85.6%.因此在不通氧气下, Ag/g-C3N4、Pd/g-C3N4、Ag-Pd/g-C3N4复合材料的选择性优于g-C3N4, 并且Ag-Pd/g-C3N4复合材料的选择性最高.

|
图 5 选择性氧化苯甲醇反应 Fig.5 Selective oxidation of benzyl alcohol |
在通入氧气下, 苯甲醇的转化率比不通氧气条件下提高很多, 其中, Pd/g-C3N4的转化率最高, 达到了25.6%.而苯甲醛的选择性却比不通氧气条件下有所降低, 材料g-C3N4、Ag/g-C3N4、Pd/g-C3N4、Ag-Pd/g-C3N4的选择性分别为53.6%、65.1%、50.1%和79.2%.因此, 通入氧气虽然可以提高苯甲醇的转化率, 但是生成苯甲醛的选择性却降低了.
另外, 研究了加入少量有机溶剂对苯甲醇选择性氧化反应的影响.从图 6中可以看出, 添加有机溶剂对苯甲醇的转化率影响不大, 但对苯甲醛的选择性影响显著.在添加三氟甲苯和三氯甲烷后, 苯甲醛的选择性从85.6%降到了20%左右, 在添加乙腈之后, 苯甲醛的选择性出现了略微地降低, 而添加乙醚之后, 苯甲醛的选择性则出现了略微地提高.结果显示, 添加三氟甲苯、三氯甲烷和乙腈对苯甲醇选择性反应有抑制作用, 而添加乙醚对反应有着促进作用.
|
图 6 不同有机溶剂(a.无; b.乙腈; c.乙醚; d.三氟甲苯; e.三氟甲烷)下Ag-Pd/g-C3N4复合材料对选择性氧化苯甲醇(反应条件: 50 mL苯甲醇溶液(10 mg/L), 50 mg催化剂, 0.1 g碳酸钠, LED灯(1.0 A), 3 h) Fig.6 Selective oxidation of benzyl alcohol by Ag-Pd/g-C3N4 composites under different organic solvents (reaction conditions: 50 mL benzyl alcohol solution (10 mg/L), 50 mg catalyst, 0.1 g sodium carbonate, LED lamp (1.0 A)), (a. None; b.Acetonitrile; c. Diethyl ether; d. Trifluorotoluene; e. Trifluoromethane) |
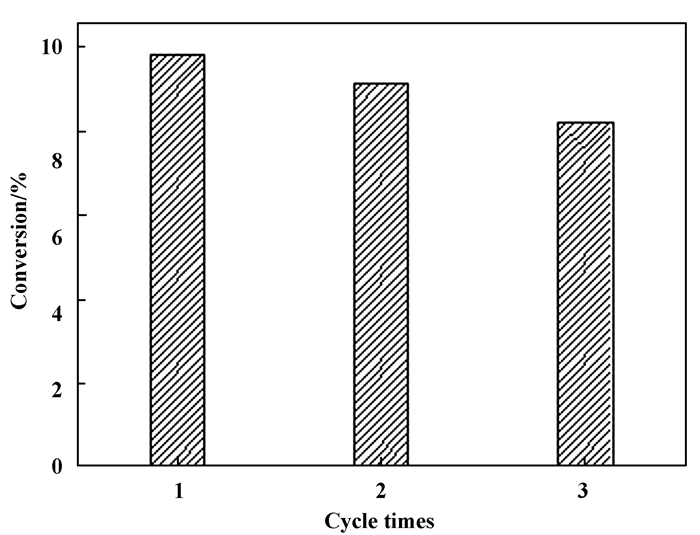
Ag-Pd/g-C3N4作为催化剂氧化苯甲醇的稳定性如图 7所示.实验将反应后的Ag-Pd/g-C3N4从混合物中离心分离, 干燥后重复使用3次, 在不通入氧气的情况下, 苯甲醇的转化率由原来的9.8%减少到8.2%, 表现出良好的稳定性.
|
图 7 三次循环使用Ag-Pd/g-C3N4催化氧化苯甲醇的转化率 Fig.7 Conversions of catalytic oxidation of benzyl alcohol using Ag-Pd/g-C3N4 for three cycles |
为了研究选择性氧化苯甲醇反应过程中的活性基团, 我们对不通氧气的反应体系进行了一系列的自由基捕获实验.在选择性氧化苯甲醇反应中分别加入3种活性物种:乙二胺四乙酸二钠(EDTA-Na2)、异丙醇(IPA)和1, 4-苯醌(BQ), 用于捕获空穴(h+)、羟基自由基(·OH)和超氧自由基(·O2-).结果如图 8(a)所示, 随着EDTA-Na2、IPA和BQ的加入, 苯甲醛的选择性都有明显的降低, 说明·O2-, ·OH和h+在选择性氧化苯甲醇反应中均起着重要的作用.

|
图 8 电子自旋共振波谱信号DMPO- O2·- (a), DMPO- h+ (b), DMPO- OH· (c)和一系列捕获剂对选择性氧化苯甲醇反应的影响(d) Fig.8 ESR signals of the DMPO- O2·- (a), the DMPO- h+ (b), the DMPO- OH· (c) and Effects of a series of scavengers on the selective oxidation of benzyl alcohol (d) |
为了检验上述结果, 对反应体系进行了电子自旋共振(ESR)测试.通过用5, 5-二甲基吡咯啉-1-氧化物(DMPO)自旋电子捕获剂与自由基形成相对稳定的自由基生成物, 利用电子自旋共振波谱仪(ESR)对自由基进行测定.如图 8(b)和(c)所示, 在黑暗中没有观察到O2·-和OH·信号.在模拟太阳光照射下, DMPO·O2-和DMPO·OH的特征峰的强度比为1:1:1:1和1:2:2:1, 并且随着光照时间的延长, ·O2-和·OH信号不断地增强, 表明·O2-和·OH信号是苯甲醇选择性氧化反应的关键活性物种.而从图 8(d)中可以看出, h+信号在黑暗中即可以观察到, 光照之后, h+信号随着时间的推移增强, 但增强幅度不明显, 与自由基捕获实验结果一致.因此, ·O2-, ·OH和h+都是选择性氧化苯甲醇反应的主要自由基, 其作用顺序为:·O2->·OH>h+.
3 结论采用硼氢化钠还原法成功地将Ag和Pd纳米颗粒负载在g-C3N4表面, 制备了Ag/g-C3N4、Pd/g-C3N4和Ag-Pd/g-C3N4复合材料.负载银和钯纳米颗粒可以提高材料对可见光的吸收能力, 同时减少光生电子和空穴的复合, 从而提高其催化活性.在可见光照、室温和水溶液中氧化苯甲醇的结果显示, 在不通氧气条件下, Ag-Pd/g-C3N4复合材料的催化效果最好, 对生成苯甲醛的选择性可达85.6%, 添加少量乙醚可以提高其选择性.自由基捕获实验表明, O2·-, OH·和h+是选择性氧化苯甲醇反应体系中的主要活性物种.我们探索了一种环境友好、节能的(可见光照射、室温、水溶液)苯甲醛合成途径, 并取得了较好的结果, 在工业上有着潜在的广阔应用前景.
| [1] |
a. Gu Y, Li C, Bai J, et al. Construction of multivariate functionalized heterojunction and its application in selective oxidation of benzyl alcohol[J]. J Photochem Photobiol A: Chem, 2018, 351: 87-94. b. Liu Lu(刘璐), Zheng Cheng-hang(郑成航), Gao Xiang(高翔). Effect of discharge atmosphere on structure and performance of composite metal oxides catalysts(放电气氛对复合金属氧化物催化剂结构和活性的影响)[J]. J Mol Catal(China)(分子催化), 2018, 32(1): 54-62. c. Li He-jian(李和健), Wu Cang-cang(吴藏藏), Zheng Li(郑丽), et al. Selective catalytic oxidation of benzyl alcohol over Cu-BTC and its derivatives(Cu-BTC及其衍生物在苯甲醇选择氧化反应中的催化活性)[J]. J Mol Catal(China)(分子催化), 2017, 31(4): 341-347. |
| [2] | Cao S, Low J, Yu J, et al. Polymeric photocatalysts based on graphitic carbon nitride[J]. Adv Mater, 2015, 27(13): 2150–2176. DOI:10.1002/adma.201500033 |
| [3] | Bai X, Wang L, Zong R, et al. Photocatalytic activity enhanced via g-C3N4 nanoplates to nanorods[J]. J Phys Chem C, 2013, 117(19): 9952–9961. DOI:10.1021/jp402062d |
| [4] | Zhan T, Tan Z, Wang X, et al. Hemoglobin immobilized in g-C3N4 nanoparticle decorated 3D graphene-LDH network:Direct electrochemistry and electrocatalysis to trichloroacetic acid[J]. Sens Actu B:Chem, 2018, 255: 149–158. DOI:10.1016/j.snb.2017.08.048 |
| [5] | Novoselov K S, Geim A K, Morozov S V, et al. Electric field effect in atomically thin carbon films[J]. Science, 2004, 306(5696): 666–669. DOI:10.1126/science.1102896 |
| [6] | Niu P, Zhang L, Liu G, et al. Graphene-like carbon nitride nanosheets for improved photocatalytic activities[J]. Adv Func Mater, 2012, 22(22): 4763–4770. DOI:10.1002/adfm.v22.22 |
| [7] | Yang S, Gong Y, Zhang J, et al. Exfoliated graphitic carbon nitride nanosheets as efficient catalysts for hydrogen evolution under visible light[J]. Adv Mater, 2013, 25(17): 2452–2456. DOI:10.1002/adma.v25.17 |
| [8] | Dong G, Zhang L. Porous structure dependent photoreactivity of graphitic carbon nitride under visible light[J]. J Mater Chem, 2012, 22(3): 1160–1166. DOI:10.1039/C1JM14312C |
| [9] | Chen X, Zhang J, Fu X, et al. Fe-g-C3N4-catalyzed oxidation of benzene to phenol using hydrogen peroxide and visible light[J]. J Amer Chem Soc, 2009, 131(33): 11658–11659. DOI:10.1021/ja903923s |
| [10] | Liu G, Niu P, Sun C, et al. Unique electronic structure induced high photoreactivity of sulfur-doped graphitic C3N4[J]. J Amer Chem Soc, 2010, 132(33): 11642–11648. DOI:10.1021/ja103798k |
| [11] | Lu X, Wang Q, Cui D. Preparation and photocatalytic properties of g-C3N4/TiO2 hybrid composite[J]. J Mater Sci & Technol, 2010, 26(10): 925–930. |
| [12] | Mounguengui-Diallo M, Vermersch F, Perret N, et al. Base free oxidation of 1, 6-hexanediol to adipic acid over supported noble metal mono-and bimetallic catalysts[J]. Appl Catal A:Gener, 2018, 551: 88–97. DOI:10.1016/j.apcata.2017.12.005 |
| [13] | Nagajyothi P C, Pandurangan M, Vattikuti S V P, et al. Enhanced photocatalytic activity of Ag/g-C3N4 composite[J]. Separ Puri Technol, 2017, 188: 228–237. DOI:10.1016/j.seppur.2017.07.026 |
| [14] | Wang Z, Song Y, Zou J, et al. The cooperation effect in the Au-Pd/LDH for promoting photocatalytic selective oxidation of benzyl alcohol[J]. Catal Sci & Technol, 2018, 8(1): 268–275. |
| [15] | Ma L, Guo X, Xiang L. Catalytic activity of Ag/SBA-15 for low-temperature gas-phase selective oxidation of benzyl alcohol to benzaldehyde[J]. Chin J Catal, 2014, 35(1): 108–119. DOI:10.1016/S1872-2067(12)60720-7 |
| [16] | Verma S, Baig R B N, Nadagouda M N, et al. Visible light mediated upgrading of biomass to biofuel[J]. Green Chem, 2016, 18(5): 1327–1331. DOI:10.1039/C5GC02951A |
| [17] | áNasir Baig R B. A photoactive bimetallic framework for direct aminoformylation of nitroarenes[J]. Green Chem, 2016, 18(4): 1019–1022. DOI:10.1039/C5GC02799C |
| [18] | Yao F, Li X, Wan C, et al. Highly efficient hydrogen release from formic acid using a graphitic carbon nitride-supported AgPd nanoparticle catalyst[J]. Appl Surf Sci, 2017, 426: 605–611. DOI:10.1016/j.apsusc.2017.07.193 |
| [19] | Nikokavoura A, Trapalis C. Graphene and g-C3N4 based photocatalysts for NOx removal:A review[J]. Appl Surf Sci, 2018, 430: 18–52. DOI:10.1016/j.apsusc.2017.08.192 |
| [20] | Xu L, Liu N, Hong B, et al. Nickel-platinum nanoparticles immobilized on graphitic carbon nitride as highly efficient catalyst for hydrogen release from hydrous hydrazine[J]. RSC Adv, 2016, 6(38): 31687–31691. DOI:10.1039/C6RA01335J |
| [21] | Dai H, Xia B, Wen L, et al. Synergistic catalysis of AgPd@ZIF-8 on dehydrogenation of formic acid[J]. Appl Catal B:Envir, 2015, 165: 57–62. DOI:10.1016/j.apcatb.2014.09.065 |
| [22] | Jiang Y, Fan X, Xiao X, et al. Novel AgPd hollow spheres anchored on graphene as an efficient catalyst for dehydrogenation of formic acid at room temperature[J]. J Mater Chem A, 2016, 4(2): 657–666. DOI:10.1039/C5TA09159D |
| [23] | Yurderi M, Bulut A, Zahmakiran M, et al. Carbon supported trimetallic PdNiAg nanoparticles as highly active, selective and reusable catalyst in the formic acid decomposition[J]. Appl Catal B:Environ, 2014, 160: 514–524. |
| [24] | Zhou X, Huang Y, Xing W, et al. High-quality hydrogen from the catalyzed decomposition of formic acid by Pd-Au/C and Pd-Ag/C[J]. Chem Commun, 2008(30): 3540–3542. DOI:10.1039/b803661f |
| [25] | Singh J A, Overbury S H, Dudney N J, et al. Gold nanoparticles supported on carbon nitride:Influence of surface hydroxyls on low temperature carbon monoxide oxidation[J]. ACS Catal, 2012, 2(6): 1138–1146. DOI:10.1021/cs3001094 |
| [26] | Zang Meng-Qiao. C3N4/TiO2 composite photocatalyst for visible light photocatalytic degradation of pollutants[D]. Heilongjiang: Harbin Institute of Technology, 2015. (in Chinese). |
| [27] | Liu J, Zhang T, Wang Z, et al. Simple pyrolysis of urea into graphitic carbon nitride with recyclable adsorption and photocatalytic activity[J]. J Mater Chem, 2011, 21(38): 14398–14401. DOI:10.1039/c1jm12620b |
| [28] | Yang L, Hua X, Su J, et al. Highly efficient hydrogen generation from formic acid-sodium formate over monodisperse AgPd nanoparticles at room temperature[J]. Appl Catal B:Environ, 2015, 168: 423–428. |
| [29] | Wang Z L, Yan J M, Wang H L, et al. Au@Pd core-shell nanoclusters growing on nitrogen-doped mildly reducedgraphene oxide with enhanced catalytic performance for hydrogen generation from formic acid[J]. J Mater Chem A, 2013, 1(41): 12721–1272. DOI:10.1039/c3ta12531a |
 2019, Vol. 33
2019, Vol. 33


