1, 4-丁炔二醇(1, 4-butynediol, 简称BYD)是一种重要的基本化工产品, 其下游产品有1, 4-丁二醇(BDO)、四氢呋喃(THF)、γ-丁内酯(GBL)等一系列高附加值化学品, 被广泛应用于石油加工、聚合材料、合成树脂、杀虫剂等领域.随下游聚酯材料等行业的发展, 对1, 4-丁炔二醇的需求量呈现逐年增长态势[1-5].
BYD的生产采用以甲醛与乙炔为原料的炔醛法工艺, 使用炔化亚铜作为催化剂.工业上, 通常先制备氧化铜或碱式碳酸铜作为催化剂的活性组分前体, 该前体在反应过程中经Cu2+还原为Cu+后与乙炔形成炔化亚铜方显示出催化活性[6-7].针对高性能炔化催化剂的研究, 研究者们[2, 8-10]从提高Cu物种分散度与调控Cu物种可还原性的角度报道了不同载体的CuO基催化剂与孔雀石催化剂, 并采用Bi2O3作为助剂以抑制Cu物种过度还原为金属铜导致的乙炔聚合副反应.近年来, 我们进一步研究发现, 除Bi2O3以外, Fe3O4助剂的引入可以使催化剂呈现可磁性分离的特性, 并作为电子助剂抑制了金属铜的生成[11].借助金红石相Ti2O载体与Cu2O形成的异质结构或N-掺杂Ti2O中Ti3+及形成的氧空位增强了Cu物种与载体相互作用, 不仅分散了Cu物种, 同时稳定了Cu+, 使其高效转化为炔化亚铜活性相[5, 10]. MgO的加入形成了MgO-SiO2复合物, 提高了Cu与载体之间的相互作用, 使Cu物种高度分散并在反应中可控还原为亚铜, 呈现出优异的催化性能[12].前期研究中TiO2相对较低的比表面积限制了CuO负载量的提高, 其对催化活性的提升有限, 而SiO2本身在水相体系中的不稳定, 容易导致催化剂结构破坏造成催化剂稳定性下降.优选更为优异的载体或助剂材料, 仍是甲醛乙炔化催化剂研究的焦点问题. ZnO作为铜基催化剂常用的助剂就被大量用来研究, 通过调变Cu物种的分散度、化学环境、表面酸碱性等性质, 使铜基催化剂在不同的催化反应中表现出优异的催化性能[13-21].
在前期铜基炔化催化剂研究基础上, 进一步制备了CuO-ZnO二元催化体系, 通过改变沉淀剂种类, 调变铜物种与金属氧化物之间的相互作用, 研究催化剂结构与其催化性能间的构效关系规律, 以期获得高活性、高稳定性的甲醛乙炔化催化剂.
1 实验部分 1.1 催化剂的制备采用共沉淀法制备Cu-Zn摩尔比为n(Cu):n(Zn)=2:1的CuO-ZnO催化剂.称取9.7 g Cu(NO3)2·3H2O和6.0 g Zn(NO3)2·6H2O加入到1000 mL三口烧瓶中, 用160 mL蒸馏水溶解, 在65 ℃水浴中用浓度为2.0 mol/L的NaOH溶液在搅拌条件下调节溶液pH至8.0, 老化3 h, 并用蒸馏水离心洗涤3~5次.将离心后的沉淀物置于65 ℃的烘箱内干燥, 然后研磨成粉末在马弗炉中450 ℃焙烧4 h, 即可得到CuO-ZnO催化剂, 标识为CZ(NaOH).其他条件不变, 将NaOH分别替换为Na2CO3与NaHCO3, 制备得到的CuO-ZnO催化剂, 分别标识为CZ(Na2CO3)和CZ(NaHCO3).
1.2 催化剂表征XRD表征在德国Bruker D8 Advance型X射线粉末衍射仪上进行, 使用Cu Kα (λ = 0.154 06 nm)辐射源, 40 kV, 40 mA条件, 2θ的范围为10°~80°, 扫描速率为0.1°·s-1.样品的热重(TG-DTG)测试在NETZSCH STA449C型热分析仪上完成.样品装入样品支架后在20 mL/min N2气氛下, 以10 ℃/min, 升温至800 ℃进行测定.拉曼光谱(Raman spectra)在Horiba Soiontific LabRam HR Evolution型紫外共焦拉曼光谱仪上进行测试, 激光波长为532 nm, 测试功率为0.1 mW. H2-TPR表征采用美国Micromeritics AutoChem Ⅱ 2920化学吸附仪, 30 mg催化剂装入样品管中, 在200 ℃下N2吹扫0.5 h, 降温至30 ℃, 通入H2/N2体积比为5:95的混合气20 mL·min-1, 待基线走平后, 以10 ℃·min-1的速率升温至500 ℃, 采用TCD检测耗氢量.
1.3 催化剂活性评价将所需量的催化剂与甲醛溶液装入圆底烧瓶中, 通N2吹扫0.5 h, 油浴中加热至所需温度, 搅拌条件下通入C2H2气, 反应15 h.反应后的物料降温离心分离后, 采用Agilent 7890A型气相色谱仪进行组份分析, 1, 4-丁二醇作内标物, 色谱柱选用DB-5(0.32 mm × 50 m), 氢火焰离子化检测器(FID), 未反应的甲醛采用碘量法测定[11-12].
2 结果与讨论 2.1 催化剂XRD表征图 1(a)为焙烧前CuO-ZnO催化剂的XRD图, 可以看出, 以NaOH为沉淀剂制备的CZ(NaOH)样品中可明显观察到Cu与Zn的氢氧化物的存在, 分别呈现2θ=35.3°、42.0°处Zn(OH)2的衍射峰, 及2θ=12.7°、25.5°处Cu(OH)2的特征衍射峰.在CZ(Na2CO3)和CZ(NaHCO3)中, 则主要观察到2θ=12.8°、14.8°、17.6°、24.1°处Cu2CO3(OH)2的特征衍射峰, 以及2θ=27.8°、32.6°处Zn5(CO3)2(OH)6衍射峰[22-23].

|
图 1 焙烧前后CuO-ZnO催化剂的XRD图 Fig.1 XRD patterns of CuO-ZnO catalysts before (a) and after (b) calcination |
焙烧后CuO-ZnO催化剂的XRD图示于图 1(b), 可以看出, 分别以NaHCO3及NaOH为沉淀剂制备的CZ(NaHCO3)及CZ(NaOH)样品中2θ=31.6°、47.7°、56.3°、62.4°处观察到尖锐的ZnO特征衍射峰, 2θ=35.5°、38.7°、46.6°、65.8°、71.9°处显示尖锐的CuO特征衍射峰[24], 表明CZ(NaHCO3)及CZ(NaOH)的样品结晶度较高, 形成较为完整的CuO与ZnO颗粒.对比CZ(NaHCO3)与CZ(NaOH)两样品, CZ(NaHCO3)样品中CuO晶相衍射峰更为尖锐, 表明从体相的平均结果分析, CZ(NaHCO3)中CuO具有较CZ(NaOH)更大的晶粒尺寸.而对于CZ(Na2CO3)样品中CuO与ZnO物种峰强度明显降低, 峰形弥散, 且发生位移与在CuO的2θ=35.5°处以及ZnO的2θ=31.6°处的衍射峰出现重叠, 说明Zn进入CuO晶格中, 形成CuO-ZnO固溶体, 产生强相互作用, 这也有效的抑制了CuO颗粒的长大[25].
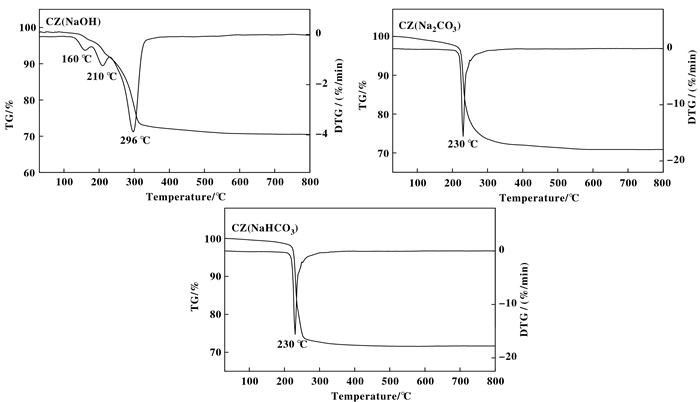
2.2 催化剂TG/DTG表征由图 2催化剂的TG图可以看出, CZ(NaOH)出现了3个明显的失重台阶, 在120~180 ℃范围内出现的失重台阶是由于物理吸附水和以氢键作用的水脱除引起的, 在180~250 ℃之间出现的失重台阶是由于Cu(OH)2分解为CuO所致, 在230~350 ℃之间出现的失重台阶归因于催化剂前驱体中Zn(OH)2分解为ZnO所致[26-27]. Cu与Zn的氢氧化物分解温度的差异, 致使优先生成CuO, 后生成ZnO, 这是CuO与ZnO均以大颗粒形式存在, 且相互作用较弱的主要原因. CZ(Na2CO3)和CZ(NaHCO3)样品均在200~270 ℃范围内出现了一个明显的失重台阶, 归因于Cu2CO3(OH)2和Zn5(CO3)2(OH)6的分解所致[28-29].对照焙烧前CZ(NaHCO3)样品的XRD图发现, Cu2CO3(OH)2及Zn5(CO3)2(OH)6的衍射峰强度较高, 晶粒较为完整, 即使两物种在同一温度区间内分解转化为相应的氧化物, 两氧化物各自呈现大的晶粒尺寸, 并具有弱的相互作用.而对于CZ(Na2CO3)样品, 焙烧前碱式盐物种分散度较高, 在焙烧过程中可产生高分散的CuO与ZnO, 并促使了Zn进入CuO晶格中, 从而呈现出CuO-ZnO固溶体结构.
|
图 2 CuO-ZnO催化剂的TG/DTG图 Fig.2 TG/DTG profiles of CuO-ZnO catalysts |
不同沉淀剂制备的CuO-ZnO催化剂的TEM图如图 3所示. CZ(Na2CO3)催化剂具有分散均匀的氧化物颗粒, 呈现近球形结构(图 3b), 而CZ(NaOH)和CZ(NaHCO3)催化剂中氧化物分散不均匀, 部分颗粒呈现规整的结晶态(图 3a和3c).这与XRD分析结果中CZ(Na2CO3)样品经焙烧后形成CuO-ZnO固溶体, 呈现出更高的分散度, 而CZ(NaOH)和CZ(NaHCO3)催化剂中CuO与ZnO结晶度较好的结论一致.

|
图 3 CuO-ZnO催化剂的TEM图 Fig.3 TEM images of CuO-ZnO catalyst. CZ(NaOH) (a), CZ(Na2CO3) (b), CZ(NaHCO3) (c) |
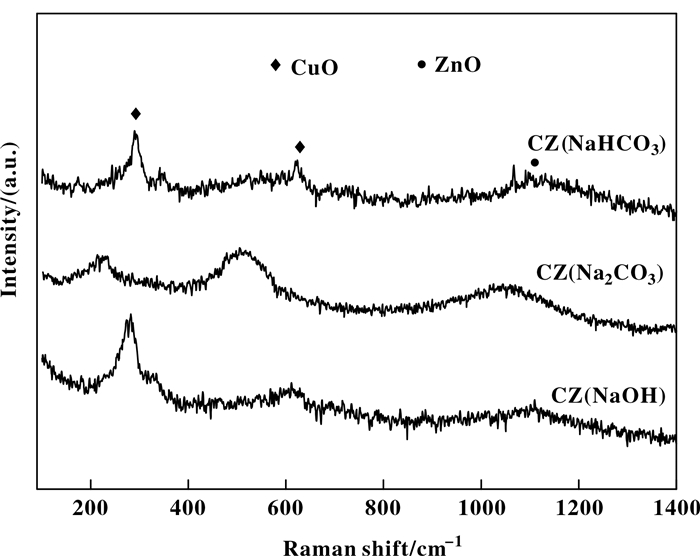
图 4为CuO-ZnO催化剂在100~1400 cm-1范围内的Raman谱图.由图可以看到, CZ(NaHCO3)及CZ(NaOH)均在280、620以及1090 cm-1出现拉曼位移.其中280以及620 cm-1的拉曼位移归属于CuO的特征峰[30-31], 而1090 cm-1左右的拉曼位移归属于ZnO的特征峰[32].对比CZ(NaOH)和CZ(NaHCO3)两样品可以发现, CZ(NaHCO3)中CuO特征峰更尖锐, 表明表层CuO的结晶度更完整, 晶粒尺寸更大.结合XRD结果, 两样品的晶体结构并不均匀, CZ(NaOH)呈现表层CuO结晶完整, 而体相结晶稍差的结构特征, CZ(NaHCO3)为表层CuO结晶差而体相结构结晶完整的状态.与CZ(NaOH)和CZ(NaHCO3)催化剂相比, CZ(Na2CO3)催化剂的拉曼峰更宽泛并向低频方向移动, 表明ZnO的掺入导致CuO结构产生空位, CuO与ZnO之间存在强相互作用[33].这进一步验证了XRD表征中所得出的沉淀剂为Na2CO3的催化剂在焙烧后形成了CuO-ZnO固溶体的结论.
|
图 4 CuO-ZnO催化剂的Raman图 Fig.4 Raman spectra of CuO-ZnO catalysts |
图 5为CuO-ZnO催化剂的H2-TPR图.通常情况下, TPR还原峰的峰位置与Cu物种的晶粒尺寸直接相关[34-35], 具有小晶粒尺寸的Cu物种分散性好, 表面具有易于吸附活化H2的氧缺陷位点, 可以在低的温度下使CuO还原[36].而大晶粒CuO物种由于表面缺陷位较少, 起始还原温度升高, 同时, 完整CuO晶粒抑制了H2向体相内的扩散, 进一步增加了还原的难度. 图 5中CZ(Na2CO3)还原峰起止温度分别为250与380 ℃, 在295 ℃表现为宽化的主耗氢峰, 与其他两样品相比, 呈现最低的还原温度, 归因于CuO物种高的分散度, 同时ZnO强的吸附活化H2能力也促进了CuO物种的还原. CZ(NaHCO3)还原峰表现为起止温度分别为275与380 ℃, 峰顶温度为325 ℃左右的单一耗氢峰, 与CZ(Na2CO3)相比, 还原温度明显向高温区迁移, 归因于CZ(NaHCO3)大的CuO晶粒及弱的CuO-ZnO间相互作用.对于CZ(NaOH), 还原峰进一步向高温区迁移, 表现为320~400 ℃之间, 峰顶温度为350 ℃左右的耗氢峰.结合XRD及Raman表征, 这归因于其晶型更为完整的表面结构, 抑制了CuO物种的初始还原及H向体相的扩散.

|
图 5 CuO-ZnO催化剂的H2-TPR图 Fig.5 H2-TPR profiles of CuO-ZnO catalysts |
表 1是3种不同沉淀剂制备的CuO-ZnO催化剂的评价结果, 在该反应中, 甲醛乙炔化的主产物为BYD.由表可知, CZ(NaOH)催化剂的甲醛转化率、1, 4-丁炔二醇选择性与产率分别为89.9%、89.7%与80.7%; CZ(NaHCO3)催化剂的甲醛转化率、1, 4-丁炔二醇选择性与产率分别为82.8%、87.0%与72.1%; CZ(Na2CO3)催化剂的甲醛转化率、1, 4-丁炔二醇选择性和产率分别为97.6%、93.5%和91.3%, 表现出最佳的催化性能.
| 表 1 CuO-ZnO催化剂的评价结果 Table 1 Evaluation results of CuO-ZnO catalysts |
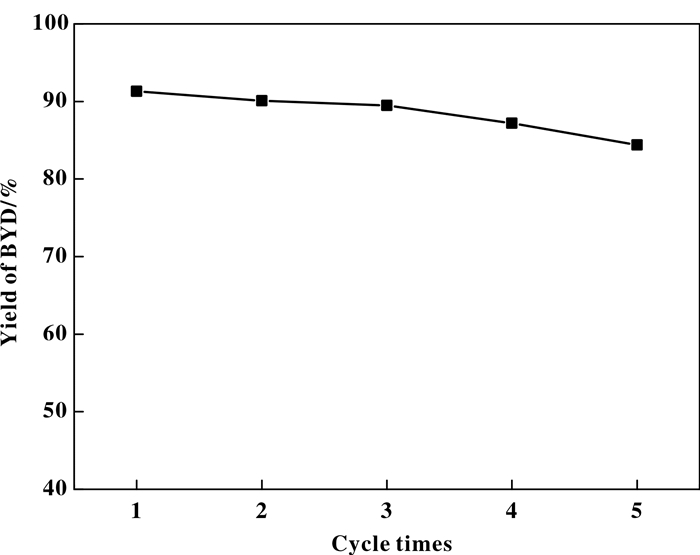
选用反应活性最佳的CZ(Na2CO3)催化剂做稳定实验, 每次反应结束后, 用离心机对反应后催化剂进行离心分离, 取分离后的物料进行分析, 催化剂重新置于烧瓶中, 补加0.2 g新鲜催化剂(补充分离过程引起的催化剂损失)并加入新的甲醛原料进行下一次实验, 重复反应5次实验, 得到实验结果如图 6所示.从图中可以看出, CZ(Na2CO3)催化剂经过3次循环套用实验, 催化剂活性基本保持不变, 但在第4、5次循环套用实验时, 催化活性有所下降, 归因于反应过程中少量活性铜物种的流失.
|
图 6 CZ(Na2CO3)催化剂的循环套用实验 Fig.6 CZ(Na2CO3) cyclic test of catalyst Reaction condition: The amount of catalyst was 2.5 g, the concentration of formaldehyde solution was 35%, the consumption was 50 mL, the reaction temperature was 90 ℃ and the reaction time was 15 h. |
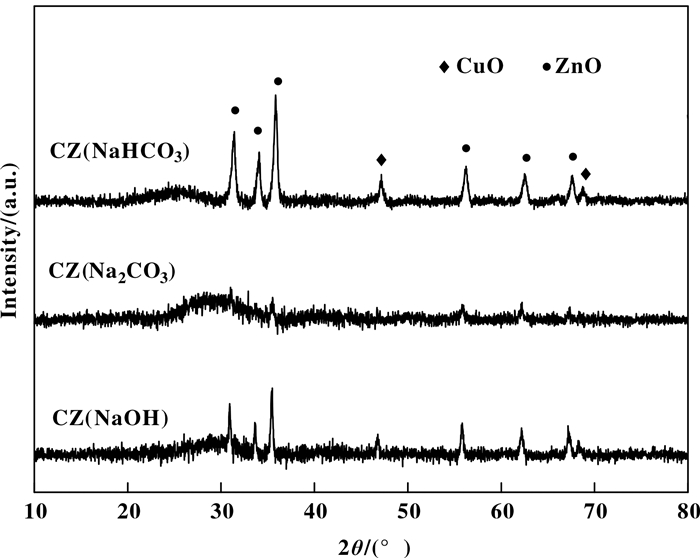
前期研究结果表明, 在甲醛乙炔化反应中, 氧化态铜物种需经过复杂的化学过程转化为活性物种炔化亚铜才能表现出反应活性, 在甲醛乙炔化反应条件下Cu+的数量与分散是影响催化活性的主要因素[8-9, 37].综合表征结果推测, CZ(Na2CO3)催化剂具有最优催化反应性能的主要原因在于, 形成了CuO-ZnO固溶体具有强的相互作用, 一方面降低了Cu2+的还原温度, 使Cu2+物种在甲醛乙炔化的反应中原位转化为Cu+活性物种, 同时有效抑制转化过程中活性组分的迁移聚集.大量炔化亚铜物种高度分散, 表现为最优的催化性能.与CZ(Na2CO3)相比, CZ(NaOH)和CZ(NaHCO3)催化剂中CuO晶粒尺寸大, 不利于活性组分Cu+的充分暴露, 所以表现出催化性能偏低.对应反应后催化剂的XRD表征进一步证实了这一点, 如图 7所示, CZ(NaOH)与CZ(NaHCO3)中出现了尖锐的ZnO衍射峰以及微弱的CuO衍射峰, 表明CuO大部分有效转化为炔化亚铜活性物种. CZ(Na2CO3)催化剂中CuO和ZnO的衍射峰几乎全部消失, 转化为无定形的炔化亚铜活性物种.因此, CZ(Na2CO3)催化剂表现出最佳的催化活性.
|
图 7 反应后CuO-ZnO催化剂的XRD图 Fig.7 XRD patterns of CuO-ZnO catalysts after reaction |
研究了以NaOH、Na2CO3和NaHCO3为沉淀剂制备的催化剂对甲醛乙炔化性能的影响.以NaOH与NaHCO3为沉淀剂制备的催化剂, 表现为大晶粒的CuO与ZnO, 且两者间相互作用弱, 不利于甲醛乙炔化反应中CuO物种的还原, 生成的炔化亚铜活性物种较少, 催化活性差.而CZ(Na2CO3)催化剂中形成了CuO-ZnO固溶体, CuO与ZnO之间产生强相互作用, 同时有效抑制了CuO颗粒的长大, 使甲醛乙炔化反应中Cu2+高效转变为炔化亚铜活性物种, 催化活性最高.
| [1] | Li H T, Zhao Y X, Gao C G, et al. Study on deactivation of Ni/Al2O3 catalyst for liquid phase hydrogenation of crude 1, 4-butanediol aqueous solution[J]. Chem Eng J, 2012, 181/182: 501–507. DOI:10.1016/j.cej.2011.06.029 |
| [2] | Wang Z P, Niu Z Z, Hao Q A, et al. Enhancing the ethynylation performance of CuO-Bi2O3 nanocatalysts by tuning Cu-Bi interactions and phase structures[J]. Catal, 2019, 9(35): 1–18. |
| [3] | Guo Jiang-yuan(郭江渊), Li Hai-tao(李海涛), Zhang Zhi-long(张智隆), et al. Effect of surface acidity on Ni/SiO2-Al2O3 catalyst performance for 1, 4-butynediol hydrogenation(表面酸性对Ni/SiO2-Al2O3催化剂催化1, 4-丁炔二醇高压加氢性能的影响)[J]. J Mol Catal (China)(分子催化), 2016, 30(1): 37–45. |
| [4] |
a. Liu Lin-li (刘琳丽), Li Hai-tao (李海涛), Wang Chang-zhen (王长真), et al. Effect of supports on the hydrogenation of 1, 4-butynediol over supported Ni catalyst (负载Ni催化剂上1, 4-丁炔二醇加氢反应的载体效应研究) [J]. J Mol Catal (China) (分子催化), 2018, 32(2): 99-106. b. Zhao Fang(赵芳), Wang Chang-zhen(王长真), Tian Ya-ni(田亚妮), et al. Metal promoter effect of Ni-M/SiO2 in hydrogenation of 1, 4-butynediol(Ni-M/SiO2催化1, 4-丁炔二醇加氢的金属助剂效应) [J]. J Mol Catal(China)(分子催化), 2019, 33(1): 83-89. |
| [5] | Wang Zhi-peng(王志鹏), Niu Zhu-zhu(牛珠珠), Ban Li-jun(班丽君), et al. Formaldehyde ethynylation reaction over Cu2O supported on TiO2 with different phases(不同晶相TiO2负载Cu2O催化甲醛乙炔化反应)[J]. Chem J Chin Univer(高等学校化学学报), 2019, 40(2): 334–341. |
| [6] | Haas T, Jaeger B, Weber R. New diol processes:1, 3-propanediol and 1, 4-butanediol[J]. Appl Catal A, 2005, 280(1): 83–88. |
| [7] | Duncanson I T, Sutherland I W, Cullen B. The hydroge-nation of 2-butyne-1, 4-diol over a carbon-supported palladium catalyst[J]. Catal Lett, 2005, 103(3/4): 195–199. |
| [8] | Ma Zhi-qiang(马志强), Zhang Hong-xi(张鸿喜), Li Hai-tao(李海涛), et al. Preparation of core-shell CuO-Bi2O3@meso-SiO2 catalyst and its catalytic performance for formaldehyde ethynylation(核壳结构CuO-Bi2O3@meso-SiO2催化剂的制备及甲醛乙炔化性能)[J]. Indus Catal (China)(工业催化), 2015, 23(5): 344–348. DOI:10.3969/j.issn.1008-1143.2015.05.003 |
| [9] | Li Hai-tao(李海涛), Niu Zhu-zhu(牛珠珠), Yang Guo-feng(杨国峰), et al. Support effect of Cu2O/TiO2 employed in Formaldehyde Ethynylation(Cu2O/TiO2催化甲醛乙炔化反应的载体效应)[J]. J Chem Indus Engineer (China)(化工学报), 2018, 69(6): 2512–2518. |
| [10] | Wang Zhi-peng(王志鹏), Niu Zhu-zhu(牛珠珠), Ban Li-jun(班丽君), et al. The influence of N doping on TiO2 supported Cu based catalyst for formaldehyde ethynylation(N掺杂对TiO2负Cu基催化剂甲醛乙炔化性能的影响)[J]. J Shanxi Norm Univer (Nat Sci Edit)(陕西师范大学学报), 2019, 47(1): 99–106. |
| [11] | Wang Jun-jun(王俊俊), Li Hai-tao(李海涛), Ma Zhi-qiang(马志强), et al. Preparation of magnetic CuO-Bi2O3/Fe3O4-SiO2-MgO catalyst and its catalytic performance for formaldehyde ethynylation(磁性CuO-Bi2O3/Fe3O4-SiO2-MgO催化剂的制备及甲醛乙炔化性能)[J]. J Chem Indus Engineer (China)(化工学报), 2015, 66(6): 2098–2104. |
| [12] | Zheng Yan(郑艳), Sun Zi-zhen(孙自瑾), Wang Yong-zhao(王永钊), et al. Preparation and acetylation performance of CuO-Bi2O3/SiO2-MgO catalysts(CuO-Bi2O3/SiO2-MgO催化剂的制备及炔化性能)[J]. J Mol Catal (China)(分子催化), 2012, 26(3): 233–238. |
| [13] | Vasiliadou E S, Fanti V L Y, Lemonidou A A. One-pot tandem processing of glycerol tream to 1, 2-propanediol with methanol refbaming as hydrogen donor reaction[J]. Appl Catal B, 2015, 163: 258–266. DOI:10.1016/j.apcatb.2014.08.004 |
| [14] | Feng Y H, Yin H B, Wang A L, et al. Gas phase hydrogenolysis of glycerol catalyzed by Cu/ZnO/MOx (MOx=TiO2 and ZrO2) catalysts[J]. Chem Engineer J, 2011, 168(1): 403–412. |
| [15] | Choi Y, Futagami K, Fujitani T, et al. The role of ZnO in Cu/ZnO methanol synthesis catalysts-moiphology effect or active site model[J]. Appl Catal A, 2001, 208(1/2): 163–167. |
| [16] | Kidd S, Thorhauge M, Falsig H, et al. Quantifying the promotion of Cu catalysts by ZnO for methanol synthesis[J]. Sci, 2016, 352(6288): 969–974. DOI:10.1126/science.aaf0718 |
| [17] | Behrens M, Studt F, Kasatkin , et al. The active site of merhanol synthsis over Cu/ZnO/Al2O3 industrial catalysts[J]. Sci, 2012, 336(6083): 893–897. DOI:10.1126/science.1219831 |
| [18] | Kuld S, Conradsen C, Moses P G, et al. Quantification of zinc atoms in a surface alloy on copper in an industial-type methanol synthesis catalyst[J]. Angew Chem Int Ed, 2014, 53(23): 5941–5945. DOI:10.1002/anie.201311073 |
| [19] | Senanayake S D, Ramirez P J, Waluyo I, et al. Hydrogenation of CO2 to methanol on CeOx/Cu(111) and ZnO/Cu(111) catalysts:Role of the metal-oxide interface and importance of Ce3+ Sites[J]. J Phys Chem C, 2016, 120(3): 1778–1784. DOI:10.1021/acs.jpcc.5b12012 |
| [20] | Bae J W, Kang S H, Lee W, et al. Effect of precipitants during the preparation of Cu-ZnO-Al2O3/Zr-ferrierite catalyst on the DME synthesis from syngas[J]. J Chem Indus Engineer, 2009, 15(4): 566–572. DOI:10.1016/j.jiec.2009.01.014 |
| [21] | Li Yuan(李源), Zhang Xiang-ping(张香平), Wang Lei(王蕾), et al. Cu/MgO/ZnO catalyst for low temperature liquid phase methanol synthesis(用于低温液相甲醇合成的Cu/MgO/ZnO催化剂)[J]. Chin J Proce Engineer(过程工程学报), 2010, 10(4): 781–787. |
| [22] | Chen Peng-ze(陈鹏泽), Gao Wen-gui(高文贵), Na Wei(纳薇), et al. Effect of different precipitants on the performance of Cu-ZnO-ZrO2 catalyst for hydrogenation of CO2 to methanol(不同沉淀剂对CO2加氢合成甲醇Cu-ZnO-ZrO2催化剂性能的影响)[J]. Chem Indus Engineer Pro(化工进展), 2017, 36(8): 2955–2961. |
| [23] | Chen Xiong(陈雄), Zheng Hua-yan(郑华艳), Yang Hao(杨浩), et al. Effect of CO2 on aging and catalytic performance of CuO/ZnO/A12O3 catalyst precursors(CO2对CuO/ZnO/A12O3催化剂前体老化及催化性能的影响)[J]. Chem Indus Engineer Pro(化工进展), 2013, 32(11): 2644–2649. |
| [24] | Fang De-ren(房德仁), Liu Zhong-min(刘中民), Xu Xiu-feng(徐秀峰), et al. Effect of aging time on the performance of Cu/ZnO/A12O3 methanol synthesis catalyst(老化时间对Cu/ZnO/A12O3合成甲醇催化剂性能的影响)[J]. J Fuel Chem Technol(燃料化学学报), 2006, 34(1): 96–99. DOI:10.3969/j.issn.0253-2409.2006.01.020 |
| [25] | Ryu S K, Lee W K, Park S J. Thermal decomposition of hydrated copper nitrate[Cu(NO3)2·3H2O] on activated carbon fibers[J]. Carbon SCi, 2004, 5(4): l80–l85. |
| [26] | MaIecka B, Gajerski R, Malecki A, et al. Mass spectral studies on the mechanism of thermal decomposition of Zn(NO3)2·nH2O[J]. Thermochim Acta, 2003, 404(1): l25–132. |
| [27] | Li J, Inui T. Characterization of precursors of methanol synthesis catalysts, copper/zinc/aluminum oxides, precipitated at different pHs and temperatures[J]. Appl Catal A, 1996, 137(1): 105–117. |
| [28] | Graeme J M, Ivan H H, Philippa J R U, et al. Characterization of precursors to methanol synthesis catalysts Cu/ZnO system[J]. J Chem Soc, Faraday Trans, 1998, 94(4): 593–600. DOI:10.1039/a703954i |
| [29] | Aguila G, Gracia F, Araya P. CuO and CeO2 catalysts supported on Al2O3, ZrO2 and SiO2 in the oxidation of CO at low temperature[J]. Appl Catal A, 2008, 343(1/2): 16–24. |
| [30] | Lin Y G, Hsu Y K, Chen S Y, et al. Microwave-activated CuO nanotip/ZnO nanorod nanoarchitectures for efficient hydrogen production[J]. J Mater Chem, 2011, 21(2): 324–326. DOI:10.1039/C0JM03022H |
| [31] | Yu T, Zhao X, Shen Z X, et al. Investigation of individual CuO nanorods by polarized micro-Raman scattering[J]. J Cryst Growth, 2004, 268(3/4): 590–595. |
| [32] | Iqbal J, Safdar N, Jan T, et al. Facile synthesis as well as structural, raman, dielectric and antibacterial characteristics of Cu doped ZnO nanoparticles[J]. J Mater Sci Technol, 2015, 31(3): 300–304. DOI:10.1016/j.jmst.2014.06.013 |
| [33] | Li Zhong(李忠), Zheng Hua-yan(郑华艳), Xie Ke-chang(谢克昌). Surface properties of methanol CuO/ZnO/Al2O3 catalysts synthesized by slurry bed(浆态床合成甲醇CuO/ZnO/Al2O3催化剂的表面性质)[J]. Chin J Catal(催化学报), 2008, 29(5): 431–435. DOI:10.3321/j.issn:0253-9837.2008.05.005 |
| [34] | He Z, Lin H, He P, et al. Effect of boric oxide doping on the stability and activity of a Cu-SiO2 catalyst for vapor-phase hydrogenation of dimethyl oxalate to ethylene glycol[J]. J Catal, 2011, 277(1): 54–63. |
| [35] | Agrell J, Birgersson H, Boutonnet M, et al. Production of hydrogen from methanol over Cu/ZnO catalysts promoted by ZrO2 and Al2O3[J]. J Catal, 2003, 219(2): 389–403. |
| [36] | Zhong Lu-xiang, Zhang Chong-chun, Chen Xiao-yun. Effect of promoter SiO2, TiO2 or SiO2-TiO2 on the performance of CuO-ZnO-Al2O3 catalyst for methanol synthesis from CO2 hydrogenation[J]. Appl Catal A, 2012, 415/416: 118–123. DOI:10.1016/j.apcata.2011.12.013 |
| [37] | Yang Guo-feng(杨国峰), Li Hai-tao(李海涛), Zhang Hong-xi(张鸿喜), et al. Effect of NaOH concentration on Cu2O structure and formaldehyde acetylation perfor-mance(NaOH浓度对Cu2O结构及甲醛乙炔化性能的影响)[J]. J Mol Catal(China)(分子催化), 2016, 30(6): 540–546. |
 2019, Vol. 33
2019, Vol. 33


