2. 昆明理工大学 环境科学与工程学院, 云南 昆明 650093;
3. 昆明理工大学 省部共建复杂有色金属资源清洁利用国家重点实验室, 云南 昆明 650093
2. Faculty of Environmental Science and Engineering, Kunming University of Science and Technology, Kunming 650093, China;
3. State Key Laboratory of Complex Nonferrous Metal Resources Clean Utilization, Kunming University of Science and Technology, Kunming 650093, China
甲醛是室内空气主要污染物之一, 对人体健康危害巨大[1-4].甲醛作为室内最典型的VOCs(挥发性有机物)[5-6], 因其强刺激性、毒性和致癌作用引起广泛关注.而在众多去除甲醛的方法中, 催化氧化是最有效的去除方法.催化氧化甲醛的催化剂分为贵金属和非贵金属催化剂, 而贵金属催化剂具有良好的低温活性[7-8].但是, 贵金属因资源匮乏、价格昂贵的缺陷, 难以广泛商用.
与Pt、Pd和Rh基催化剂相比, Ag基催化剂由于兼具贵金属低温高活性和价格成本低的优点而备受关注[9-13], 且在VOCs催化氧化中显示出优异的活性. Qu等[14]研究了不同Ag物种的形成及其对NH3-SCO性能的影响, 并提出了Ag物种和NH3-SCO性能的关系模型.储伟等[15]探究了4种载体、银含量及焙烧温度对银基催化剂催化丙烯选择还原NO的反应性能的影响, 结果表明Ag/Al2O3催化剂具有较好的催化性能.通常情况, 沉淀过程中沉淀剂的选取对催化剂最终的电子价态和表面氧含量存在影响[16]. Chen等[17]通过沉淀法制备两种Au/CeO2催化剂, 分别采用尿素和氢氧化钠作为沉淀剂得到Au/CeO2(DPU)和Au/CeO2(DPN).由于Au-CeO2强相互作用产生的活性表面氧物质含量增加, Au/CeO2(DPU)催化剂的活性高于DPN催化剂, 室温下甲醛转化为CO2和H2O的转化率为100%.另外, Peng等[18]研究表明, 活性组分的负载含量也对催化剂整体活性具有显著影响, Pt/TiO2表面适量的Pt物种能够更好的分散暴露更多的活性位点.
综上所述, 为进一步探究甲醛低温催化氧化方面的应用, 考察了不同沉淀剂和Ag含量变化对甲醛降解性能的影响, 通过不同的表征手段以及活性测试评价来研究催化剂的结构和理化性质.
1 实验部分 1.1 催化剂的制备不同沉淀剂制备CeO2-Co3O4载体:采用共沉淀法制备CeO2-Co3O4载体.以六水硝酸铈(Ce(NO3)2·6H2O)和六水硝酸钴(Co(NO3)2·6H2O)为前驱体源, 共称取5份20 mmol Ce(NO3)2·6H2O和Co(NO3)2·6H2O, 将其按物质的量比Ce:Co为1:19分别溶解于去离子水中.选用不同沉淀剂, 包括KHCO3、NaHCO3、NH4HCO3、NH3·6H2O和草酸, 将适量1 mol/L不同沉淀剂分别缓慢滴加至上述溶液中, (Ce+Co)/沉淀剂物质的量比为1:3.于室温剧烈搅拌1 h, 静置2 h, 过滤、水洗数次, 80 ℃干燥过夜, 并在450 ℃焙烧4 h.分别标记为CeCo-K、CeCo-Na、CeCo-NH4、CeCo-NH3、CeCo-OA.
采用过量浸渍法制备不同Ag负载含量的Ag/CeO2-Co3O4催化剂, 分别称取1 g制得的CeCo-OA于化学计量的AgNO3溶液中于60 ℃搅拌蒸干.所得固体80 ℃过夜干燥后放入马弗炉内, 350 ℃焙烧3 h. Ag的理论负载量分别为: 0.1%、0.25%、0.5%、1%、2%、4% (重量百分比).所得样品粉末分别标记为0.1Ag/CeCo、0.25Ag/CeCo、0.5Ag/CeCo、1Ag/CeCo、2Ag/CeCo、4Ag/CeCo.
1.2 催化剂的表征XRD可用于分析样品中的物种和存在形式, 仪器为德国布鲁克的Bruker D8 Advance, 以6°/min, 在10°~80°进行扫描.其入射光源为Cu靶, 步长0.02°, 工作电压40 kV, 工作电流40 mA.
氮气吸-脱附可测定样品的织构性质, 仪器为美国Micromeritics公司的TriStarⅡ3020型物理吸附仪.样品在200 ℃和真空的条件下进行3 h的预处理, 以N2为吸附质在-196 ℃下进行测量.然后计算比表面积、孔容和平均孔径.
拉曼光谱测试用Renishaw inVia Reflex 2000型激光显微拉曼光谱仪进行测试.在测试前, 使用硅晶片对拉曼光谱在520.5 cm-1处进行校准.以Ar为激发光源, 其波长为532 nm.在室温下, 2100~800 cm-1区间测试.
氢气程序升温还原(H2-TPR)是在内径为4 mm固定床微型石英管反应器内进行的, 其检测器为TCD.首先称取30 mg的样品, 在N2的气体流量为30 mL/min条件下升温至300 ℃并保持40 min, 然后降至室温, 在30 mL/min H2/Ar (H2=5%)的气流下升温至850 ℃.
原位漫反射傅立叶变换红外(In-situ DRIFTS)的测试仪器是Harrick Scientific漫反射附件的Nicolet iS 50红外光谱仪.在进行实验前, 将样品放到反应池中(含有ZnSe窗片), 且在N2气流为100 mL/min和温度为200 ℃的条件下吹扫60 min, 待其降至室温.升温至70 ℃时, 首先通入HCHO和N2吸附30 min, 然后N2吹扫15 min, 最后通入O2和N2来进行反应并采集谱图.
1.3 活性测试评价催化剂活性测试装置为固定床石英管(i.d.=6 mm).使用氮气鼓泡37%甲醛溶液产生HCHO和N2的混合气体, 混合气总流量为100 mL/min, 催化剂用量则为200 mg.在测试前, 将催化剂于10%H2/N2氛围下以及温度为150 ℃时还原1 h, 稳定性测试的气体组分为: 0.2%HCHO+20%O2+N2, 混合气总流量为100 mL/min, 在80 ℃下进行连续反应, 时长为30 h.最后, 将反应后的气体通到9780型气相色谱(含有TCD和FID检测器且安装甲烷化炉, 色谱柱采用填充柱)中分析, 其进样方式通过六通阀进样. HCHO的转化率用CO2的产率评估.
| $ {{\rm{X}}_{{\rm{HCHO}}}}\left( \% \right) = \frac{{{{\left[ {{\rm{C}}{{\rm{O}}_2}} \right]}_{{\rm{out}}}}}}{{{{[{\rm{HCHO}}]}_{{\rm{in}}}}}} \times 100\% $ | (1) |
式中, [CO2]out为产物中CO2的体积分数, [HCHO]in为进气中HCHO的体积分数.
2 结果与讨论 2.1 活性测试如图 1所示, 对于不同沉淀剂制备的催化剂, 其甲醛催化氧化性能存在明显差异.各催化剂在WHSV = 30 000 mL·g-1·h-1时的T90高低依次为: Ag/CeCo-NH4> Ag/CeCo-K > Ag/CeCo-NH3> Ag/CeCo-Na > Ag/CeCo-OA.总体而言, 所有催化剂均能在≤ 90 ℃时达到100%甲醛去除率.此外, 所有催化剂在甲醛催化转化温度下反应产物中未检测到CO, 表明所有催化剂表面无CO生成.显然, 在80 ℃时Ag/CeCo-OA和Ag/CeCo-Na催化剂上甲醛100%氧化成CO2, 因此这两种催化剂具有在这项研究中的优异的催化性能.相对而言, Ag/CeCo-OA在低温段各温度点的活性都略优于Ag/CeCo-Na.总体来讲, 在甲醛催化氧化反应中Ag/CeCo-OA显示出最优的低温活性, 说明草酸沉淀剂对催化剂活性影响明显.

|
图 1 不同沉淀剂制备的各催化剂上甲醛催化氧化性能 Fig.1 The HCHO catalytic performance on the various catalysts prepared with different precipitants |
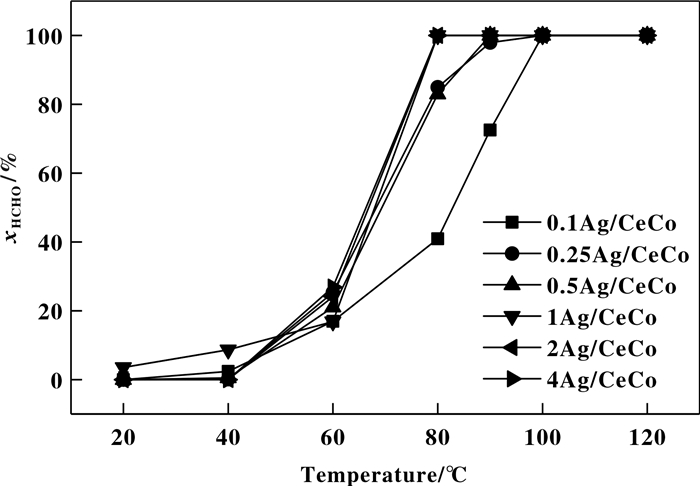
为进一步明确CeO2-Co3O4复合氧化物载体表面浸渍Ag的最优负载量, 图 2列举了一系列不同Ag含量的Ag/CeO2-Co3O4催化剂用于甲醛催化氧化的低温活性结果.由图 2可知, 系列催化剂均显示出较好的低温催化性能, 其中, 0.1Ag/CeCo在100 ℃便实现甲醛的完全转化, CeO2-Co3O4复合金属氧化物能够在120 ℃达到100%甲醛转化, 痕量的Ag物种加入能明显提高其催化性能, 并直接作为活性位点参与到甲醛催化氧化反应过程中.当Ag负载量 < 1%(重量百分比)时, 甲醛的催化氧化性能随Ag含量的增加而提高. 1Ag/CeCo, 2Ag/CeCo和4Ag/CeCo都能够在80 ℃达到甲醛的完全降解, 但是, 3种催化剂在低温段的催化活性增长趋势一致, 差异甚小.因此, 选取1Ag/CeCo催化剂作为催化氧化甲醛的最佳催化剂.
|
图 2 不同Ag负载量催化剂上甲醛催化氧化性能 Fig.2 HCHO catalytic performance on various catalysts prepared with different Ag contents |
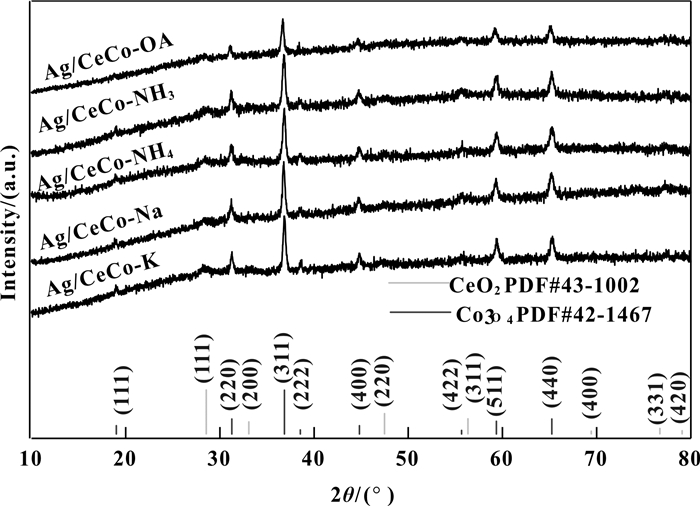
经不同沉淀剂制备的各催化剂XRD图谱见图 3.所有样品中位于28.5°、33.0°、47.6°、56.2°、69.5°、76.9°和79.0°处较弱的衍射峰分别归属于具有立方萤石结构的CeO2(PDF#43-1002)的(111)、(200)、(220)、(311)(400)、(331)和(420)晶面.而在19.0°、31.2°、36.8°、38.7°、44.9°、55.5°、59.3°和65.2°处的特征衍射峰分别对应具有尖晶石结构的Co3O4(PDF#42-1467)的(111)、(220)、(311)、(222)、(400)、(422)、(511)、(440)晶面.随着沉淀剂的变化, 所对应的CeO2和Co3O4衍射峰强度逐渐变弱, 表明其结晶度逐渐降低, 对应缺陷相继增多, 有利于催化活性增强.其中, Ag/CeCo-OA催化剂中CeO2和Co3O4的衍射峰强度最弱, 说明其对应的缺陷最多, 有利于催化氧化甲醛, 这与活性测试结果一致.相比之下, Ag/CeCo-K和Ag/CeCo-NH4催化剂对应的衍射峰强度略微增强, 表明其对应的结晶度较高, 对应的结构缺陷少, 不利于甲醛的催化降解.另外, 所有样品中均未发现明显关于Ag物种的相关衍射峰, 说明通过过量浸渍法负载的活性组分Ag均匀分散于CeO2-Co3O4载体上.
|
图 3 不同沉淀剂制备的各催化剂XRD图谱 Fig.3 The XRD patterns of the various catalysts prepared with different precipitants |
不同Ag负载含量催化剂的XRD图谱如图 4所示, 所有样品在图例衍射角度范围内存在相同衍射峰, 分别属于CeO2立方萤石结构和Co3O4尖晶石结构.其中, 分属于CeO2立方萤石结构对应衍射峰强度相对较弱, 这归因于其在整体占比中含量较小(Co/Ce=19).相比之下, Co3O4对应的衍射峰更明显, 说明其相应的结晶度较高.然而, 不同Ag含量的Ag/CeO2-Co3O4催化剂其组分结晶度有所不同.随着Ag含量的增加对应的CeO2和Co3O4衍射峰强度逐渐变弱, 表明其结晶度逐渐降低, 对应缺陷增多.说明Ag物种与CeO2-Co3O4复合氧化物载体存在强烈的相互作用.其中, 1Ag/CeCo催化剂中CeO2和Co3O4的衍射峰强度最弱, 说明其对应的缺陷最多, 有利于催化活性增强.随着Ag含量进一步增多, 催化剂的结晶度再次增强, 活性也未出现明显提高, 说明结构缺陷对催化活性有积极的影响.但是, 2Ag/CeCo和4Ag/CeCo催化剂也显示出与1Ag/CeCo催化剂相当的催化性能, 可能是因为Ag含量的增加促使对应活性位点的增多.除此之外, 所有样品中也未发现关于Ag物种的衍射峰, 说明Ag物种能够高度分散于CeO2-Co3O4复合氧化物载体表面.

|
图 4 不同Ag负载量催化剂的XRD图谱 Fig.4 The XRD patterns of various catalysts prepared with different Ag contents |
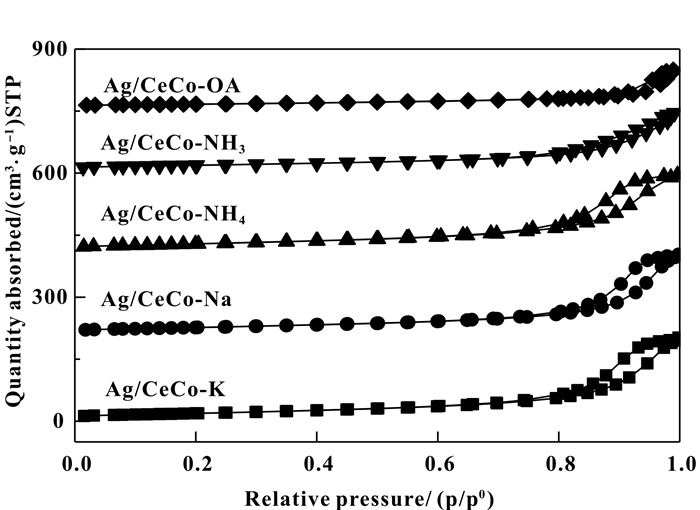
由图 5可知, 所有样品显示出典型的Ⅳ类等温线、H4型滞回环, 表明所有材料均是介孔结构, 且不同沉淀剂制备的Ag/CeO2-Co3O4催化剂对应的氮气吸附量不同, 说明制备过程中沉淀剂的选择对其织构性质影响显著.根据表 1数据结果显示, 不同沉淀剂制备的催化剂其织构性质差异明显, 然而比表面积和孔容、孔径之间没有明显关联.总体来说, HCO3-类沉淀剂制得的催化剂比表面积更大, OH-次之, C2O42-最小.其中, 由HCO3-沉淀得到的催化剂中Ag/CeCo-K和Ag/CeCo-Na对应的比表面积相比Ag/CeCo-NH4更小, 可能是由残留的K、Na物质填充了微孔, 导致比表面积下降, 孔体积变大[19].结合活性测试结果, 平均孔径大小与其活性测试结果一致: Ag/CeCo-OA ≥ Ag/CeCo-Na > Ag/CeCo-NH3> Ag/CeCo-K > Ag/CeCo-NH4.
|
图 5 不同沉淀剂制备的各催化剂N2吸脱附曲线 Fig.5 N2 adsorption-desorption isotherms of the various catalysts prepared with different precipitants |
| 表 1 不同沉淀剂制备的各催化剂的孔结构参数 Table 1 Pore structural parameters of various catalysts prepared with different precipitants |
不同Ag负载含量的催化剂织构性质差异通过氮气吸脱附实验测试, 实验结果如图 6所示, 所有样品的氮气吸脱附曲线显示出Ⅳ类等温线和H4型滞回环, 典型的介孔结构.由图 6可知, 各样品的氮气吸脱附曲线趋势一致, 且未观测出明显差异, 表明Ag负载含量对其织构性质影响较小, 且Ag的加入对CeO2-Co3O4复合氧化物载体的影响也较小.根据表 2中各催化剂的孔结构参数不难发现, 不同Ag含量对催化剂的表面积、孔体积及平均孔径有一定的影响, 使其在最终测试结果中显示出细微的差别.其中, 比表面积随着Ag负载含量的增加而增加, 1%(重量百分比) Ag/CeO2-Co3O4比表面积最大, Ag含量进一步增加后比表面积下降, 说明不同金属负载量的分散呈火山型, 1%(重量百分比) Ag/CeO2-Co3O4显示出最高的分散度, 其对应的金属颗粒应该是最小的.相比之下, 孔体积和孔径随Ag含量变化无明显规律可循.根据活性测试结果可以推测催化性能与Ag颗粒的分散度有关.

|
图 6 不同Ag负载含量催化剂N2吸脱附曲线 Fig.6 N2 adsorption-desorption isotherms of various catalysts with different Ag contents |
| 表 2 不同Ag含量的各催化剂的孔结构参数 Table 2 Pore structural parameters of various catalysts prepared with different Ag contents |
不同沉淀剂制备的各催化剂拉曼光谱如图 7所示, Ag物种的衍射峰均未从催化剂中观测到, 说明经不同沉淀剂制备的催化剂中Ag物种无明显的拉曼散射信号.所有催化剂均显示出对应Co3O4尖晶石结构的伸缩振动峰.其中, 186和669 cm-1波数附近的散射峰分别对应于Co2+-O2-和Co3+-O2-[20].通常, Co2+填充Co3O4的四面体位置, 而Co3+则填充八面体位置.根据图 7可知, 经不同沉淀剂制备的样品其Raman峰位置, 尤其是八面体位置(CoO6), 存在不同程度的偏移.其中, 经HCO3-沉淀制备的3种催化剂, Ag/CeCo-Na对应的拉曼光谱向高波数偏移.由于其光子限制效应, 拉曼带的蓝移可归因于表面氧空位[21], 氧空位的存在可以有效改善氧分子的流动性且更容易形成活性氧物种, 从而进一步提高催化性能.相比之下, Ag/CeCo-OA和Ag/CeCo-NH3的拉曼光谱也存在类似的蓝移, Ag/CeCo-OA蓝移程度较明显, 表面氧空位最多.催化剂对应的偏移程度与活性测试结果一致, 表明不同沉淀剂在制备过程中对Ce、Co前驱体作用机制有所区别, 导致相应的结构无序度和残留应力的差异, 进而导致相应的活性差异.

|
图 7 不同沉淀剂制备的各催化剂拉曼光谱 Fig.7 The Raman spectra of the various catalysts prepared with different precipitants |
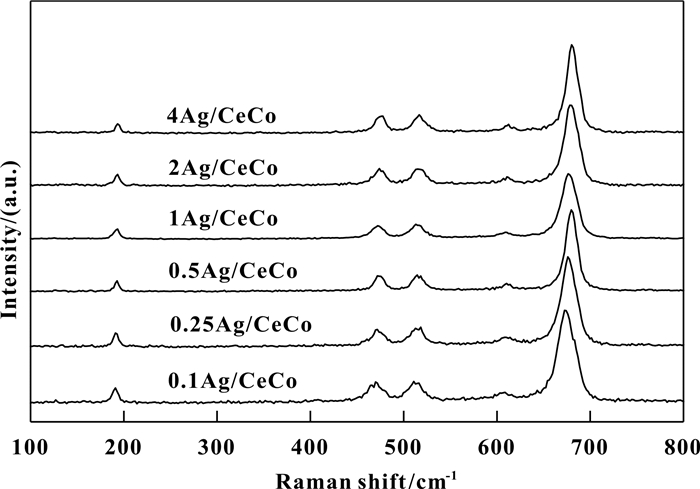
为了进一步探究不同负载Ag含量对催化剂结构影响, Raman光谱实验进一步开展, 其测试结果如图 8所示.在100~800 cm-1范围内, 检测出明显分别属于Co3O4四面体位置振动和八面体位置振动的F2g和Eg模式.所有样品中仍未发现Ag的散射峰, 说明其高度分散或难以检测. Ag/CeCo-OA由于少量Ce的加入, 位于689 cm-1处的峰位置出现红移, 而根据图 8不难发现, 随着Ag含量的增加检测到A1g伸缩振动峰朝较高波数偏移, 说明Ag物种与载体之间存在强相互作用力, 且随含量的增加而增加.另一方面, 观测到随着Ag含量的增加, A1g相应的半峰宽轻微增加, 特别是对于1Ag/CeCo, 该现象与高度缺陷结构的形成有关, 这可能有利于将吸附的氧分子活化为活性氧物种[22].随着Ag含量的进一步增加, 2Ag/CeCo和4Ag/CeCo催化剂中A1g的半峰宽不再继续减小, 与1Ag/CeCo相比反而出现轻微增加.因此, 1Ag/CeCo显示出最优异的催化活性.
|
图 8 不同Ag负载量催化剂的拉曼光谱 Fig.8 The Raman spectra of the various catalysts prepared with different Ag contents |
不同沉淀剂制备的催化剂还原性能均通过氢气程序升温还原(H2-TPR)实验测试, 如图 9所示.样品在测试温度范围内主要有两个还原峰, 分别对应于Co3O4的分步还原.低温段的还原峰代表Co3+到Co2+的还原, 形成CoO中间体, 高温段的还原峰则代表Co2+到Co0的还原.根据文献可知, 与纯Co3O4相比, 图例中各样品的还原峰均向低温偏移[23], 表明CeO2和Ag物种的存在有利于Co3O4的还原, 提高了催化剂的氧化还原性能.但是, 经不同沉淀剂制备的催化剂氧化还原性能存在一定差异, 即CeO2-Co3O4复合氧化物载体间二元金属之间相互作用力强弱不同.

|
图 9 不同沉淀剂制备的各催化剂H2-TPR图 Fig.9 The H2-TPR profiles of the various catalysts prepared with different precipitants |
不同Ag负载量催化剂的氧化还原性能的H2-TPR实验结果如图 10所示.位于210 ℃附近低温段的宽还原峰归属于Ag+还原为Ag的H2消耗, 而位于301 ℃附近还原峰则属于Co2+到Co0的H2消耗.催化剂的还原温度随着Ag含量的增加向低温偏移, 表明Ag的加入有助于催化剂的氧化还原性能的提高.所以, 1Ag/CeCo形成更多的缺陷结构, 更有利于催化活性.

|
图 10 不同Ag负载含量催化剂的H2-TPR图 Fig.10 H2-TPR profiles of various catalysts prepared with different Ag contents |
通过共沉淀法制备了一系列利用不同沉淀剂合成的Ag/CeO2-Co3O4催化剂.研究表明, 所有催化剂对甲醛氧化降解都表现出优异的催化性能, WHSV=30 000 mL·g-1·h-1时, 均能在≤90 ℃实现甲醛的完全净化, 其T90顺序为: Ag/CeCo-OA < Ag/CeCo-Na < Ag/CeCo-NH3 < Ag/CeCo-K < Ag/CeCo-NH4.表征结果发现, 草酸沉淀降低了Ce-Co氧化物的结晶度, Co2+含量增加, 能够提供更多的氧空位, 进而促进氧分子的活化与迁移, 有利于提高催化活性.
此外, 通过过量浸渍法于草酸沉淀制得的CeO2-Co3O4载体上负载不同Ag含量(0.1%~4%(重量百分比))的Ag/CeO2-Co3O4催化剂,实验结果发现, 当Ag负载量仅为0.1%(重量百分比)时, 能够在100 ℃实现甲醛的完全去除.其催化效果优于目前大部分负载型Ag基催化剂, 且贵金属负载含量极低.研究表明, Ag负载量小于1%(重量百分比)时, 活性与负载量成正比关系, Ag负载量大于1%(重量百分比)并无明显变化, 在80 ℃下甲醛的转化率为100%.
| [1] |
Zhang Yi(张溢), Shi Ji(石琎), Zhang Zhi-xiang(张志翔), et al. Study on simultaneous removal of formaldehyde and ozone by manganeae oxygen octahedral molecular sieve at room temperature(锰氧八面体分子筛室温同时去除甲醛和臭氧的性能研究)[J]. J Mol Catal(China)(分子催化), 2019, 33(3): 1–8.
|
| [2] |
Hu Bing(胡兵), Zhang Xu-yi(张徐毅), Guo Peng-fei(郭鹏飞), et al. Research progress on detection methods of trace formaldehyde in food packaging materials(食品包装材料中微量甲醛检测方法的研究进展)[J]. Light Indus Technol(轻工科技), 2019, 35(7): 25–26.
|
| [3] |
Xu Kuang-liang(徐匡亮), Yan Zhao-xiong(严朝雄), Jin Mei(晋梅), et al. Catalytic oxidation of formaldehyde at room temperature over Pt/CuO catalyst prepared from different(不同前驱体制备的Pt/CuO室温催化氧化甲醛性能的研究)[J]. J Huanggang Normal Univer(黄冈师范学院学报), 2019, 39(3): 52–56.
DOI:10.3969/j.issn.1003-8078.2019.03.11 |
| [4] |
Che Xiao-li(车晓莉). Progress in catalytic combustion catalyst of formaldehyde(甲醛催化燃烧催化剂研究进展)[J]. Shandong Chem Indus(山东化工), 2018, 47(19): 64–66.
DOI:10.3969/j.issn.1008-021X.2018.19.025 |
| [5] |
Gao Han(高寒), Dong Yan-chun(董艳春), Zhou Shu-yuan(周术元). Catalytic combustion of volatile organic compounds by noble metals catalysts(贵金属催化剂催化燃烧挥发性有机物(VOCs)的研究进展)[J]. Environ Engineer(环境工程), 2019, 37(3): 136–141.
|
| [6] |
Zeng Jun-lin(曾俊淋), Liu Xiao-long(刘霄龙), Wang Jian(王健), et al. Advances in noble metal catalysts for catalytic oxidation of volatile organic compounds(贵金属催化剂对VOCs催化氧化的研究进展)[J]. Environ Engineer(环境工程), 2015, 33(11): 72–77.
|
| [7] |
Han Shuai(韩帅), He Yong-jun(贺拥军), Liang Yao-dong(梁耀东). The lastest research in removal of formaldehyde by catalytic oxidation(催化氧化法去除甲醛最新研究进展)[J]. Appl Chem Indus(应用化工), 2018, 47(5): 1019–1022.
DOI:10.3969/j.issn.1671-3206.2018.05.042 |
| [8] |
Zhang Chang-bin(张长斌), He Hong(贺泓), Wang Lian(王莲), et al. Review of noble metal catalysts for the oxidation of formaldehyde and air purification in indoor environment at room temperature(负载型贵金属催化剂用于室温催化氧化甲醛和室内空气净化)[J]. Chin Sci Bull(科学通报), 2009, 54(3): 278–286.
|
| [9] |
Gao Ming-ming(高明明), Zhao Huan-juan(赵欢娟), Mu Bo(牟博), et al. Study of noble metal catalysts for the oxidation of formaldehyde at low temperature(负载型贵金属低温催化氧化甲醛催化剂的研究)[J]. Chem Engineer(China)(化学工程), 2019, 47(2): 18–24.
DOI:10.3969/j.issn.1005-9954.2019.02.004 |
| [10] |
Chen Can-chang(陈参昌). Study on catalytic oxidation of formaldehyde over silver-based catalysts(甲醛催化氧化Ag基催化剂性能的研究)[D]. Xi'an Shiyou Univ(西安石油大学), 2018.
|
| [11] |
Zhang Li(张丽), Liang Qing-man(梁青满), Ning Hong-yu(宁弘宇), et al. Photocatalytic performance of CuO/CuAl2O4 composite photocatalysts modified by precious metals (Pt, Ag, Ru)(贵金属(Pt, Ag, Ru)负载修饰CuO/CuAl2O4复合光催化剂及其光催化性能)[J]. Min Metall Engineer(矿冶工程), 2018, 38(1): 115–118.
DOI:10.3969/j.issn.0253-6099.2018.01.028 |
| [12] |
Ma Xiao-kun(马孝坤). Preparation of Pd and Au based precious metal catalysts and their catalytic performance for the electrooxidation of Na BH (Pd、Au基贵金属催化剂的制备及催化NaBH4电氧化性能的研究)[D]. Harbin Engineer Univer(哈尔滨工程大学), 2018.
http://cdmd.cnki.com.cn/Article/CDMD-10217-1018286063.htm |
| [13] |
Chen Yang(陈阳), Yang Xiao-yan(杨晓燕), Zhang Peng(张鹏), et al. Noble metal-supported rod-like ZnO photocatalysts with enhanced photocatalytic proformance(贵金属负载的棒状ZnO复合光催化剂的制备及其提升的光催化性能)[J]. Acta Phys -Chim Sin(物理化学学报), 2017, 33(10): 2082–2091.
DOI:10.3866/PKU.WHXB201705176 |
| [14] |
Qu Z, Wang H, Wang S, et al. Role of the support on the behavior of Ag-based catalysts for NH3 selective catalytic oxidation (NH3-SCO)[J]. Appl Surf Sci, 2014, 316(10): 373–379.
|
| [15] |
Shi Xin-yu(石新雨), Chu Wei(储伟). Effect of support and Ag loading on the performance of silver-based catalysts for selective catalytic reduction of NO by C3H6(载体及银含量等参数对丙烯选择还原NO用银基催化剂性能的影响)[J]. Nat Gas Chem Indus(天然气化工(C1化学与化工)), 2009, 34(4): 47–52.
DOI:10.3969/j.issn.1001-9219.2009.04.012 |
| [16] |
Fan Z Y, Zhang Z X, Fang W J, et al. Low-temperature catalytic oxidation of formaldehyde over Co3O4 catalysts prepared using various precipitants[J]. Chin J Catal, 2016, 37(6): 947–954.
DOI:10.1016/S1872-2067(15)61086-5 |
| [17] |
Chen B B, Shi C, Crocher M, et al. Catalytic removal of formaldehyde at room temperature over supported gold catalysts[J]. Appl Catal B, 2013, 132、133(3): 245–255.
|
| [18] |
Peng J, Wang S. Performance and characterization of supported metal catalysts for complete oxidation of formaldehyde at low temperatures[J]. Appl Catal B, 2007, 73(3/4): 282–291.
|
| [19] |
Sun X C, Lin J, Guan H L, et al. Complete oxidation of formaldehyde over TiO2, supported subnanometer Rh catalyst at ambient temperature[J]. Appl Catal B, 2018, 226(6): 575–584.
|
| [20] |
Lou Y, Ma J, Cao X M, et al. Promoting effects of In2O3 on Co3O4 for CO oxidation:Tuning O2 activation and CO adsorption strength simultaneously[J]. ACS Catal, 2014, 4(11): 4143–4152.
DOI:10.1021/cs501049r |
| [21] |
Wang Z, Wang W Z, Zhang L, et al. Surface oxygen vacancies over Co3O4 mediated catalytic formaldehyde oxidation at room temperature[J]. Catal Sci Technol, 2016, 6(11): 3845–3853.
DOI:10.1039/C5CY01709B |
| [22] |
Ren Q M, Feng Z T, Mo S P, et al. 1D-Co3O4, 2D-Co3O4, 3D-Co3O4, for catalytic oxidation of toluene[J]. Catal Today, 2019, 332(7): 160–167.
|
| [23] |
Fan A Y, Fang W J, Zhang Z X. Highly active rod-like Co3O4 catalyst for the formaldehyde oxidation reaction[J]. Catal Commun, 2018, 103(1): 10–14.
|
 2019, Vol. 33
2019, Vol. 33


