2. 昆明理工大学 环境科学与工程学院, 云南 昆明 650504;
3. 昆明贵研催化剂有限责任公司 贵金属催化技术与应用国家地方联合工程实验室, 云南 昆明 650106
2. Kunming University of Science and Technology, School of Environmental Science and Engineering, Kunming 650504, China;
3. State-Local Joint Engineering Laboratory of Precious Metal Catalytic Technology and Application, Kunming Sino-platinum Metals Catalysts Co. Ltd, Kunming 650106, China
汽车尾气排放是城市大气“霾化学”NOx污染的重要来源[1].与国V标准相比, 国VI标准的NOx污染物排放限值大幅度降低, 使得稀燃工况下NOx净化成为汽车尾气治理领域的研究热点[2]. NOx存储-还原(NSR)技术可有效降低NOx排放, 是最具有应用前景的汽车NOx排放控制技术之一[3-4].
长期以来, Pt/BaO/Al2O3体系催化剂普遍应用于NSR技术, 受到了广泛关注和高度重视[5].我们前期研究发现, MnOx添加能够明显提高催化剂的NOx存储能力[6]. Xiao等[7]通过物理混合法制备Mn/Ba/Al2O3-Pt/Ba/Al2O3催化剂, 结果发现在300~500 ℃温度范围内该催化剂比双倍铂负载量的Pt/Ba/Al2O3具有更高稀燃NO氧化-存储活性和NOx脱除效率.
在实际汽车尾气中存在高浓度的H2O和CO2组分, 这些组分对NOx存储-还原性能的影响不容忽视. Lietti等[8]发现, 添加0.3%~ 3%CO2组分显著降低低温NOx存储能力, 而添加1%H2O组分促进低温NOx存储, 但抑制高温NOx存储.查尔默斯理工大学Olsson研究团队[9]研究发现, H2O和CO2对Pt/Ba/Al2O3催化剂的NOx存储性能均有抑制作用, 且与H2O含量成反比, 富燃阶段CO2能够促进NOx的释放, 促使低温区NH3副产物的生成. Cao等[10]研究了CO2组分浓度对NOx存储吸附结构的影响, 发现增加CO2浓度不利于BaO-NO2形式存储, 抑制亚硝酸盐和硝酸盐物种的形成. Schouten课题组[11]的研究结果表明, H2O的存在能够抑制NO氧化为NO2, 进而影响Pt/Ba/Al2O3催化剂的NOx存储性能.
然而, H2O和CO2组分对Pt/Ba-MnOx/Al2O3催化剂的NOx存储能力及存储速率、还原产物分布特性的影响还有待探讨.我们采用分步浸渍法制备了Pt/Ba-MnOx/Al2O3催化剂, 并研究H2O、CO2对NOx存储与还原特性的影响.
1 实验部分 1.1 试剂与原料乙酸锰((CH3CO2)2Mn·4H2O, 99.0%, 分析纯, 上海麦克林生化科技有限公司);乙酸钡((CH3CO2)2Ba, 99.0%, 分析纯, 西陇科学股份有限公司);氧化铝(γ-Al2O3, 99.99%, 分析纯, 阿拉丁试剂有限公司);羟胺铂(Pt(NH3)4(OH)2, Pt含量为14.69%, 贵研铂业股份有限公司).
1.2 催化剂的制备采用分步浸渍法制备Pt/Ba-MnOx/Al2O3催化剂.称取56.45 g乙酸锰、53.82 g乙酸钡, 分别在适量的去离子水中充分溶解.称取148.11 g γ-Al2O3粉末分散于去离子水中, 加入乙酸锰溶液, 80 ℃水浴搅拌7 h, 120 ℃过夜干燥, 经550 ℃静置空气焙烧3 h后得到MnOx/Al2O3粉末;将乙酸钡溶液加入到MnOx/Al2O3悬浮液中, 80 ℃水浴搅拌7 h, 120 ℃干燥, 550 ℃静置空气焙烧3 h, 再经850 ℃静置空气焙烧4 h, 得到Ba-MnOx/Al2O3粉末样品, 其中, Mn、Ba的目标质量百分含量分别为10%MnO2、16%BaO.
以Ba-MnOx/Al2O3粉末为载体, 选用羟胺铂(Pt(NH3)4(OH)2)作为前驱体, 采用浸渍法制备铂负载量为1.2%(质量分数)的催化剂, 经590 ℃静置空气焙烧2 h后得到的新鲜催化剂Pt/MnBaAl. 800 ℃静置空气中焙烧16 h得到老化样品Pt/MnBaAl-A.
1.3 催化剂的表征Pt的分散度测试在CHEMBET 3000型化学吸附仪上完成.将100 mg催化剂装入U型石英管中, 在氦气气氛下加热升温至450 ℃进行脱气处理30 min后降至50 ℃, 稳定60 min, 连续脉冲注射高纯CO(体积分数为99.9%)10次, 并采用TCD检测气体信号.
催化剂表面的活性贵金属Pt原子数Ns按照CO/Pt(1:1)的比例进行计算[12], Pt分散度DPt按公式(1)计算[13]:
| $ {D_{Pt}} = \frac{{{V_a}/22\;414}}{{m{W_{Pt}}/195}} $ | (1) |
式中, Va表示为CO的吸附总量, (mL, STP);m表示为实验中催化剂样品的实际质量, 单位为g;WPt表示经ICP-OES测定的催化剂中Pt实际负载量.
| $ d{\rm{ }} = \frac{{1.1}}{{{D_{Pt}}}} $ | (2) |
采用德国STA-449-F3型同步热分析仪进行储氧能力(OSC)测试.将100 mg催化剂装入Al2O3坩埚中, 在10% O2/N2气氛下升温至550 ℃, 进行氧化处理30 min后, 切换至氮气降温至50 ℃并稳定45 min, 切换至10% H2/Ar, 以10 ℃/min的速率升温至550 ℃恒温60 min, 实时记录样品的质量变化. OSC值由还原过程中样品质量损失百分比计算得到. OSC(μmol/g)按公式(3)计算:
| $ OSC = \frac{\lambda }{{1.6 \times {{10}^{ - 6}}}} $ | (3) |
式中, λ表示催化剂样品质量损失百分比.
1.4 催化剂的评价采用常压多功能微型固定床反应装置评价催化剂的NOx存储性能.将约1.0 g催化剂(0.450~0.280 mm)样品装填于内径为5 mm的反应管内, 在500 ℃下预处理40 min, 预处理气氛为5% O2/N2, 气体总流量为500 mL/min, 气体体积空速(GHSV)为30 000 mL/(h·g), 吸附时间为50 min, 吸附温度分别为200、300和400 ℃. NOx存储气氛组成如表 1所示.通过MKS公司MultiGas系列FT-IR红外光谱仪实时在线检测NO、NO2浓度. NOx存储量(NSC)由公式(4)计算得到:
| 表 1 催化剂的NOx存储性能测试配气组成 Table 1 Composition of gas mixture for NOx storage capacity of catalyst |
| $ NSC{\rm{ }} = \frac{{\int_0^t {{{\left[ {N{O_x}} \right]}_{in}}} - {{\left[ {N{O_x}} \right]}_{out}}dt{\rm{ }} \times {\rm{ }}v}}{{22.4{\rm{ }} \times {\rm{ }}{m_{cat.}}}} $ | (4) |
式中, V为反应气体的流速, [NOx]out、[NOx]in分别为NOx的出、入口浓度, t为NOx吸附时间, mcat.为催化剂的实际装填质量.
NOx存储效率由公式(5)计算得到:
| $ \eta N{O_x} = \left[ {1 - \frac{{\int_0^t {{{\left[ {N{O_x}} \right]}_{out}}} dt}}{{{{\left[ {N{O_x}} \right]}_{in}} \times {\rm{ }}t}}} \right] \times 100\% $ | (5) |
式中, η为NOx存储效率.
待吸附结束后关闭所有气体的质量流量计, 降温至100 ℃, 然后在0.4% CO/N2气氛中以10 ℃/min的速率升温至600 ℃, 采用FT-IR红外光谱仪实时在线检测CO、NO、N2O、NO2和NH3的浓度.
同样采用常压多功能微型固定床反应装置评价催化剂的NOx存储-还原性能.将约1.0 g催化剂(0.450~0.280 mm)装填于内径为5 mm的反应管内, 在500 ℃下预处理40 min, 预处理气氛为5% O2/N2, 气体总流量为2000 mL/min.稀燃气氛: 0.04% NO + 5% O2 + 5% CO2 + 5% H2O, 富燃条件: 0.35% CO + 0.1% C3H6 + 5% CO2 + 5% H2O, 具体反应条件如表 2所示.采用FT-IR红外光谱仪实时在线检测NO2、NO、N2O、NH3浓度.待各气体组分至少有3个反应循环峰面积几乎相等时开始记录, 实时在线采集至少5个反应循环的NO2、NO、N2O、NH3浓度数据.
| 表 2 催化剂的NOx存储-还原性能测试配气组成 Table 2 Composition of gas mixture for NOx storage-reduction capacity of catalyst |
NOx脱除效率(XNOx)、NO转化率(XNO)分别由公式(6)和(7)计算得到[15]:
| $ {X_{N{O_x}}}\left( \% \right){\rm{ }} = 100 \times \frac{{\int_0^{{t_c}} {{{\left[ {N{O_x}} \right]}_{in}}} - {{\left[ {N{O_x}} \right]}_{out}}dt}}{{{{\left[ {N{O_x}} \right]}_{in}} \times {\rm{ }}t}} $ | (6) |
| $ {X_{NO}}\left( \% \right){\rm{ }} = 100 \times \frac{{\int_0^{{t_c}} {{{\left[ {NO} \right]}_{in}}} - {{\left[ {NO} \right]}_{out}}dt}}{{{{\left[ {NO} \right]}_{in}} \times {\rm{ }}t}} $ | (7) |
NH3、N2O、NO2、N2的选择性分别由公式(8-11)计算得到[16]:
| $ {S_{N{H_3}}}\left( \% \right){\rm{ }} = \frac{{\int_0^{{t_c}} {{{\left[ {N{H_3}} \right]}_{out}}dt} }}{{\int_0^{{t_c}} {{{\left[ {NO} \right]}_{in}}} - {{\left[ {NO} \right]}_{out}}dt}} $ | (8) |
| $ {S_{{N_2}O}}\left( \% \right){\rm{ }} = \frac{{2\int_0^{{t_c}} {{{\left[ {{N_2}O} \right]}_{out}}dt} }}{{\int_0^{{t_c}} {{{\left[ {NO} \right]}_{in}} - {{\left[ {NO} \right]}_{out}}dt} }} $ | (9) |
| $ {S_{N{O_2}}}\left( \% \right){\rm{ }} = \frac{{\int_0^{{t_c}} {{{\left[ {N{O_2}} \right]}_{out}}dt} }}{{\int_0^{{t_c}} {{{\left[ {NO} \right]}_{in}} - {{\left[ {NO} \right]}_{out}}dt} }} $ | (10) |
| $ \begin{array}{l} {S_{{N_2}}}\left( \% \right){\rm{ }} = 100\% - {S_{N{H_3}}} - {S_{{N_2}O}} - {S_{N{O_2}}} \end{array} $ | (11) |
式中, SNH3、SN2O、SNO2、SN2分别为NH3、N2O、NO2、N2的选择性, tc为300 s.
2 结果与讨论 2.1 Pt分散度与催化剂储氧能力表 3列出了Pt/MnBaAl和Pt/MnBaAl-A样品的CO吸附量、Pt的分散度和平均晶粒尺寸及催化剂储氧能力的对比结果.从表 3可以看出, Pt/MnBaAl和Pt/MnBaAl-A催化剂的分散度分别为35%和20%, 铂纳米晶的平均晶粒尺寸分别为3.1和5.4 nm, 储氧能力分别为1131和775 μmol/g, 说明催化剂表面铂原子数降低, 高温导致了铂纳米颗粒的烧结和储氧性能的劣化.
| 表 3 Pt/MnBaAl和Pt/MnBaAl-A催化剂样品分散度与储氧能力分析结果 Table 3 Dispersion and oxygen storage capacity of Pt/MnBaAl and Pt/MnBaAl-A catalyst samples |
图 1为在200、300、400 ℃时Pt/MnBaAl和Pt/MnBaAl-A催化剂的NOx存储能力对比图(NOx储存量的实验计算相对误差绝对值≤ 0.5%).由图 1可知, 在吸附气氛为NO+O2, 存储温度为300 ℃时Pt/MnBaAl和Pt/MnBaAl-A均达到最大的NOx存储量, 分别为381、361 μmol/g.在反应气中加入CO2、H2O或CO2+H2O组分, NOx存储能力均有不同程度的降低, 这些组分对NOx存储性能的抑制效果按CO2> CO2 + H2O > H2O依次降低.

|
图 1 Pt/MnBaAl (a)和Pt/MnBaAl-A (b)催化剂的NOx存储能力对比图 Fig.1 NOx storage capacities (NSC) of the Pt/MnBaAl (a) and Pt/MnBaAl-A (b) catalysts (Adsorption time 50 min, GHSV= 30 000 mL/(h·g)) |
在NO+O2存储气氛的基础上, 额外添加5% H2O导致Pt/MnBaAl催化剂的NOx存储能力在200、300和400 ℃分别下降了9.8%、4.5%、2.7%, 表明H2O抑制NOx存储主要表现在低温区.与之相比, CO2对Pt/MnBaAl催化剂的存储性能的影响更为明显, 其NOx存储量分别下降了24.6%、28.1%、65.2%, 表明CO2对NOx存储能力的抑制效果比H2O更为明显, 且在高温区尤为突出, 这可归因于CO2的存在会抑制(亚)硝酸盐形式吸附存储[10].与NO+O2+ CO2存储气氛相比, 同时添加CO2和H2O使得催化剂的NOx存储性能略有改善, 这是因为H2O能够减弱CO2与NOx在Ba位点上的竞争性吸附[8], 但双组分的添加对NOx存储性能的抑制作用却远大于H2O, 这表明CO2对抑制NOx存储起主导作用[9].
经800 ℃老化16 h后的Pt/MnBaAl-A样品在存储气氛为NO+O2, 存储温度为200、300和400 ℃时, NOx存储量分别为315、361和278 μmol/g, 其存储能力分别下降了12.0%、5.2%、25.5%, 这与高温导致催化剂表面铂原子数降低有密切联系.在NO+O2存储气氛的基础上, 额外添加5% H2O, Pt/MnBaAl-A的NOx存储能力分别下降了20.0%、3.9%、1.4%;而添加CO2组分, 其NOx存储能力分别下降30.2%、35.7%、64.4%, 可见CO2表现出更为明显的抑制作用.而同时添加CO2和H2O时对Pt/MnBaAl-A催化剂的NOx存储性能影响与新鲜样品一致.
图 2为在200、300和400 ℃时不同气氛下Pt/ MnBaAl、Pt/MnBaAl-A催化剂的NOx存储速率对比图.随着温度的升高, H2O对Pt/MnBaAl、Pt/MnBaAl-A催化剂的NOx存储速率的抑制作用降低, 其中在400 ℃时催化剂的NOx存储速率与吸附气氛为NO+O2时基本保持一致, 进一步表明H2O对催化剂NOx存储能力的抑制作用主要表现在低温区.同时, CO2对催化剂NOx存储速率的抑制作用随着反应温度的升高进一步增大.此外, 在200~400 ℃温度范围内CO2对催化剂存储速率的抑制作用大于H2O, 且随着反应温度的升高, CO2、H2O对NOx存储速率抑制作用的差异性更为显著.

|
图 2 不同温度下NOx存储速率对比图 Fig.2 NOx storage rates measured under lean conditions at different temperature (Adsorption time 50 min, GHSV= 30 000 mL/(h·g)); Solid: Pt/MnBaAl, dash: Pt/MnBaAl-A |
在0.4% CO/N2气流中进行程序升温表面反应(CO-TPSR), 研究了催化剂在不同存储气氛下存储NOx物种的瞬态还原性. 图 3、图 4分别为Pt/MnBaAl和Pt/MnBaAl-A催化剂在300 ℃不同气氛下吸附NOx后的CO-TPSR曲线对比结果.吸附气氛为NO+O2时, Pt/MnBaAl催化剂的T90(CO)为186 ℃, 在150~285 ℃温度范围内有NO和少量的N2O释放, 在285~380 ℃温度范围内CO被完全转化, 且在304 ℃又有少量的NO释放, 这与催化剂中尚未还原的表面Ba(NO3)2分解有着密切联系.整个还原过程中未检测到NO2, 这可归因于CO与因NOx存储而形成的Ba(NO3)2发生了如下化学反应(I)、(II)和(III)[17-18]:

|
图 3 300 ℃不同气氛下吸附NOx后Pt/MnBaAl催化剂的CO-TPSR曲线对比 Fig.3 CO-TPSR profiles of Pt/MnBaAl catalysts with NOx adsorption under different gas compositions at 300 ℃ |

|
图 4 300 ℃不同气氛下吸附NOx后Pt/MnBaAl-A催化剂的CO-TPSR曲线对比 Fig.4 CO-TPSR profiles of Pt/MnBaAl-A catalysts with NOx adsorption under different gas compositions at 300 ℃ |
Ba(NO3)2+ 2CO → Ba(NO2)2+2CO2(Ⅰ)
Ba(NO3)2+ 8CO → Ba(NCO)2+6CO2(Ⅱ)
Ba(NO3)2+ 5CO → BaCO3 + N2+4CO2(Ⅲ)
5Ba(NCO)2+3Ba(NO3)2→ 8BaCO3+8N2+2CO2 (Ⅳ)
Ba(NCO)2 + Ba(NO2)2→ 2BaCO3+2N2(Ⅴ)
在CO的还原过程中有一定量的NH3产生, 这可归因于催化剂表面羟基与解离N原子的反应.此外, 形成的Ba(NCO)2与硝酸盐和亚硝酸盐通过反应(IV)和(V)生成N2[17].如表 4所示, 整个还原过程中, CO的消耗量为1842.8 μmol/g, 其消耗量远大于催化剂的NOx存储量, 这可归因于CO在催化剂表面发生催化氧化及歧化反应[17, 19].其中, 含氮气态污染物(NO、N2O、NH3)产生64.5 μmol/g, 为NOx存储量的16.9%, 其中主要污染物为NO, 占总含氮气态污染物的84.8%.与之相比, NOx吸附气氛中额外添加H2O, T90(CO)向高温偏移了14 ℃左右, 在160~285 ℃温度范围内有大量的NO产生, 且伴有少量的N2O产生, 在285~405 ℃温度范围内CO被完全转化, 且在290 ℃又有少量的NO产生.整个还原过程中, CO的消耗量为1673.8 μmol·g-1, 含氮气态污染物产生85.1 μmol·g-1, 占NOx存储量的23.38%, 其中NO占总含氮气态污染物的87.16%.在添加CO2时, T90(CO)向高温偏移了约5 ℃, NO和N2O在150~285 ℃范围内产生, CO的消耗量为1581.5 μmol·g-1, 含氮气态污染物产生93.0 μmol·g-1, 占NOx存储量的33.9%.同时添加CO2和H2O时, CO的消耗量为1499.4 μmol·g-1, 含氮气态污染物产生87.1 μmol·g-1, 占NOx存储量的28.28%.添加CO2与H2O均能造成含氮气态污染物比例增加, 含氮气态污染物生成量与NOx存储量的比值按CO2> CO2 + H2O > H2O的顺序依次降低.
| 表 4 Pt/MnBaAl和Pt/MnBaAl-A在CO-TPSR中CO的消耗量和产物生成量 Table 4 Consumed and produced CO amounts during CO-TPSR over Pt/MnBaAl and Pt/MnBaAl-A |
相对于Pt/MnBaAl催化剂而言, Pt/MnBaAl-A的T90(CO)向高温偏移了~50℃, 说明老化后催化剂对NOx的还原能力明显减弱, 同时产生大量的含氮气态污染物, 其比例按照NO+O2+CO2、NO+O2+CO2+ H2O、NO+O2+H2O、NO+O2存储气氛依次为76.3%、67.0%、66.8%、66.5%, 均远大于50%.
2.4 NOx存储-还原性能表 5为反应温度在200、300和400 ℃时Pt/MnBaAl和Pt/MnBaAl-A催化剂NOx脱除效率、NO转化率和产物选择性的对比结果.从表 5中可以看出, 对于Pt/MnBaAl催化剂而言, 400 ℃为催化剂NOx转化的最佳温度点, NOx转化率均大于90%.与H2O相比, CO2的添加使得NOx转化率降低了约7.2%, 表明CO2对催化剂NOx脱除有抑制作用, 而这一现象在300 ℃时也有所体现.随着温度的降低, 催化剂NOx脱除效率进一步降低, 当反应温度为200 ℃时, NOx的脱除性能严重下降, 其NOx脱除效率均远低于30%, 这可归因于Pt-CO的强相互作用使得催化剂上活性Pt位点失活从而抑制了存储NOx物种的分解及还原[20].与Pt/MnBaAl相比, Pt/MnBaAl-A在400 ℃时CO2对催化剂NOx脱除抑制作用更为明显;当反应温度为200和300 ℃时, 其NOx脱除效率均远低于30%.此外, 在200~300 ℃的温度范围内, H2O的添加后反应中有明显的副产物NH3产生, 这是因为CO和C3H6分别发生水煤气变换和蒸汽重整反应进而产生H2 , 并进一步还原NOx[21-22].
| 表 5 不同组分下催化剂的NOx转化率和产物选择性 Table 5 NOx conversions and product selectivities of the catalyst under different components |
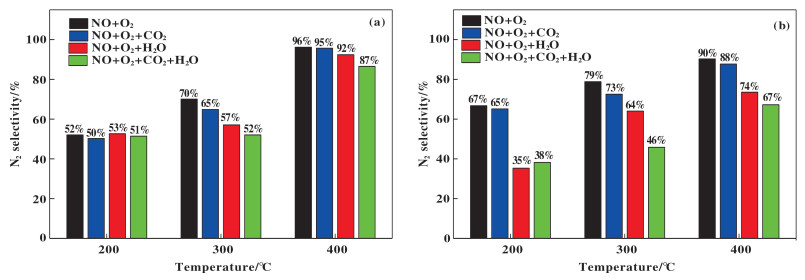
图 5为在200、300和400 ℃时Pt/MnBaAl和Pt/MnBaAl-A催化剂的N2选择性对比图.由图 5可知, 400 ℃是N2选择性的最佳温度点, 且在200~ 400 ℃温度范围内N2选择性与温度呈正相关, 与NOx转化率一致.在300~400 ℃温度范围内, 不同组分对催化剂N2选择性的抑制作用按CO2 + H2O > H2O > CO2的顺序依次降低, 而在200 ℃并未表现出明显的差异.与Pt/MnBaAl相比, 在低温下, H2O对Pt/MnBaAl-A的N2选择性抑制作用更为显著, 在300~400 ℃温度范围内不同组分对N2选择性影响与Pt/MnBaAl保持一致.
|
图 5 Pt/MnBaAl (a)和Pt/MnBaAl-A (b)催化剂的N2选择性对比图 Fig.5 N2 selectivities of the Pt/MnBaAl (a) and Pt/MnBaAl-A (b) catalysts |
通过对比试验研究, 发现CO2、H2O或CO2+H2O均能抑制催化剂的NOx存储能力, 其抑制效果按CO2> CO2 + H2O > H2O的顺序依次降低, H2O对催化剂NOx存储能力的抑制作用主要表现在低温区, CO2对催化剂NOx存储能力的抑制作用在高温区更为显著. CO2对催化剂NOx存储速率的抑制效果高于H2O, 且随着温度的升高其NOx存储速率的差异更为明显.还原过程中, CO2、H2O或CO2+H2O对催化剂N2选择性抑制作用按CO2 + H2O > H2O > CO2的顺序依次降低.
| [1] |
Chu Bi-wu(楚碧武), Ma Qing-xin(马庆鑫), Duan Feng-kui(段凤魁), et al. Atmospheric"Haze Chemistry": Concept and research prospects(大气"霾化学":概念提出和研究展望)[J]. Prog Chem(化学进展), 2020, 32(1): 1–4.
|
| [2] |
GB18352.6-2016. Limits and measurement methods for emissions from light-duty vehicles (CHINA 6) (轻型汽车污染物排放限值及测量方法(中国第六阶段))[S]. Beijing(北京): Ministry of Environmental Protection (环境保护部), Administration of Quality Supervision, Inspection and Quarantine (国家质量监督检验检疫总局), 2016.
|
| [3] |
Roy S, Baiker A. NOx storage-reduction catalysis: From mechanism and materials properties to storage-reduction performance[J]. Chem Rev, 2009, 109(9): 4054–4091.
|
| [4] |
Wang T, Jia L W, Wang X T, et al. Enhancing low-temperature NOx storage and reduction performance of a Pt-based lean NOx trap catalyst[J]. Rare Met, 2019, 38(1): 81–86.
|
| [5] |
Epling W S, Peden C H F, Szanyi J. Carbonate formation and stability on a Pt/BaO/γ-Al2O3 NOx storage/reduction catalyst[J]. J Phys Chem C, 2008, 112(29): 10952–10959.
|
| [6] |
Ren De-zhi(任德志), Wang Cheng-xiong(王成雄), Guo Lv(郭律), et al. Impact of Mn and Ce modification on NOx storage capacity of Pt/BaCO3/Al2O3 catalysts(锰铈改性对Pt/BaCO3/Al2O3催化剂NOx存储性能的影响)[J]. Chin J Rare Metals(稀有金属), 2019.
DOI:10.13373/j.cnki.cjrm.XY19080030 |
| [7] |
Xiao J H, Li X H, Deng S, et al. NOx storage-reduction over combined catalyst Mn/Ba/Al2O3-Pt/Ba/Al2O3[J]. Catal Commun, 2008, 9(5): 563–567.
|
| [8] |
Lietti L, Forzatti P, Nova I. NOx storage reduction over Pt-Ba/γ-Al2O3 catalyst[J]. J Catal, 2001, 204(2): 175–191.
|
| [9] |
Lindholm A, Currier N W, Fridell E, et al. NOx storage and reduction over Pt based catalysts with hydrogen as the reducing agent: Influence of H2O and CO2[J]. Appl Catal B: Environ, 2007, 75(1/2): 78–87.
|
| [10] |
Cao L, Li Z, He L, et al. Influence of CO2 concentration and inlet temperature on adsorption path of lean NOx trap[J]. Energy Procedia, 2019, 158(1): 4383–4388.
|
| [11] |
Scholz C M L, Nauta K M, Croon M H J M D, et al. Kinetic modeling of storage and reduction with different reducing agents(CO, H2, and C2H4) on a Pt-Ba/γ-Al2O3 catalyst in the presence of CO2 and H2O[J]. Chem Eng Sci, 2008, 63(11): 2843–2855.
|
| [12] |
Bourane A, Bianchi D. Heats of adsorption of the linear CO species on Pt/Al2O3 using infrared spectroscopy: Impact of the Pt dispersion[J]. J Catal, 2003, 218(2): 447–452.
|
| [13] |
Yang Chun-yan(杨春雁), Yang Wei-dong(杨卫亚), Ling Feng-xiang(凌凤香), et al. Determination of metal dispersion on supported metal catalyst surface(负载型金属催化剂表面金属分散度的测定)[J]. Chem Ind Eng Prog(化工进展), 2010, 29(8): 97–102.
|
| [14] |
Clayton R D, Harold M P, Balakotaiah V, et al. Pt dispersion effects during NOx storage and reduction on Pt/BaO/Al2O3 catalysts[J]. Appl Catal B: Environ, 2009, 90(3/4): 662–676.
|
| [15] |
Ting W L, Li M, Harold M P, et al. Fast cycling in a non-isothermal monolithic lean NOx trap using H2, as reductant: Experiments and modeling[J]. Chem Eng J, 2017, 326(15): 419–435.
|
| [16] |
Hodjati S, Bernhardt P, Petit C, et al. Removal of NOx part Ⅱ. Species formed during the sorption/desorption processes on barium aluminate[J]. Appl Catal B: Environ, 1998, 19(3/4): 221–232.
|
| [17] |
Forzatti P, Lietti L, Nova I, et al. Reaction pathway of the reduction by CO under dry conditions of NOx species stored onto Pt-Ba/Al2O3 lean NOx trap catalysts[J]. J Catal, 2010, 274(2): 163–175.
|
| [18] |
Castoldi L, Lietti L, Bonzi R, et al. The NOx reduction by CO on a Pt-K/Al2O3 lean NOx trap catalyst[J]. J Phys Chem C, 2011, 115(4): 1277–1286.
|
| [19] |
Zhou Ren-xian(周仁贤), Xu Xiao-ling(徐晓玲), Zheng Xiao-ming(郑小明). Effect of CeO2 on oxidation of CO over Pd/Al2O3 catalyst(氧化铈对Pd/Al2O3表面上CO氧化性能的影响)[J]. Chem J Chin Univer(高等学校化学学报), 1996, 17(3): 443–446.
|
| [20] |
Meunier , Frederic , Marie , et al. Effects of temperature and rich-phase composition on the performance of a commercial NOx storage-reduction material[J]. Appl Catal B: Environ, 2016, 181(2): 534–541.
|
| [21] |
Partridge W P, Choi J S. NH3 formation and utilization in regeneration of Pt/Ba/Al2O3 NOx storage-reduction catalyst with H2[J]. Appl Catal B: Environ, 2009, 91(1/2): 144–151.
|
| [22] |
Koí P, Plát F, Štěpánek J, et al. Global kinetic model for the regeneration of NOx storage catalyst with CO, H2 and C3H6 in the presence of CO2 and H2O[J]. Catal Today, 2009, 147: S257–S264.
|
 2020, Vol. 34
2020, Vol. 34


