2. 北方民族大学 国家民委化工技术基础重点实验室, 宁夏 银川 750021
2. Key Laboratory of Chemical Engineering and Technology, State Ethnic Affairs Commission, North Minzu University, Yinchuan 750021, China
随着工业化进程的不断推进, 化石燃料消耗日趋增大, 全球面临着环境退化和资源短缺的挑战逐渐凸显, 人们认识到, 社会需要在生产和消耗能源的方式上进行转变, 最有效途径是寻找和开发可持续的绿色能源[1-3]. 其中太阳能作为取之不尽的绿色环保能源, 可以一定程度上代替化石燃料, 具有满足世界能源需求和可持续发展的潜力[4-5], 利用可再生太阳能通过氧化和还原来激活化学反应的光催化是解决环境问题和能源枯竭最有效方法之一, 这种光催化系统引起了科学界的极大兴趣[6], 已经应用于产氢[7-8]、有机合成[9]、CO2还原[10]和有机物降解[11]等方面, 并均取得了较为理想的效果.
光热催化利用太阳光的广泛吸收来刺激热化学过程和光化学过程的耦合, 从而协同促进驱动催化反应. 光热催化被解释为光催化反应的热加速和热催化反应的光增强的集成. 在光催化反应的热加速中, 太阳光谱的可见光部分和大部分红外光可能不适合激发空穴/电子, 但是它们的热效应可用于光催化. 在光催化热催化反应中, 光辅助热催化的温度和压力通常低于热驱动的热催化反应[12], 并且两者的有效结合能够超过单一催化形式的效果, 在能源和环境领域具有重大的意义和价值. 现阶段研究的焦点主要集中在对传统催化技术的改良和新型催化技术的开发上, 对此国内外的学者进行了大量的相关研究, 并已经实现在诸多领域的应用.
1 光热催化技术的应用 1.1 光热催化CO2转化长期以来, 传统化石燃料的燃烧导致CO2浓度急剧增加, 2018年全球CO2排放量达到3.70×1010 t, 是自然界吸收总量的2倍. 大量的CO2排放可以加速温室效应, 导致全球变暖和冰川融化, 进而引起海平面上升, 对人类生存环境造成严重威胁[13], 因此除了减少CO2的排放和开发新的可替代能源外, 如何将CO2转化为清洁燃料已逐渐被认为是一种有前途的化学转化方法, 可以同时减轻化石燃料的消耗和全球变暖问题. 通过光催化将CO2还原为燃料是一种有价值的方法, 但是此反应面临着高热量输入和低转换率的问题[14]. 尽管CO2还原是光电子催化反应, 反应温度对其影响较小, 但温度升高可以通过增强热力学来改善反应程度, 甚至表现出光热协同催化作用[15], 因此, 近年来研究者们通过在还原反应中引入光热协同作用, 希望可以提高目标产物的收率和选择性.
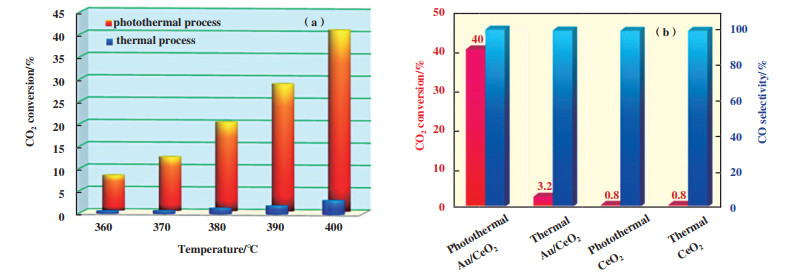
逆水煤气变换(RWGS)反应(CO2+H2→CO+H2O)是典型的CO2还原反应, 热驱动系统可促进高速率的CO2加氢, 反应的缺点是需要较高的温度(250~627 ℃)和压力, 但是引入光催化后, 在相对较低的温度下就能达到与高温相同转化率, 并且选择性进一步提高. Zhang等[15]使用自制的聚光太阳光反应器系统, 用Fe2O3薄膜实现了H2O对CO2的高光热还原. 结果显示产物总转化率比自然光照和室温下的转化率高约700倍, 结合表征分析发现, 在高强度光照射和高温条件下, Fe2O3薄膜可以部分还原形成Fe2O3/Fe3O4异质结, 在高光热条件以及Fe2O3/Fe3O4 Z-方案系统的共同作用下, 极大地提高了CO2的还原效率. Lu等[16]基于具有CeO2纳米棒负载Au纳米颗粒的方案, 构建了一种适用于光热过程的稳定催化剂, 该催化剂作为CO2吸附和活化的最佳载体, 合成后的Au/CeO2催化剂在光热过程中的活性高于热过程中的活性, 同时可实现近100%的CO选择性, 如图 1所示. 结合分析表征发现, 光热过程中的高转化率不应仅归因于热效应, Au对光热过程中高CO2转化率的决定性作用, Au纳米颗粒因等离子体共振的独特能力使其能够吸收光能并产生热电子, 这些电子可能转移到吸附的H2分子中并引起解离. 因此, 光照射有助于克服H2离解步骤中的能量垒, 并有利于随后将CO2加氢成CO.
|
图 1 (a)Au/CeO2催化剂光热和热过程催化转化CO2; (b)不同条件下Au/CeO2和CeO2催化剂在400 ℃时CO2转化率和CO选择性[16] Fig.1 (a) CO2 conversion on Au/CeO2 in photothermal or thermal process; (b) CO2 conversion & CO selectivity on Au/CeO2 or CeO2 catalysts at 400 ℃ under different conditions[16] |
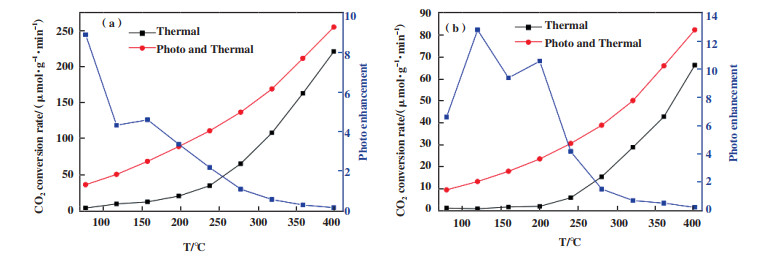
Zhao等[17]通过浸渍法制得Pt/Al2O3催化剂, 并用于光热协同催化CO2加氢反应. 从图 2中可以看出, 在催化加氢的反应中, Pt/Al2O3催化剂表现出光热协同效应, 光辐射显著促进了CO2转化和CO产生速率, 在120 ℃、光照条件下, CO2转化率约为50 μmol·g-1·min-1, 远远高于黑暗条件下的10 μmol·g-1·min-1. 后续通过原位漫反射红外光谱(operando DRIFTS)和密度泛函理论计算(DFT)对光照因素在该催化反应过程的作用机制进行了进一步深入研究, 表明CO气体分子从Pt纳米颗粒上的脱附过程是该反应的重要步骤, 反应过程中CO分子从Pt表面脱附有利于反应活性位点Pt的充分暴露, 光照条件下, 可以引起明显的CO分子吸附位点的转移, 从而促进CO2加氢反应的进行.
|
图 2 CO2在Pt/Al2O3上进行光热加氢时的转化率(a)和CO产生速率(b)[17] Fig.2 CO2 (a) conversion and CO production rates (b) in photothermal CO2 hydrogenation on Pt/Al2O3[17] |
Jia等[18]以Nb2O5纳米棒负载0.5%(质量分数)Pd纳米颗粒为催化剂, 在可见光和近红外光照射下驱动RWGS反应, CO2和H2比例为1∶1时, 催化速率大约是传统热催化(无光照)条件下的5倍, 这表明在Pd@Nb2O5催化剂上的光可以有效地驱动RWGS反应. 分析发现, 在光照下吸收的光子最终热化并产生热量, 导致Pd@Nb2O5催化剂中的局部高温, 加速了RWGS反应. Ghuman等[19]通过热处理In(OH)3纳米晶体, 合成了In2O3-x(OH)y催化剂, 在一定温度和光照下催化RWGS反应, 相较于无光照情况(165 ℃才可观察微量CO生成), 150 ℃即可表现出较高的催化活性, CO2转化率可达15.4 μmol·g-1·h-1, 190 ℃时增加到153 μmol·g-1·h-1. 随后, Hoch等[20]通过把In2O3-x(OH)y涂覆在SiNW得到In2O3-x(OH)y/SiNW膜, 同样用于催化RWGS反应. 结果显示对于均匀涂层的In2O3-x(OH)y/SiNW膜, 高光强度氙灯照射下很容易达到150 ℃, 并且催化活性可达22.0 μmol·g-1·h-1. 诸多研究都为光热CO2加氢反应机理提供见解, 并对其它多相反应的高效光热催化剂的设计提供有益的指导. 这些研究将有助于高效光热催化剂的设计、合成和优化, 利用全太阳光谱将气相CO2转化为有价值的化学品和燃料.
在光热催化的条件下, 烃类产物的转化率和选择性都大大提高. Xu等[21]以葡萄糖辅助溶剂热方法, 制备出具有强界面相互作用的TiO2-G复合材料, 结果表明石墨烯的引入对TiO2的表面积和CO2吸收能力影响不显著, 但极大地改善了光催化剂的电荷载流子分离和表面温度, 使CH4的生产速率高达26.7 μmol·g-1·h-1, 高于纯TiO2的5.1倍. 表征分析发现TiO2-G复合材料具有更好的光热效应, 光诱导的局部光热效应将增强气体分子和电荷载流子的移动, 从而促进它们在石墨烯表面上的反应, 从而生成CH4. Wang等[22]使用热氢气处理过的m-WO3, 在光和热条件下进行了CO2还原实验, 仅考虑CH4作为主要产物, 只有可见光照射的情况下生成微量CH4, 但在光热耦合条件下表现出较高的催化CO2还原性能(25.77 μmol·g-1·h-1). 此外, CH4的额外收率增加约20%, 推测这可能是光和热的结合产生了独特的协同光/热催化作用所致. Meng等[23]制备了一系列Ⅷ族金属(Ru、Rh、Ni、Co、Pd、Pt、Ir和Fe)负载型纳米催化剂, 并用于CO2与H2转化为CH4的反应, 结果显示通过光热活化实现的CO2反应速率比单一光催化方法高出大约6个数量级, 且CH4的选择性均达到99%以上. Chen等[24]以MOFs为模板制备了分散良好的Co/Al2O3纳米颗粒催化剂, 用于光热催化CO2制备CH4, 结果显示, 引入适量Co可以显著提高CO2转化率和CH4选择性, 产率高达6036 μmol·g-1·h-1, CH4选择性为97.7%. CO2甲烷化为典型的放热反应, 反应温度对催化过程有很大影响, 提高温度有助于提高反应物的流动性, 从而促进反应的进行. 在整个催化过程中, 催化剂对整个太阳光谱都表现出强的吸收, 反应温度迅速升高. 因此可以看出, 光热协同催化在CO2催化转化为CH4体系中得到了较单一技术优越的催化性能和选择性.
甲醇同样是CO2转化生成的重要有机化合物, 它可以作为液体燃料, 但反应本身却同样受到热力学和操作条件的限制. 除了热激发之外, 还可以通过光激发具有光子响应的半导体或金属来产生热电子, 这使得光催化CO2还原能够在温和的条件下发生. 虽然升高的温度有利于CO2活化, 但由于反应的放热性质以及在较高温度下存在竞争性的反向水煤气转换(RWGS)反应会对甲醇的生产产生不利影响. 对此, Xie等[25]研究了电子激发对铜/氧化锌/氧化铝(CZA)催化剂上光热催化对CO2加氢生产甲醇的影响. 结果显示, 在紫外可见辐射(350~800 nm)下, 甲醇的产量提高了30%. 同时, 光热催化系统与单独的热催化系统相比, 可以在低50 ℃的情况下达到同样的甲醇生产能力. 到目前为止, 虽然已经对CO2加氢制甲醇进行了广泛而深入的研究, 但高压条件是工业上需要克服的一个重要障碍. He等[26]受之前的研究结果启发, 制备了CoO/Co/TiO2 Z方案型复合催化剂, 在标准大气压下就可以实现反应, 光热催化条件下获得的甲醇量比热条件高得多, 而且光和热条件的结合可以明显提高二氧化碳加氢制甲醇的活性. Wu等[27]使用Pd/ZnO作为模型催化剂, 将光辐射引入到传统的CO2加氢制甲醇的催化过程中, 旨在促进低压条件下的CO2转化和甲醇生产, 发现压力低至1.2 MPa时, 光的引入仍可显著提高了CO2转化率和甲醇产量. 除了C1产物甲醇外, 作为C2产物之一的乙醇也受到人们的关注, 但CO2具有非常稳定的性质, 有效破坏碳氧键以促进碳碳偶联的方法仍然具有挑战性, 因此, 促进碳碳偶联, 提高C2产品收率和产品选择性的催化剂亟待开发. Li等[28]采用AuCu NPs改性的超薄多孔g-C3N4纳米片用于CO2光热催化还原为乙醇, 120 ℃时乙醇的产率和选择性分别为0.89 mmol·g-1·h-1和93.1%, 分别是单一光催化的4.2倍和单一热催化的7.6倍. 这表明合适的催化体系下光热协同作用可以大大提高CO2转化为乙醇的活性, 且过程中的碳碳耦合不受甲醇生产的影响.
此外, 催化剂本身对光和热的吸收具有差异性, 使得催化剂与周围环境之间存在较大的温度梯度, 从而导致催化活性和选择性具有明显差异. Cai等[29]将工业催化剂Ni/SiO2-Al2O3分别负载于硅片、铜板和玻璃载玻片上, 探究了光热催化CO2的性能和过程中的温度变化, 结果显示, 玻璃载玻片上CO2的转化率是硅片和铜板的1.3倍和1.5倍. 通过红外相机对不同催化剂薄膜的表面温度进行监测发现, 玻璃片的平均温度为113.7 ℃, 远高于硅片上的50 ℃和铜片上的46 ℃. 所以, 光热催化剂中载体的光热转化能力以及催化剂和载体之间的热传递十分重要, 也为高效太阳能光化学能转换的反应器设计提供了新的思路.
1.2 光热催化污染物降解生物质燃料和化石燃料的燃烧导致空气中氮氧化物(NOx)的含量增加, 对环境和人类的健康造成了严重威胁[30]. 使用催化剂进行氮氧化物的选择性催化还原(SCR)已被公认为是最有效的处理方法之一. 在过去的几十年中, 还原反应所使用的催化剂得到快速发展, 但这些催化剂只有在特定的高温范围才能显示出高转化率[31-32], 因此近些年人们开始寻找在相对低的温度下实现反应的催化剂和方法. 光催化氧化NO可以在低温下进行, 且不引入有毒氨, 成本低廉, 具有良好的工业应用前景, 但收率和选择性都比较低, 同样限制了其广泛的应用, 因此, 开发光热协同氧化NO受到越来越多的关注.
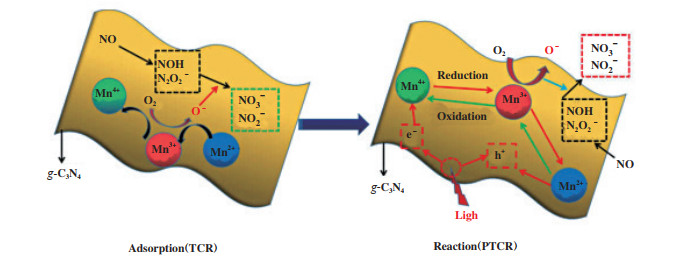
Chen等[32]通过室温沉淀法直接合成不同摩尔比的MnOx /g-C3N4催化剂, 结果显示, 在光热条件下其对NO的降解表现出极佳的性能, 通过表征发现在催化剂表面含有不同价态的MnOx. 在60 ℃下, 通过原位红外光谱研究了紫外-可见光诱导的MnOx热催化NO以及MnOx /g-C3N4光热协同催化NO的机理, 结果表明光照对MnOx热催化NO的过程几乎没有影响, 但对MnOx /g-C3N4光热协同催化NO产生积极作用并且形成重要的催化循环机制(如图 3所示). 具体过程是光生电子(e-)转移到MnOx上参与光热协同的还原循环(Mn4+→Mn3+→Mn2+), 且低价Mn离子易给出电子(e-)与光生空穴(h+)相结合而诱导逆向的循环(Mn2+→Mn3+→Mn4+), 使活性氧空位再生. 通过MnOx(Mn4+/Mn3+/Mn2+)变价而产生的活性氧(O-)可将中间产物(NOH和N2O2-)氧化为终产物(NO2-和NO3-).
|
图 3 60 ℃下, 无光条件下NO的吸附和有光条件下NO的氧化机理[32] Fig.3 Mechanism of NO adsorption without light and NO oxidation with light at 60 ℃[32] |
Hu等[33]首次选择Fe3O4NPs作为光热剂, 以提高太阳能近红外光催化氧化NO的利用率, 并试图利用这一能量来提高NO的转化率. 以P25作为碱性光催化剂代表, 制备了不同比例的P25/Fe3O4@SiO2复合催化剂. 结果显示, 在整个反应过程中P25/Fe3O4@ SiO2催化剂表面的最高温度达到了59.7 ℃, 并且在一段时间内反应温度和催化性能保持不变, 其中比例为3∶1的P25/Fe3O4@SiO2表现出最佳的催化性能, NO转化率达30%, 相比于纯P25活性提高了38.9%. Bai等[34]以氧化石墨烯为模板, 在PVA的辅助下合成了W掺杂的Fe2O3纳米片型催化剂. 结果显示, W/Fe2O3纳米薄片显示出较低的NO转化起始温度, 在250 ℃时的脱氮(88%)效率比大块W/Fe2O3(3.1%)高28.3倍. 但对于W/Fe2O3纳米片来说, 其对太阳光的吸收并不理想, 热损失也较为严重. 为此他们设计了一个由氮化铝薄膜和真空层组成的光热系统, 充分吸收阳光, 减少热能耗散. 太阳光通过AlNx薄膜而不是W/Fe2O3纳米片吸收, 保证了完全的太阳光吸收以及低热能辐射. 在一个标准太阳能的照射下, W/Fe2O3纳米片在AlNx薄膜辅助下的温度为276 ℃, 而纯W/Fe2O3纳米片的温度仅为79 ℃. 同时, 在12 h的一次太阳照射期间, 配备有AlNx膜的W/Fe2O3纳米片的N2选择性高于96%. 结果表明, 光热催化体系可以实现高效的无二次能量输入的氮氧化物的选择性催化还原, 该设计充分显示了工业化光热催化氮氧化物选择性催化还原的巨大潜力.
双酚A是一种重要的有机化学品, 在生产聚碳酸酯塑料、环氧树脂、阻燃剂和包装食品时用作中间体和原料[35]. 到目前为止, 在空气、水、土壤和食物等自然环境中, 以及在人体组织和体液中都检测到了双酚A的微量存在. 双酚A可能通过生产双酚A或含双酚A产品的工业废水排放污染地表水, 致使其广泛分布于河流、湖泊、地下水和其他天然水体中[36]. 双酚A会破坏内分泌系统的正常功能, 对生物体的生殖健康造成不利的影响. 光催化被认为是解决与水处理有关环境问题的一个有前途的选择. 具有强光催化能力的可见光响应光催化材料可以有效地利用阳光并为改善水质提供高修复效率, 其中基于银、银的氧化物和他们的复合物在可见光照射下对有机污染物的降解具有优异的光氧化性能, 而光热效应被证实是进一步提高其光催化活性有效途径之一.
2014年, Xiu等[37]通过水热光还原策略制备了3D分层Fe3O4/Ag/Bi2MoO6磁性微球复合材料, 在室温下模拟阳光照射, 以Aatrex和BPA的液相光降解速率来评价其催化性能, 结果显示Fe3O4/Ag/Bi2MoO6催化剂对Aatrex和BPA(pH=3)降解速率分别达到了98.9%和99.2%, 比原始Bi2MoO6高2.3倍和3.8倍. Fe3O4/Ag/Bi2MoO6所表现出的优异的降解性能主要可以归因于以下两个因素, 首先, 所制得的Fe3O4/Ag/Bi2MoO6磁性微球具有明显的3D分层结构, 这种分层结构能够克服传统催化剂的光利用率低造成的催化性能低的缺点; 同时, Fe3O4的宽光谱响应和添加的Ag产生的表面等离子体共振效应, 增强了光的吸收并促进了光热响应的增强, 光照样品后对应的温度变化显示出其光热效应的变化, 使得最终样品Fe3O4/Ag/Bi2MoO6的表面温度比纯Bi2MoO6的表面温度有很大提高. 以上原因均会降低光生电子-空穴的复合速率, 延长光生载流子的寿命, 从而有利于光热催化性能的提高. 以同样的思路, Zhao等[38]通过简便的两步水热法、光沉积法和原位固态还原法, 最终合成了Ag/MoS2/TiO2-x催化剂, 同样以有机污染物BPA的降解作为指标, 实验结果显示, Ag/MoS2/TiO2-x三元异质结显示出比TiO2, MoS2/TiO2和Ag/MoS2/TiO2更高的光热性能和光催化活性, BPA的降解速率高达96.7%. 同样的, Wang等[39]通过油浴、光还原和水热法制备了新型球状花状Bi5O7I/Ag/CdS串联异质结光催化剂. 独特的三维分级球花状Bi5O7I纳米片可以提供大量的表面活性位点, 有利于与有机污染物充分接触. 在制备的Bi5O7I/Ag/CdS三元异质结体系中, CdS量子点的引入显著提高了可见光的吸收, 甚至将吸收范围扩展到近红外区. 经过120 s的辐照后, 最终样品的表面温度与纯Bi5O7I和Bi5O7I/Ag相比显著升高, 中心温度可达到70.8 ℃, 这为在可见光照射下, 光催化-光热效应降解污染物提供了基础. 实验选用双酚A模拟有机污染物, 在可见光(λ > 420 nm)下测试了光催化降解性能, 三元复合材料具有最高的降解速率, 比纯Bi5O7I高8.5倍. 通过在有效光催化剂的基础上引入具有光热效应的物质, 构建多元复合催化剂, 能够大大提高污染物的光降解速率.
此外, 硝基苯酚及其衍生物具有高的毒性和结构稳定性, 同样是工业废水中最难降解的污染物之一. 美国环境保护局(USEPA)将硝基苯酚列为114种最主要的有机污染物[40]. 而通过还原4-硝基苯酚(4-NP)获得的4-氨基苯酚(4-AP), 是制药、照相和塑料工业的重要反应性中间体. 所以研究者们一直在探索使用合适的催化剂, 在温和污染少的条件下实现硝基苯酚的还原. Gu等[41]通过有机组分和金属前体的协同作用, 按比例合成强耦合的Ag/TiO2异质结, 在光热协同作用下催化4-NP还原为4-AP, 低温下(15 ℃时)在光照射下的反应速率大约是在无光照下的3倍, 甚至比在无光照下(25 ℃时)还高. 表征分析发现Ag/TiO2是一种有效的还原4-NP的催化剂, 光辐射能够促进4-NP的转化是因为Ag的局部表面等离子共振效应, 产生了热的e-和h+颗粒, 以及在光照下颗粒周围的局部加热, 从而促进了4-NP的还原. Wu等[42]同样以Ag作为活性中心, 采用简单的两步法策略制备了Ag@GQD(石墨烯量子点)复合催化剂. 在相同的底物浓度和催化剂条件下, 光照反应的速率明显高于黑暗的环境中. 在可见光照射下, 发现Ag@GQD由于催化剂表面形成热点, 可通过Ag NP的光热效应有效地提高还原速率.
然而, 对于广泛的工业应用来说, 金属光催化剂具有包括高成本、潜在的毒性、易聚集等缺点, 为此开发基于无金属材料的光热催化剂受到越来越多的关注. 到目前为止, 已经开发了多种包含金属和无金属材料的纳米光热催化剂, 可以在不同的光照射下将4-NP分子还原为4-AP分子. Liu等[43]通过简单的溶剂热处理合成了水可分散的N-GQDs碳催化剂, 考察了其在近红外光下无金属催化性能. 在相同的辐射条件下, 加入0.3 mg催化剂的溶液温度升高了近33 ℃, 而作为对比的纯水溶液温度仅升高了0.3 ℃, 通过后续计算得知, N-GQDs的光热转化效率高达33.5%. 对于4-NP的还原反应, 在没有催化剂的情况下, 即使加入过量的还原剂硼氢化钠, 4-硝基苯酚的还原也不会在环境温度下发生. 而对于同一反应混合物进行红外辐射时, 4-NP的降解速率在8 min内达到了100%. 作者指出, N-GQDs表现出高催化活性的原因之一是在近红外辐射下可以有效地将光转化为热, 这可以明显提高反应体系的局部温度. 同时, 局部温度的升高会加速近红外辐射下光激发N-GQDs产生电子的转移速率, 从而导致4-NP的反应速率更快. 这类碳催化剂所展现出的光热效应增强的光催化活性, 为非金属介导的均相催化在能源和环境中的应用提供了新的机遇.
另外, 甲苯同样是挥发有机污染化合物之一. 甲苯衍生的一系列中间体, 广泛用于生产精细化学品, 如染料、药物、杀虫剂、炸药、助剂和香料, 也用于合成材料工业. 在这些合成材料的应用和后期阶段, 甲苯不可避免地会释放到大气中, 对环境和人类的健康造成影响. 相比较于传统的催化燃烧, 通过光催化和热催化结合可以在低的温度下降解挥发性有机化合物, 并且光催化活性得到进一步增强. Tang等[44]将钙钛矿光催化剂和直接Z方案的不均匀性结合在一起, 把Ce掺杂到具有良好光热协同作用的LaMnO3催化剂中, 制备了一系列La1-x-CexMnO3催化剂, 225 ℃时, La0.75Ce0.25MnO3催化剂表现出最佳的催化性能, 气态甲苯的转化率超过90%, 二氧化碳产率也达到100%, 同时, 催化剂活性的温度范围显著降低. 高催化活性的原因是催化剂在整个太阳光区的强吸收, 以及太阳能向热能的有效转化, 这导致温度显著升高, 超过热催化反应的临界温度. Yu等[45]通过H2O2选择性还原KMnO4合成了Mn2O3, 并与Pt纳米粒子结合制备了用于光驱动光热催化甲苯氧化的Pt/Mn2O3催化剂. UV-Vis-NIR漫反射光谱显示, Pt/Mn2O3在200~2500 nm范围内表现出强的光吸收, 说明样品具有良好的光利用能力. 特别是在红外区, 强吸收导致样品具有优异的光热转换能力, 这种光-热转换的能量供应可能会驱动降解的热催化反应. 在相同温度时, 光照下的甲苯转化率和CO2产率明显高于在黑暗中直接加热, 这表明高的降解速率不仅来自光-热转化的热效应, 还来自光活化的光效应. 同时, 在相同的温度下, 全光谱照射下甲苯的转化率高于红外, 表明热量不是催化甲苯降解的唯一因素. 综上, 作者认为全光谱光驱动甲苯降解实际上可视为紫外-可见光促进红外驱动的热催化.
1.3 光热催化制氢气氢(H2)能源是保护友好的绿色燃料, 而光催化产氢被认为是最环保和节能的方法. 所以越来越多的科学家密切关注研究H2的转化, 但单一光催化面临低的产氢效率和太阳能转化率的问题, 所以人们开始尝试使用光热或光电等方式来提高太阳能的利用率.
自光催化技术被应用以来, 寻找合适的光催化剂一直是人们关注的重点. 藤岛和本田[46]首先报道了TiO2电极上光催化分解水, 自此TiO2上的多相光催化一直是催化研究的主题. TiO2由于其化学性质稳定, 寿命长, 无毒, 低成本且对可见光良好的透明性而被广泛地应用[47], 但是, 由于宽带隙(3.2 eV)的存在, TiO2仅在紫外光照射下被激活[48], 而占太阳光48%的可见光和44%的红外光的利用率较低, 另外, TiO2中的光生电子和空穴易发生快速重组, 这会大大降低催化反应的效率, 限制了其在光催化领域的应用[49]. 为了抑制电子空穴的重组, Pt被广泛用作光催化生产H2的助催化剂, 因为它在苛刻的操作条件下也具有很高的活性和稳定性. 早在1998年, Kennedy等[50]就已经研究了反应条件对于Pt/TiO2上乙醇氧化的影响. 结果发现, Pt/TiO2催化剂表现出明显的光热协同效应, 作者将此协同效应归因于Pt位点发生的热反应和TiO2位点发生的光反应的耦合作用, 后来, 越来越多的人开始关注于Pt/TiO2催化剂上热作用的影响, 以及由此产生的光热协同效应. Liu等[51]通过制得的光催化剂Pt/TiO2在UV-Vis, UV-Vis-IR和IR的条件下催化水-甲醇溶液产氢, 探究红外光的光热效应对溶液产氢速率的影响. 结果显示, 在水-甲醇溶液中, 在UV-Vis-IR全光谱照射后, 催化产氢达到27.4 mmol·g-1, 是相同时间内UV-Vis光照射下的2倍. 然而, 在红外光照射下, 没有氢气产生, 所以红外光不能激发Pt/TiO2. 而Song等[52]使用同样的催化剂研究了4种典型的有机牺牲试剂, 即甲醇(MeOH)、三乙醇胺(TEOA)、甲酸(HCOOH)和葡萄糖在Pt/TiO2光催化剂上的光热制氢. 结果甲酸表现出了最佳的活性, 在光热催化反应时, 90 ℃下的氢产率比在光或热单一条件下高约8.1倍和4.2倍, 结果表明, Pt/TiO2纳米颗粒可以有效地耦合光能和热能, 从而更有效地驱动氢的产生. 通常, 金属纳米粒子的光热效应是通过将光子能量转换为热能或将光和热效应耦合来产生的, Pt/TiO2对产氢所表现出的优越性能主要有以下几个方面: (1)由光热效应引起的产氢增加部分归因于非等离子体Pt金属纳米颗粒的存在, 这种金属纳米粒子可以有效地利用光能和热能, 从而进行出色的光热制氢.(2)在光热条件下的优异催化性能也应归因于TiO2纳米颗粒的存在, TiO2的光生电子被认为转移到Pt上, 对于光热制氢的高活性至关重要.(3)有效的光热性能也可能与中间体在催化剂表面迁移速率有关, 存在热能时中间体的迁移要比不存在热能时更快.
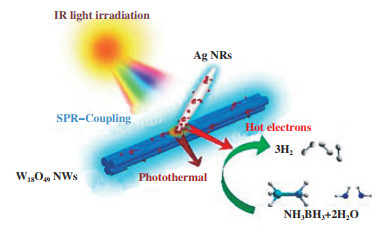
除了Pt以外的其他贵金属同样能够起到光热耦合作用. Liu等[53]将Ag纳米环(NRs)组装到W18O49纳米线(NWs)上, 制备一种新型的等离子体耦合异质结构薄膜, 并使其在掺杂F的SnO2玻璃表面生长. 紫外-可见-近红外吸收光谱显示, 与纯Ag和W18O49薄膜相比, AgNRs和W18O49 NWs在其异质结构膜中表现出强的等离激元耦合效应, 模拟太阳光照射的情况下催化NH3BH3水解产生氢气(图 4). 结果显示将Ag纳米结构组装到W18O49 NWs膜上之后, 所获得的Ag/W18O49异质结构膜的催化活性显著增强, H2析出速率(0.18 μmol·min-1)超过纯Ag纳米结构膜或W18O49 NWs膜(0.02 μmol·min-1)几乎一个数量级. 在反应溶液中引入Ag/W18O49异质结构薄膜后, 仅照射5 min, 反应温度可达55 ℃, 该催化温度分别比由纯W18O49 NWs(45 ℃)和Ag NRs膜(28 ℃)获得的相应值高1.22和1.96倍. 在表面等离子体共振耦合激发下的局部温度可以克服水解反应中的小能量障碍, 从而加速H2释放.
|
图 4 氨硼烷的光/热催化在Ag/W18O49异质结构上产生H2的示意图[53] Fig.4 Schematic diagram of the photo/thermal catalysis of ammonia borane for H2 evolution over the Ag/W18O49 heterostructure |
除了贵金属之外, 同样具有明显整合光热作用的非贵金属因为其低的成本同样得到了广泛的应用. Song等[54]设计了颗粒尺寸小于10 nm的Cu负载的Cu/TiO2棒状纳米复合材料, 系统研究了可见-近红外光下等离子体诱导的光热效应的作用. 紫外可见光谱显示, Cu的整合并没有改变TiO2在紫外光区的吸收, 但却扩展了可见光和近红外光的吸收区间, 使太阳能的全光谱利用成为可能. 在全光谱下, Cu/TiO2的产氢速率几乎是紫外-可见光下的2倍. 在红外热像仪下, Cu/TiO2与TiO2的表面温差可达到12.5 ℃, 证明了Cu的光热效应. Cu纳米粒子在近红外光照射下产生的LSPR效应可以引发光热效应, 从而提高TiO2-Cu界面的温度, 进而提高反应体系的温度, 加速了电子的转移速率, 降低载流子复合的几率, 且Cu的光热效应随着近红外功率的增强而增强, 产氢性能也随之增强. 另一方面, 由光热效应所引起的局部温度的升高能够降低光催化反应的表观活化能, 提高了反应速率. He等[55]采用简便的一步水热法制备石墨烯修饰的WO3/TiO2/rGO(WTG)S型异质结光催化剂. 在Xe光灯照射下, WTG复合材料上H2的析出速率提高到245.8 μmol·g-1·h-1, 大约是WT(WO3/TiO2)的2.3倍, 分析发现利用石墨烯的强光吸收能力和导热性的特点, 可以把石墨烯作为光催化分解水产氢有效的共催化剂, 同时也说明了光热效应在光催化产氢中所起到的积极作用.
为了整合光热和催化的双重功能, 核-壳异质结构应该是一个合理的模型[56]. Sun等[57]采用氢化法制备的核壳TiO2纳米粒子, 该纳米粒子在近红外区具有很强的光吸收和显著的光热转换能力以及稳定性, 其光热转换效率高达55.2%, 是完全氢化非晶TiO2的204%, 在生物和化工方面已经实现了应用. Nikitenko等[58]同样在不存在任何贵金属的情况下以简单且环保的方法合成Ti@TiO2核壳纳米粒子. 在MeOH-H2O溶液中, Vis/NIR光和热的共同作用下, Ti@TiO2纳米颗粒在H2的形成中表现出最强的催化活性. 与原始TiO2相比, Ti@TiO2纳米颗粒将光响应从UV扩展到NIR光区域, 其作为光催化剂产生H2的热效应是由中间体的迁移决定的, 而不是由吸附在催化剂表面的反应物分子的振动激发决定的, 而光催化作用最可能是由于Ti核的电子激发通过带间电子跃迁引起的. Gao等[59]采用SiO2/Ag@TiO2核-壳结构进行光热催化研究, 以模拟海水的产氢探究其催化性能. 结果显示, 相比于SiO2和SiO2@TiO2, SiO2/Ag@TiO2显示出了更强的催化性能, 并在真实的海水中达到了相似的效果. 提出的光热效应机理是: TiO2多孔壳能够吸收太阳光谱的紫外线部分, 而SiO2/Ag吸收可见光和近红外光, SiO2介质中的银金属颗粒会散射传播的光, 以提高光吸收能力. 故SiO2/Ag@TiO2核-壳结构方案能够实现光催化氢产生的广谱利用, 其中高能光子用于光催化电子-空穴对的产生, 而低能光子用于有利的光热效应. 这些模型充分地展示了在自然阳光下可持续光热驱动海水催化的可行性, 同时实现了在无额外资金投入和二次能源输入的情况下提高能源的利用率和氢气的产生速率.
此外, 石墨氮化碳(g-C3N4)是一种具有合适带隙能量的半导体光催化剂, 但是, 由于其表面氧化还原反应产生的光生电荷的快速复合, 它们在光催化制氢中的活性通常不令人满意, 为此, 通常与助催化材料(通常以贵金属纳米颗粒的形式)结合, 或通过构建核-壳结构等方式以促进表面质量和能量的转移和交换来提高催化性能. Lu等[60]以一种简单的方法合成了富含硫空位的NiS和石墨氮化碳(g-C3N4)组成的NiS@g-C3N4复合光催化剂. 该催化剂在近红外区域表现出强烈的吸收, 说明了其良好的光热效应. 模拟太阳光照射下, NiS@g-C3N4具有良好的光催化H2生成速率, 为31.3 mmol·g-1·h-1, 并且经历5次循环试验H2的生成速率保持恒定, 研究显示, S空位与光热效应之间的协同作用在提高H2的生产性能中起着重要作用. 此外他们还制作了一系列其他基于g-C3N4的光催化剂, 与NiS@g-C3N4的H2生产速率比较如表 1所示. Guo等[61]通过种子介导法合成了核壳结构的铜镍纳米片, 然后通过水热处理将这些纳米片紧密附着在g-C3N4光催化剂的表面, 形成Cu@Ni/g-C3N4复合催化剂. 此复合催化剂固有带隙激发了长波太阳能的充分利用, 能够显著诱导光热转化, 有利于光催化过程. Cu@Ni/g-C3N4显示出最高催化活性, H2产率达到55 μmol·g-1·h-1, 分别是Cu/g-C3N4和g-C3N4的5倍和110倍, 表征发现光热效应在催化活性中起主导作用, 同时Ni助催化剂表面的光热效应可以增加反应表面的能量和质量转移和交换, 最终导致催化活性的增加. 因此通过整合金属异质纳米粒子, 可以实现光电效应和光热效应的有效耦合, 为实现全光谱太阳能转换提供了一种有效的途径.
| 表 1 其他基于g-C3N4的光催化剂和NiS @g-C3N4的H2生产率的比较[60] Table 1 Comparison of H2 production rate of other g-C3N4 based photocatalyst and NiS@g-C3N4[60] |
除了采取结构改进, 引入杂原子(金属或非金属)以调节其电子能带结构的方法外, 与其他组分(金属氧化物、单体、碳基材料等)偶联同样能够有效增强其光生电荷分离, 提高其催化性能, 其中与碳基材料相结合表现出优异的导电性和非凡的化学稳定性, 以及对g-C3N4的高亲和力. Zhang等[62]采用两步法合成了一种新型CF(碳纤维)/ g-C3N4复合材料, 对所得复合材料光催化分解水进行了系统的研究. CF/g-C3N4复合材料的带隙变窄, 有助于其光催化能力. CF在可见光下显示出光催化活性, H2产率为236 μmol·g-1·h-1, 而与g-C3N4复合后, 复合材料的H2生产率提高到537 μmol·g-1·h-1. 作者认为, CF与g-C3N4的结合可以改善后者的光催化性能的一部分原因是光热效应, CF可以在可见光照射后提高光催化反应体系的温度, 这也可能有助于提高CF/g-C3N4复合材料光催化H2的产生.
1.4 光热催化费托合成反应费-托合成(FTS)或一氧化碳加氢是将非石油碳资源(例如天然气, 煤炭和生物质)转化为燃料(例如汽油和柴油)的关键中间步骤. 而传统的热式FTS需要大量的能量输入(250 ~400 ℃, 2~5 MPa), 为了能在较温和的条件下实现该反应, 科学家们引入太阳光, 以光热协同驱动反应, 以降低较高的反应温度和压力, 因此光热催化被认为是利用丰富太阳能将合成气转化为有价值化学品的绿色和可持续的方法[63]. 在FTS反应中, 最常用的催化剂是ⅧB族过渡金属, 尤其是铁、钴、镍和钌. 这些催化剂的一氧化碳加氢活性和产物选择性不同, 其中几种金属经常一起使用(以合金形式), 可以获得高的一氧化碳转化率或提高对特定产物或一组产物的选择性.
Wang等[64]采用初期湿润浸渍法制备了不同Co负载量的TiO2纳米管(TNT)催化剂, 通过构建这样一个热活性成分与光敏载体结合而成的光热催化体系, 研究了其用于光热催化FTS反应过程中的作用以及紫外线(UV)照明在传统的热化学FTS反应中的作用. 结果表明, 紫外线的引入显着提高了CO转化率, 对于20%Co/TNT, CO转化率从9.2%提高到64.0%, 另外, UV照射引起了石蜡选择性的增加. 紫外线辐射可以大大提高Co/TNT对FTS的内在催化能力, 增强的活性主要归因于照明的存在下, 紫外线确实会促进CO在Co位点的吸附, 从而促进了CO的解离. 同时, 紫外线照射下, 随着温度的升高, CO的转化率成线性增加, 但对于较低的反应温度, 即使引入紫外线照射, 反应也不会发生, 说明FTS反应需要在一定的温度下才能获得动力学来克服活化障碍. 同时, 220 ℃、UV辐射下的CO转化率与无光照、298 ℃下的转化率相当. 因此, 与热催化过程相比, 光热催化过程是一种节能过程. 由于TiO2在费托反应中所表现出的优异性能, 所以Yu等[65]研究了以介孔TiO2为催化剂载体的催化行为. 在光热驱动费托合成中, 探究了不同Fe负载量下的费托催化活性. 结果不同浓度下各种低碳烯烃的选择性与Fe的含量呈现一定的规律性变化, CO转化率为85%, 对应样品的Fe∶Ti原子比为20%. TiO2在两种体系中所起到的作用也不相同, 在热催化过程中, TiO2只是起到了分散和稳定活性金属物质的载体作用; 而在光热催化过程中, TiO2不仅是一种载体, 而且是一种有效的光助催化剂. 除了单一TiO2以外, TiO2的核壳结构也显示出良好的高光热性能, 因此通过TiO2合理的结构设计, 使核壳产品成为通过控制结晶性质来改善光热性能的理想催化剂, 实现在能源等方面的应用.
通过在不同条件下还原层状双氢氧化物(LDH)纳米片而制得的光热催化剂在费托合成反应中被广泛应用, 并且表现出良好的选择性和稳定性. Li等[66]通过在300 ~700 ℃下H2还原ZnCoAl层状双氢氧化物纳米片, 成功制备了具有不同化学组成的一系列新型Co基光热催化剂, 并且在紫外可见光辐射下催化费-托合成反应. 结果显示, 在450 ℃的温度下制备的光热催化剂具有出色的CO加氢性能, 在CO转化率为15.4%时, 烯烃(C2-4=)的选择性为36.0%, 烯烃/石蜡比为6.1. 对于其机理的研究结果显示, 负载金属Co纳米颗粒和Co3O4纳米颗粒(即Co/Co3O4异质结)的共存是在CO氢化过程中促进烯烃形成并超过氢化成烷烃的基本要求. 所以金属Co和Co3O4的演化是对实现CO加氢过程中的光热效应和对轻烯烃的高选择性很重要的两相. 当还原温度为450 ℃时, Co-450与金属Co、Co3O4和ZnO的缔合非常紧密, Co纳米颗粒分布良好. 最后通过使用与催化剂床表面紧密接触的热电偶来监测催化剂床温度的方法证实了基于Co-450的FTO工艺是由于光热效应引起的. 与含Co的催化剂相比, Fe基催化剂由于其独特的电子结构而提供了更加中等的中间键合能, 使得Fe基光催化剂体系可能会为实现烯烃的高选择性提供新途径. 后来他们[67]以相同的思路在不同温度下, 将ZnFeAl-LDH纳米片前体进行氢还原合成一系列Fe-x光催化剂. 结果显示, Fe-500光催化剂在紫外可见激发下表现出出色的光催化FT反应性能, 对烯烃的选择性非常高, 对CO2的选择性很低. 在还原此类层状双氢氧化物时所制得的衍生催化剂中, Zn氧化物是紫外线响应半导体, 而Al2O3是热稳定的载体, 有利于避免反应过程中不良的催化剂烧结和聚集. 在适宜的温度下, 催化剂中会含有适量的Fe、Co或Ni, 可作为CO加氢的活性位点, 同时存在大量的这类金属和其氧化物界面, 从而提供具有中等中间体的异质结构的结合能, 促进烯烃的形成并抑制CO2的释放.
由于Fe基催化剂具有低成本和高操作活性的优点, 在高反应温度下对低级烯烃具有高选择性, 所以在FTS中具有不可或缺的地位. Li等[68]制备了一系列负载于不同载体(疏水SiO2、亲水SiO2、α-Al2O3、γ-Al2O3和α, γ-Al2O3)上的Fe5C2催化剂, 比较它们在光热FTS中的催化活性. 在所有的催化剂中, Fe5C2/α-Al2O3表现出更好的催化活性, 一氧化碳转化率为52.5%, 低碳烯烃选择性为50.3%. 同时, Fe5C2/α-Al2O3表现出更高的光-热转化效率. 在光照条件下, Fe5C2/α-Al2O3催化剂在3 min内迅速升温至316 ℃, 30 min内升温至340 ℃, 远高于其他载体的催化剂. 随着反应温度的升高, 分子运动变快, 产生的有效碰撞增加, 导致一氧化碳的转化率升高. Gao等[69]通过实验揭示了氧修饰Fe5C2具有高催化活性的原因, Fe5C2催化剂具有高的太阳能利用率, 可进行光诱导的热转化, 而不会出现明显的光诱导电荷(电/空穴). 在光辐射下, Fe5C2的局部温度显著升高, 可提供能量来克服反应障碍并启动反应过程. 光驱动FTO是一种可持续的途径, 并生产有价值的燃料和化学品, 此外, 与热催化反应相比, 光的存在能够明显改变反应的选择性.
在FTS反应过程中, 铁基催化剂对轻质烯烃表现出良好的选择性. 然而, 铁基催化剂上的FTS通常需要高于300 ℃的温度, 这可能导致焦炭形成和活性位点的烧结, 从而导致催化剂失活. 然而, 镍基催化剂能够很好克服上述缺点, 并且由于低成本的优点可以实现工业化应用. 但是, 在反应过程中目标产物是难以控制的(除非CH4是目标产品). 为了在镍基催化剂上获得更有价值的轻烯烃, 研究重点主要放在改变活性相的电子结构以降低其氢化能力等策略上. Wang等[70]通过在250 ~600 ℃之间的温度下氢气还原NiMn混合金属氧化物制备了一系列的Ni0/MnO催化剂, 探究镍基催化剂对轻质烯烃实现高选择性的条件. 在紫外-可见光照射下, 所有的催化剂均表现出对光的强吸收, 其中Ni-500的光热转化能力最强, 在15 min内从24 ℃快速升高到210 ℃. 在反应过程中, Ni-500催化剂显示出最佳的光热性能, CO转化率达到14.9%, 对轻烯烃的高选择性为33%, 而对CO2的选择性仅为1.0%. 最后, 作者通过对比实验确定Ni-500催化剂优异的催化性能是光热催化过程而不是光催化过程, 使用Ni基催化剂能够在一定程度上解决低成本生产轻质烯烃的FTS催化剂的问题.
Mn常以氧化态的形式作为促进剂广泛应用于费托合成(FTS). Li等[71]采用一步湿化学法合成了负载CoMn合金的MnO催化剂, 研究CoMn合金对FTS催化性能的影响. 所制得的ConMnx /(MnO)m-x催化剂表现出对太阳能的高利用效率, 进而显示出优异的光热催化性能. 其中Co1Mnx /(MnO)2-x催化剂显示出最佳的催化性能, 轻质烯烃(27.0%, o/p=3.2)为主要产品. 同时, 一氧化碳转化率为13.9%, CO2选择性仅为22.6%. 通常锰合金的形成改变了钴的电子结构, 从而影响了合成气转化为低碳烯烃的光热催化性能. 这种内置的电子促进剂比外部的MnO更有效, 但其潜在机制仍在进一步研究中. 但是可以调节活性组分的微结构和合理的支撑, 实现高效的太阳能转化为化学能.
2 总结与展望光热催化是协同效应, 而不是简单的光催化和热催化的叠加, 被认为是一种实现环境保护和能源综合利用的新途径. 对于不同的催化反应和体系, 光热协同效应通常会产生意想不到的效果. 光热催化的性能通常高于光催化或热催化, 其潜在的机理不是十分清楚, 需要进一步探索, 但现在已经在许多方面得到了应用.
光热催化是一种实现高效催化效果的新方法, 具有十分广阔的前景. 将来研究方向和重点可能如下: 1)需要对催化剂的材料和结构进行优化, 以实现更高的转化效率和产物的选择性. 2)考虑与其他能量转化相结合, 采用简单廉价的方法来改变催化剂的光吸收率. 3)希望对反应机理有更深入的了解, 尤其是光热协同效应. 相信在不久的将来, 随着对体系的深入认识, 光热催化将会成为催化领域的一个新热点.
| [1] |
Ediger V S. An integrated review and analysis of multi-energy transition from fossil fuels to renewables[J]. Energy procedia, 2019, 156: 2–6.
DOI:10.1016/j.egypro.2018.11.073 |
| [2] |
a. Li Q, Lu G. Significant effect of pressureon the H2 releasing from photothermal-catalytic water steam splitting over TiSi2 and Pt/TiO2[J]. Catal Lett, 2008, 125(3): 376-379. b. Ge Jian-hua(葛建华), Zhang Zhi-ping(章志平), Jiang Dao-chuan(江道传), et al. Ni3N decorated BiVO4 photoanodes for solar-driven water splitting(Ni3N修饰BiVO4用于光电催化分解水的研究)[J]. J Mol Catal(China)(分子催化), 2021, 35(3): 235-242. c. Feng Chen chen(冯晨晨), Zhang Ya-jun(张亚军), Bi Ying-pu(毕迎普). Research progress and challenges of α-Fe2O3 photoanode for photoelectrochemical water splitting(α-Fe2O3光阳极光电化学分解水的研究进展与挑战)[J]. J Mol Catal(China)(分子催化), 2020, 34(3): 227-241. d. Wang Meng(王蒙), Ma Jian-tai(马建泰), Lu Gongxuan(吕功煊). The inhibition of hydrogen and oxygen recombination reverse reaction on cocatalyst surface in photocatalytic overall water splitting for hydrogen evolution(光催化全分解水制氢中助催化剂表面氢氧复合反应的抑制)[J]. J Mol Catal(China)(分子催化), 2019, 33(5): 461-485. |
| [3] |
York R, Bell S E. Energy transitions or additions? Why a transition from fossil fuels requires more than the growth ofrenewable energy[J]. Energy Res Soc Sci, 2019, 51: 40–43.
DOI:10.1016/j.erss.2019.01.008 |
| [4] |
Xiao J D, Jiang H L. Metal-organic frameworks for photocatalysis and photothermal catalysis[J]. Accounts Chem Res, 2018, 52(2): 356–366.
|
| [5] |
Zhu L, Gao M, Peh C K N, et al. Solar-driven photothermal nanostructured materials designs and prerequisites for evaporation and catalysis applications[J]. Mater Horizons, 2018, 5(3): 323–343.
DOI:10.1039/C7MH01064H |
| [6] |
Lee K M, Lai C W, Ngai K S, et al. Recent developments of zinc oxide based photocatalyst in water treatment technology: A review[J]. Water Res, 2016, 88: 428–448.
DOI:10.1016/j.watres.2015.09.045 |
| [7] |
Ni M, Leung M K H, Leung D Y C, et al. A review and recent developments in photocatalytic water-splitting using TiO2 for hydrogen production[J]. Renew Sust Energ Rev, 2007, 11(3): 401–425.
DOI:10.1016/j.rser.2005.01.009 |
| [8] |
Zhu J, Zäch M. Nanostructured materials for photocatalytic hydrogen production[J]. Curr Opin Colloid Interface Sci, 2009, 14(4): 260–269.
DOI:10.1016/j.cocis.2009.05.003 |
| [9] |
Shiraishi Y, Hirai T. Selective organic transformations on titanium oxide-based photocatalysts[J]. J Photochem Photobiol C-Photochem, 2008, 9(4): 157–170.
DOI:10.1016/j.jphotochemrev.2008.05.001 |
| [10] |
Low J, Cheng B, Yu J. Surface modification and enhanced photocatalytic CO2 reduction performance of TiO2: A review[J]. Appl Surf Sci, 2017, 392: 658–686.
DOI:10.1016/j.apsusc.2016.09.093 |
| [11] |
Chatterjee D, Dasgupta S. Visible light induced photocatalytic degradation of organic pollutants[J]. J Photochem Photobiol C-Photochem Rev, 2005, 6(2/3): 186–205.
|
| [12] |
Tang S, Sun J, Hong H, et al. Solar fuel from photo-thermal catalytic reactions with spectrum-selectivity: A review[J]. Front Energy, 2017, 11(4): 437–451.
DOI:10.1007/s11708-017-0509-z |
| [13] |
Wang L, Liu X, Dang Y, et al. Enhanced solar induced photo-thermal synergistic catalytic CO2 conversion by photothermal material decorated TiO2[J]. Solid State Sci, 2019, 89: 67–73.
DOI:10.1016/j.solidstatesciences.2018.12.018 |
| [14] |
Li K, Peng B, Peng T. Recent advances in heterogeneous photocatalytic CO2 conversion to solar fuels[J]. ACS Catal, 2016, 6(11): 7485–7527.
DOI:10.1021/acscatal.6b02089 |
| [15] |
Zhang Z, Gao Z, Liu H, et al. High photo thermally active Fe2O3 film for CO2 photoreduction with H2O driven by solar light[J]. ACS Appl Energ Mater, 2019, 2(12): 8376–8380.
DOI:10.1021/acsaem.9b01825 |
| [16] |
Lu B, Quan F, Sun Z, et al. Photothermal reverse-watergas-shift over Au/CeO2 with high yield and selectivity in CO2 conversion[J]. Catal Commun, 2019, 129: 105724.
DOI:10.1016/j.catcom.2019.105724 |
| [17] |
Zhao Z, Doronkin D E, Ye Y, et al. Visible light-enhanced photothermal CO2 hydrogenation over Pt/Al2O3 catalyst[J]. Chin J Catal, 2020, 41(2): 286–293.
DOI:10.1016/S1872-2067(19)63445-5 |
| [18] |
Jia J, O'Brien P G, He L, et al. Visible and near-infrared photothermal catalyzed hydrogenation of gaseous CO2 over nanostructured Pd@Nb2O5[J]. Adv Sci, 2016, 3(10): 160–189.
|
| [19] |
Ghuman K K, Wood T E, Hoch L B, et al. Illuminating CO2 reduction on frustrated Lewis pair surfaces: Investigating the role of surface hydroxides and oxygen vacancies on nanocrystalline In2O3-x(OH)y[J]. Phys Chem Chem Phys, 2015, 17(22): 14623–14635.
DOI:10.1039/C5CP02613J |
| [20] |
Hoch L B, O'Brien P G, Jelle A, et al. Nanostructured indium oxide coated silicon nanowire arrays: A hybrid photothermal/photochemical approach to solar fuels[J]. ACS Nano, 2016, 10(9): 9017–9025.
DOI:10.1021/acsnano.6b05416 |
| [21] |
Xu M, Hu X, Wang S, et al. Photothermal effect promoting CO2 conversion over composite photocatalyst with high graphene content[J]. J Catal, 2019, 377: 652–661.
DOI:10.1016/j.jcat.2019.08.010 |
| [22] |
Wang L, Wang Y, Cheng Y, et al. Hydrogen-treated mesoporous WO3 as a reducing agent of CO2 to fuels (CH4 and CH3OH) with enhanced photothermal catalytic performance[J]. J Mater Chem A, 2016, 4(14): 5314–5322.
DOI:10.1039/C5TA10180H |
| [23] |
Meng X, Wang T, Liu L Q, et al. Photothermal conversion of CO2 into CH4 with H2 over Group Ⅷ nanocatalysts: An alternative approach for solar fuel production[J]. Angew Chem Int Ed, 2014, 53(43): 11478–11482.
DOI:10.1002/anie.201404953 |
| [24] |
Chen X, Li Q, Zhang M, et al. MOF-Templated preparation of highly dispersed Co/Al2O3 composite as the photothermal catalyst with high solar-to-fuel efficiency for CO2 methanation[J]. ACS Appl Mater Interfaces, 2020, 12(35): 39304–39317.
DOI:10.1021/acsami.0c11576 |
| [25] |
Xie B, Wong R J, Tan T H, et al. Synergistic ultraviolet and visible light photo-activation enables intensified low-temperature methanol synthesis over copper/zinc oxide/alumina[J]. Nat Commu, 2020, 11(1): 1–11.
DOI:10.1038/s41467-019-13993-7 |
| [26] |
He Z H, Jiang C S, Wang K, et al. Photothermal CO2 hydrogenation to methanol over a CoO/Co/TiO2 catalyst in aqueous media under atmospheric pressure[J]. Catal Today, 2020, 356: 579–588.
DOI:10.1016/j.cattod.2020.01.007 |
| [27] |
Wu D, Deng K, Hu B, et al. Plasmon-assisted photothermal catalysis of low-pressure CO2 hydrogenation to methanol over Pd/ZnO catalyst[J]. ChemCatChem, 2019, 11(6): 1598–1601.
DOI:10.1002/cctc.201802081 |
| [28] |
Li P, Liu L, An W, et al. Ultrathin porous g-C3N4 nanosheets modified with AuCu alloy nanoparticles and C-C coupling photothermal catalyticreduction of CO to ethanol[J]. Appl Catal B-Environ, 2020, 266: 118618.
DOI:10.1016/j.apcatb.2020.118618 |
| [29] |
Cai M J, Li C R, He L. Enhancing photothermal CO2 catalysis by thermal insulating substrates[J]. Rare Metals, 2020, 39: 881–886.
DOI:10.1007/s12598-020-01431-3 |
| [30] |
Chen L, Li J, Ge M, et al. Enhanced activity of tungsten modified CeO2/TiO2 for selective catalytic reduction of NOx with ammonia[J]. Catal Today, 2010, 153(3/4): 77–83.
|
| [31] |
Kang M, Park E D, Kim J M, et al. Manganese oxide catalysts for NOx reduction with NH3 at low temperatures[J]. Appl Catal A-Ge, 2007, 327(2): 261–269.
DOI:10.1016/j.apcata.2007.05.024 |
| [32] |
Chen P, Dong F, Ran M, et al. Synergistic photo-thermal catalytic NO purification of MnOx/g-C3N4: Enhanced performance and reaction mechanism[J]. Chin J Catal, 2018, 39(4): 619–629.
DOI:10.1016/S1872-2067(18)63029-3 |
| [33] |
Hu J, Wang H, Dong F, et al. A new strategy for utilization of NIR from solar energy-Promotion effect generated from photothermal effect of Fe3O4@SiO2 for photocatalytic oxidation of NO[J]. Appl Catal B-Environ, 2017, 204: 584–592.
DOI:10.1016/j.apcatb.2016.12.009 |
| [34] |
Bai X, Yuan D, Xu Y, et al. Realizing efficient natural sunlight-driven photothermal selective catalytic reduction of nitrogen oxides by AlNx assisted W doped Fe2O3 nanosheets[J]. Sol Energy Mater Sol Cells, 2020, 208: 110395.
DOI:10.1016/j.solmat.2020.110395 |
| [35] |
Jia C, Wang Y, Zhang C, et al. Photocatalytic degradation of bisphenol A in aqueous suspensions of titanium dioxide[J]. Environ Eng Sci, 2012, 29(7): 630–637.
DOI:10.1089/ees.2011.0132 |
| [36] |
Liu B, Qiao M, Wang Y, et al. Persulfate enhanced photocatalytic degradation of bisphenol A by g-C3N4 nanosheets under visible light irradiation[J]. Chemosphere, 2017, 189: 115–122.
DOI:10.1016/j.chemosphere.2017.08.169 |
| [37] |
Xiu Z, Cao Y, Xing Z, et al. Wide spectral response photothermal catalysis-fenton coupling systems with 3D hierarchical Fe3O4/Ag/Bi2MoO6 ternary hetero-superstructural magnetic microspheres for efficient high-toxic organic pollutants removal[J]. J Colloid Interface Sci, 2019, 533: 24–33.
DOI:10.1016/j.jcis.2018.08.047 |
| [38] |
Zhao T, Xing Z, Xiu Z, et al. Synergistic effect of surface plasmon resonance, Ti3+ and oxygen vacancy defects on Ag/MoS2/TiO2-x ternary heterojunctions with enhancing photothermal catalysis for low-temperature wastewater degradation[J]. J Hazard Mater, 2019, 364: 117–124.
DOI:10.1016/j.jhazmat.2018.09.097 |
| [39] |
Wang K, Xing Z, Du M, et al. Plasmon Ag and CdS quantum dot co-decorated 3D hierarchical ball-flower-like Bi5O7I nanosheets as tandem heterojunctions for enhanced photothermal-photocatalytic performance[J]. Catal Sci Technol, 2019, 9(23): 6714–6722.
DOI:10.1039/C9CY01945F |
| [40] |
Feng J, Su L, Ma Y, et al. CuFe2O4 magnetic nanoparticles: A simple and efficient catalyst for the reduction of nitrophenol[J]. Chem Eng J, 2013, 221: 16–24.
DOI:10.1016/j.cej.2013.02.009 |
| [41] |
Gu Y, Jiao Y, Zhou X, et al. Strongly coupled Ag/TiO2 heterojunctions for effective and stable photothermal catalytic reduction of 4-nitrophenol[J]. Nano Res, 2018, 11(1): 126–141.
DOI:10.1007/s12274-017-1612-5 |
| [42] |
Wu C, Yuan Y, He Q, et al. Two-step synthesis of Ag@GQD hybrid with enhanced photothermal effect and catalytic performance[J]. Nanotechnology, 2016, 27(48): 48LT02..
DOI:10.1088/0957-4484/27/48/48LT02 |
| [43] |
Liu H, Wang H, Qian Y, et al. Nitrogen-Doped graphene quantum dots as metal-free photocatalysts for near-infrared enhanced reduction of 4-nitrophenol[J]. ACS Appl Nano Mater, 2019, 2(11): 7043–7050.
DOI:10.1021/acsanm.9b01549 |
| [44] |
Tang Y, Tao Y, Zhou T, et al. Direct Z-scheme La1-xCexMnO3 catalyst for photothermal degradation of toluene[J]. Environ Sci Pollut Res, 2019, 26(36): 36832–36844.
DOI:10.1007/s11356-019-06856-7 |
| [45] |
Yu E, Li J, Chen J, et al. Enhanced photothermal catalytic degradation of toluene by loading Pt nanoparticles on manganese oxide: Photoactivation of lattice oxygen[J]. J Hazard Mater, 2020, 388: 121800.
DOI:10.1016/j.jhazmat.2019.121800 |
| [46] |
Fujishima A, Honda K. Electrochemical photolysis of water at a semiconductor electrode[J]. Nature, 1972, 238(5358): 37–38.
DOI:10.1038/238037a0 |
| [47] |
Nakata K, Fujishima A. TiO2 photocatalysis: Design and applications[J]. J Photochem Photobiol C-Photochem Rev, 2012, 13(3): 169–189.
DOI:10.1016/j.jphotochemrev.2012.06.001 |
| [48] |
Fajrina N, Tahir M. 2D-montmorillonite-dispersed g-C3N4/TiO2 2D/0Dnanocomposite for enhanced photo-induced H2 evolution from glycerol-water mixture[J]. Appl Surf Sci, 2019, 471: 1053–1064.
DOI:10.1016/j.apsusc.2018.12.076 |
| [49] |
Sun W, Zhang S, Liu Z, et al. Studies on the enhanced photocatalytic hydrogen evolution over Pt/PEG-modified TiO2 photocatalysts[J]. Int J Hydrog Energy, 2008, 33(4): 1112–1117.
DOI:10.1016/j.ijhydene.2007.12.059 |
| [50] |
Kennedy III J C, Datye A K. Photothermal heterogeneous oxidation of ethanol over Pt/TiO2[J]. J Catal, 1998, 179(2): 375–389.
DOI:10.1006/jcat.1998.2242 |
| [51] |
Liu X, Ye L, Ma Z, et al. Photothermal effect of infrared light to enhance solar catalytic hydrogen generation[J]. Catal Commun, 2017, 102: 13–16.
DOI:10.1016/j.catcom.2017.08.014 |
| [52] |
Song R, Luo B, Jing D. Efficient photothermal catalytic hydrogen production over nonplasmonic Pt metal supported on TiO2[C]//Solar Hydrogen and Nanotechnology XI. International Society for Optics and Photonics. 2016, 9935: 99350C.
|
| [53] |
Liu Y, Zhang Z, Fang Y, et al. IR-Driven strong plasmonic-coupling on Ag nanorices/W18O49 nanowires heterostructures for photo/thermal synergistic enhancement of H2 evolution from ammonia borane[J]. Appl Catal B-Environ, 2019, 252: 164–173.
DOI:10.1016/j.apcatb.2019.04.035 |
| [54] |
Song R, Liu M, Luo B, et al. Plasmon-induced photothermal effect of sub-10-nm Cu nanoparticles enables boosted full-spectrum solar H2 production[J]. AICHE J, 2020, 66(11): e17008.
|
| [55] |
He F, Meng A, Cheng B, et al. Enhanced photocatalytic H2-production activity of WO3/TiO2 step-scheme heterojunction by graphene modification[J]. Chin J Catal, 2020, 41(1): 9–20.
DOI:10.1016/S1872-2067(19)63382-6 |
| [56] |
Wang F, Huang Y, Chai Z, et al. Photothermal-enhanced catalysis in core-shell plasmonic hierarchical Cu7S4 microsphere@zeolitic imidazole framework-8[J]. Chem Sci, 2016, 7(12): 6887–6893.
DOI:10.1039/C6SC03239G |
| [57] |
Sun L, Li Z, Li Z, et al. Design and mechanism of coreshell TiO2 nanoparticles as a high-performance photothermal agent[J]. Nanoscale, 2017, 9(42): 16183–16192.
DOI:10.1039/C7NR02848B |
| [58] |
Nikitenko S I, Chave T, Cau C, et al. Photothermal hydrogen production using noble-metal-free Ti@TiO2 core-shell nanoparticles under visible-NIR light irradiation[J]. ACS Catal, 2015, 5(8): 4790–4795.
DOI:10.1021/acscatal.5b01401 |
| [59] |
Gao M, Connor P K N, Ho G W. Plasmonic photothermic directed broadband sunlight harnessing for seawater catalysis and desalination[J]. Energy Environ Sci, 2016, 9(10): 3151–3160.
DOI:10.1039/C6EE00971A |
| [60] |
Lu L, Xu X, An K, et al. Coordination polymer derived NiS@g-C3N4 composite photocatalyst for sulfur vacancy and photothermal effect synergistic enhanced H2 production[J]. ACS Sustain Chem Eng, 2018, 6(9): 11869–11876.
DOI:10.1021/acssuschemeng.8b02153 |
| [61] |
Guo X, Xue F, Xu S, et al. Coupling photothermal effect into efficient photocatalytic H2 production by using a plate-like Cu@Ni core-shell cocatalyst[J]. ChemCatChem, 2020, 12(10): 2745–2751.
DOI:10.1002/cctc.202000258 |
| [62] |
Zhang J, Huang F. Enhanced visible light photocatalytic H2 production activity of g-C3N4 via carbon fiber[J]. Appl Surf Sci, 2015, 358: 287–295.
DOI:10.1016/j.apsusc.2015.08.089 |
| [63] |
Li Z, Liu J, Zhao Y, et al. Photothermal hydrocarbon synthesis using alumina-supported cobalt metal nanoparticle catalysts derived from layered-double-hydroxide nanosheets[J]. Nano Energy, 2019, 60: 467–475.
DOI:10.1016/j.nanoen.2019.03.069 |
| [64] |
Wang L, Zhang Y, Gu X, et al. Insight into the role of UV-irradiation in photothermal catalytic Fischer-Tropschsynthesis over TiO2 nanotube-supported cobalt nanoparticles[J]. Catal Sci Technol, 2018, 8(2): 601–610.
DOI:10.1039/C7CY02304A |
| [65] |
Yu S, Zhang T, Xie Y, et al. Synthesis and characterization of iron-based catalyst on mesoporous titania for photo-thermal F-T synthesis[J]. Int J Hydrog Energy, 2015, 40(1): 870–877.
DOI:10.1016/j.ijhydene.2014.10.121 |
| [66] |
Li Z, Liu J, Zhao Y, et al. Co-Based catalysts derived from layered-double-hydroxide nanosheets for the photothermal production of light olefins[J]. Adv Mater, 2018, 30(31): 1800527.
DOI:10.1002/adma.201800527 |
| [67] |
Zhao Y, Li Z, Li M, et al. Reductive transformation of layered-double-hydroxide nanosheets to Fe-based heterostructures for efficient visible-light photocatalytic hydrogenation of CO[J]. Adv Mater, 2018, 30(36): 1803127.
DOI:10.1002/adma.201803127 |
| [68] |
Li Y, Li R, Li Z, et al. Effect of support on catalytic performance of photothermal Fischer-Tropsch synthesis to produce lower olefins over Fe5C2-based catalysts[J]. Chem Res Chin Univer, 2020, 36: 1006–1012.
DOI:10.1007/s40242-020-0253-5 |
| [69] |
Gao W, Gao R, Zhao Y, et al. Photo-driven syngas conversion to lower olefins over oxygen-decorated Fe5C2 catalyst[J]. Chem, 2018, 4(12): 2917–2928.
DOI:10.1016/j.chempr.2018.09.017 |
| [70] |
Wang Y, Zhao Y, Liu J, et al. Manganese oxide modified nickel catalysts for photothermal CO hydrogenation to light olefins[J]. Adv Energy Mater, 2020, 10(5): 1902860.
DOI:10.1002/aenm.201902860 |
| [71] |
Li R, Li Y, Li Z, et al. A Metal-segregation approach to generate CoMn alloy for enhanced photothermal conversion of syngas to light olefins[J]. Sol RRL, 2021, 5(2): 2000488.
DOI:10.1002/solr.202000488 |
 2021, Vol. 35
2021, Vol. 35


