2. 东南大学 能源与环境学院, 江苏 南京 210096
2. School of Energy and Environment, Southeast University, Nanjing 210096, China
近年来, NH3法选择性催化还原(NH3-SCR)已被证明是控制燃煤NOx排放最有效的技术之一[1], 蜂窝状V2O5-WO3/TiO2是目前NH3-SCR脱硝反应系统使用最广泛的商用催化剂[2-3], 具有良好的催化效率, 但其反应活性温度窗口(300~400 ℃)较高. 在低温条件下催化效率下降明显, 而某些行业如: 焦化行业烟气温度一般低于300 ℃, 若采用中高温脱硝, 需将烟气加热至350 ℃, 会耗费大量能源, 因此, 开展中低温脱硝催化剂的研究已成为烟气脱硝领域的研究热点[4-5].
目前, 以TiO2为载体的钒氧化物催化剂是目前应用较广的SCR脱硝催化剂, Ce、Fe、Mn等元素改性的V2O5-TiO2催化剂对NOx具有一定的催化活性[6-7]. Zhao等[8]报道了Mn-Ce-V-WOx/TiO2系列催化剂, 其脱硝活性明显高于TiO2分别负载的单组分催化剂, 尤其是活性组分/TiO2=0.2摩尔比的催化剂在150~400 ℃表现出最优的催化性能. Xin等[9]设计并制备了由Mn2O3和Mn2V2O7组成的复合催化剂, 相比于Mn2O3, 其低温NO转化率和N2选择性均有显著提高. 虽然Mn2V2O7具有较好的N2选择性, 但NO转化率却较低. V0.05-MnOx催化剂在120~240 ℃温度区间取得了超过90%的NO转化率和80%的N2选择性. 已有研究表明PdOx复合材料是挥发性有机物催化氧化、NH3-SCR脱硝反应中最活跃的物种[10-11]. 此外, 以前的研究[12-13]表明通过添加PdOx物种, 可以大大提高V/TiO2催化剂的催化活性. 因此, Pd改性V/TiO2催化剂可能是一种潜在的NH3-SCR脱硝催化材料, 而其表面发生的脱硝反应机理亟待深入研究.
基于已有的研究基础, 我们提出在TiO2载体上负载V2O5和PdOx, 制备得到多活性位点PdV/TiO2催化剂, 开展催化剂脱硝活性性能测试, 并结合XRD、BET、SEM、NH3/O2-TPD、H2-TPR、XPS、In situ DRIFT等表征方法以及DFT计算分析催化剂表面NH3-SCR脱硝机理.
1 实验部分 1.1 材料与试剂烟气分析仪(Testo350-XL)购自德图仪器国际贸易有限公司. 实验所用溶液纯度均为分析纯(AR), 其中, 硝酸钯、偏钒酸铵、锐钛矿型二氧化钛(> 99.9%)均购自阿拉丁试剂有限公司; 催化剂活性测试所用N2、NH3、NO、O2均由南京上元气体有限公司提供.
1.2 实验 1.2.1 催化剂制备催化剂采用等体积浸渍法制备, 其制备方法如下: 将2 g TiO2粉末加入30 mL去离子水中, 分别根据Pd和V与TiO2的质量比(%), x g Pd(NO3)2·nH2O和y g NH4VO3粉末进行测定, 然后加入去离子水中, 制备混合溶液. 将混合溶液在25 ℃下搅拌直至水蒸发至干, 然后在105 ℃下干燥8 h, 然后在500 ℃下焙烧5 h, 以获得不同质量分数的催化剂, 记为PdxVy/TiO2催化剂. 其中x和y表示Pd和V元素的质量分数.
1.2.2 催化剂表征采用扫描电子显微镜(SEM, Ultra Plus, Zeiss, 德国)分析催化剂样品的形态和表面结构. 采用Bruke D8 Advance X射线衍射仪(德国)进行催化剂的物相组成和晶体结构分析. 测试中用Cu-Kα辐射源, 设定电压为30 kV, 扫描速度为5(°)/min, 扫描范围为10°~80°, 步长为0.02°. 采用V-Sorb2800P型比表面积及孔径分析仪, 在液氮温度(-196 ℃)下进行N2吸附-解吸实验. 比表面积是通过应用Brunauer-Emmett-Teller(BET)方程从N2吸附等温线计算得出的. O2-温度程序解吸(TPD)和H2-温度程序还原(TPR)分析均在与FINESORB-3010仪器连接的石英U型石英管反应器中进行. 对于TPD测量, 催化剂样品用量为70 mg, O2-He作为吸附剂. 使用10 mL·min-1 NH3和30 mL·min-1 N2的混合物进行吸附. 吸附饱和后, 以30 mL·min-1的速度吹扫He, 直到TCD检测器信号变得稳定为止, 然后, 在He气氛中(以30 mL·min-1的流速)从100升高到600 ℃进行解吸, 并且记录工作曲线. 在进行TPR测量之前, 将样品(20 mg)在高纯度Ar(20 mL·min-1)中于200 ℃预处理30 min, 并保持35 min, 然后冷却至室温. 随后以20 mL·min-1的流速引入H2, 然后以10 ℃/min的速度由室温升高至800 ℃以进行程序升温还原, 使用TCD检测器采集信号. X射线光电子能谱(XPS)是通过Thermo Scientific K-Alpha+使用AlKα作为辐射源进行的. Ti 2p, V 2p, O 1s和Pd 3d的结合能由表面污染C 1s在284.8 eV处的峰值能量校正. O2/NH3/NO/NO2吸附的In situ DRIFT光谱是在Nicolet6700光谱仪(Thermo Electron Corporation, 美国)上进行的, 波数范围为1200~2000 cm-1, 分辨率为4 cm-1(每个光谱进行32次扫描).
1.2.3 催化剂活性测试在固定床石英反应器中开展催化剂NH3-SCR反应活性测试. 该反应器由内径为8 mm的石英管制成, 催化剂用量约100 mg(0.450~0.280 mm). 入口烟气中由0.06% NH3、0.06% NO和10% O2组成, N2作为平衡气. 反应空速(GHSV)为12 000 mL·g-1·h-1. 催化氧化实验测试温度范围为100~400 ℃, 且每个温度测试前稳定30 min. 实验采用烟气分析仪检测进出口处气体浓度(NO、NO2和O2). 入口烟气在进入反应器之前, 在气体室内混合预热.
根据以下公式计算PdxVy/TiO2催化剂的NOx转化率和N2选择性:
式中, NOxConversion和N2Selectivity分别代表NOx转化率和N2选择性. C(NH3)in和C(NOx)in分别代表NH3和NOx进口气体浓度, 而C(NOx)out、C(NH3)out、C(N2O)out和C(CO2)out分别代表NOx、NH3和N2O出口气体浓度.
| $ \mathrm{NO}_{x \text { Conversion }}=\frac{\mathrm{C}\left(\mathrm{NO}_{x}\right)_{\text {in }}-\mathrm{C}\left(\mathrm{NO}_{x}\right)_{\text {out }}}{\mathrm{C}\left(\mathrm{NO}_{x}\right)_{\text {in }}} \times 100 \% $ | (1) |
| $ \mathrm{N}_{2 \text { Selectivity }}=1-\frac{2 \mathrm{C}\left(\mathrm{N}_{2} \mathrm{O}\right)_{\text {out }}}{\mathrm{C}\left(\mathrm{NO}_{x}\right)_{\text {in }}+\mathrm{C}\left(\mathrm{NH}_{3}\right)_{\text {in }}-\mathrm{C}\left(\mathrm{NO}_{x}\right)_{\text {out }}-\mathrm{C}\left(\mathrm{NH}_{3}\right)_{\text {out }}} \times 100 \% $ | (2) |
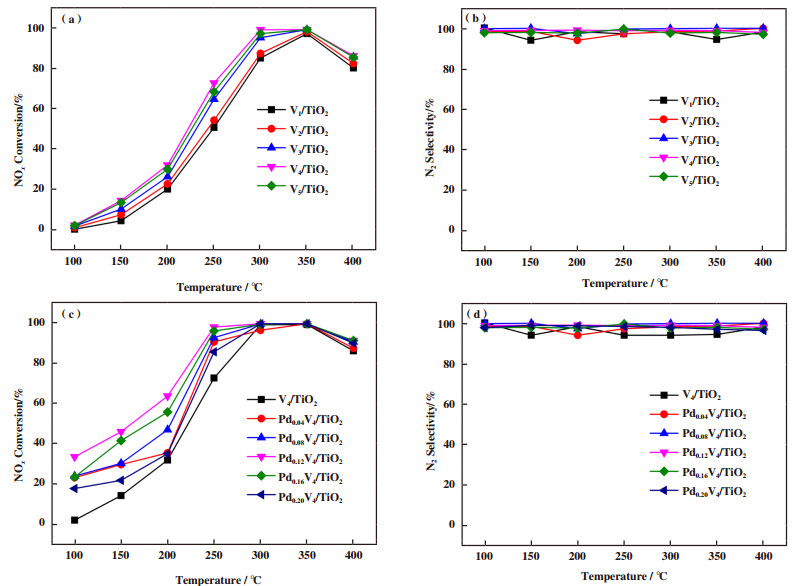
图 1显示了不同浓度Pd元素改性PdxVy/TiO2系列催化剂表面NOx转化率和N2选择性与反应温度的关系. 总体而言, 在测试温度范围(100~400 ℃)内, PdxVy/TiO2催化剂对NOx的催化活性与N2选择性均随温度升高而增强, 其中, Pd0.12V4/TiO2催化剂表现出最优的NOx催化脱除性能, 在250 ℃时可达到接近100%的NOx转化率和N2选择性, 这可能是由于过多Pd元素的添加可能导致活性组分在催化剂表面发生团聚, 进而使得其催化活性有所降低.
|
图 1 PdxVy/TiO2催化剂NOx转化率与N2选择性 Fig.1 NOx conversion and N2 selectivity of PdxVy/TiO2 catalysts |
Pd0.12V4/TiO2催化剂的SEM及其对应EDX能谱如图 2(a-f)所示, 可以发现, Pd0.12V4/TiO2催化剂结构呈层状分布, 疏松多孔, 这有利于气相催化反应的进行. 此外, EDX能谱检测到催化剂中O, Ti, V和Pd 4种元素, 并且活性组分(PdOx和VOx)非常均匀地分散在锐钛矿型TiO2表面上. 活性组分PdOx和VOx主要以无定型的形态存在于载体材料表面, 这与文献报道结论一致[14].

|
图 2 Pd0.12V4/TiO2催化剂SEM-EDX图 Fig.2 SEM images of Pd0.12V4/TiO2 catalysts |
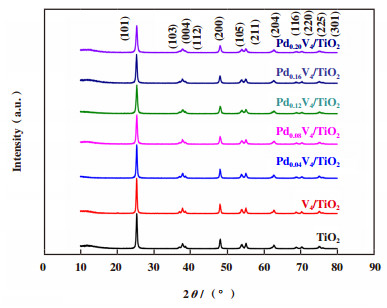
V4/TiO2和不同浓度Pd元素改性PdxV4/TiO2系列催化剂的XRD结果如图 3示. 这3款催化剂中均仅发现对应于锐钛矿型TiO2(PDF#21-1272)不同晶面的衍射峰, 且在各晶面中, (101)面是出现频率最高面. 此外, 由于锐钛矿型TiO2催化剂载体上的Pd和V含量较低且分散度较高, 因此, 未检测到所有催化剂的PdOx和VOx物种所对应的衍射峰. 此外, 催化反应前后催化剂晶体结构未发生明显变化.
|
图 3 不同催化剂XRD图 Fig.3 XRD patterns of different catalysts |
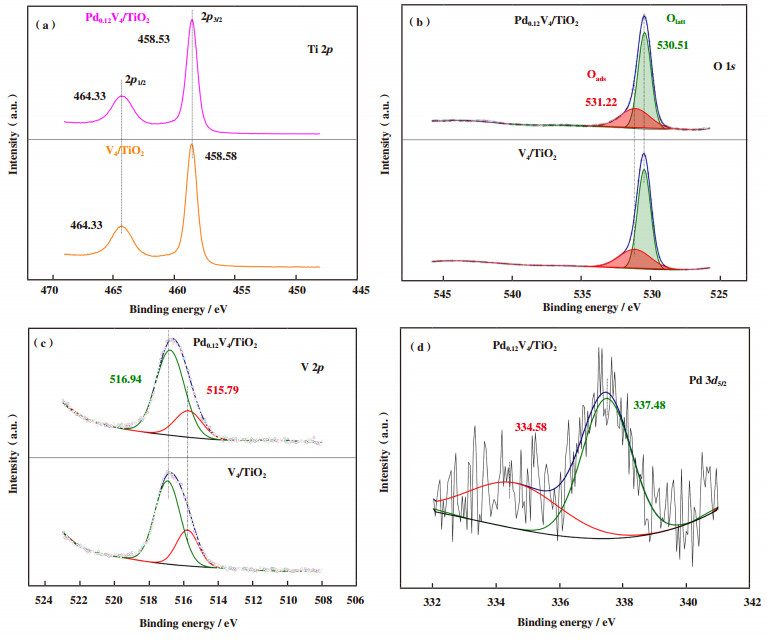
实验同时利用XPS表征方法对催化剂的表面物种和化学状态进行分析, 测试分析结果如图 4和表 1所示. 图 4(a)显示了V4/TiO2和Pd0.12V4/TiO2两款催化剂的Ti 2p XPS光谱. 在两种催化剂Ti 2p1/2和2p3/2的光谱中观察到双特征峰, 结合能(BE)= 458.59和464.33 eV, 均对应于Ti4+[15], 未观测到对应于Ti3+的特征峰. Pd0.12V4/TiO2和Used Pd0.12V4/TiO2催化剂的Ti 2p XPS光谱衍射强度略低于V4/TiO2催化剂. 相比于新鲜Pd0.12V4/TiO2催化剂, 稳定性测试后催化剂表面Ti4+峰强度降低, 这表明部分Ti4+参与了催化氧化过程, 并被还原为Ti2+或Ti3+. O 1s XPS光谱及其分峰拟合处理结果如图 4(b)所示, 其中, BE = 530.51和531.22 eV处的氧物种分别对应于晶格氧(Olatt)和表面吸附氧(Oads), 如: O2-, O22-, O-或OH-)物种[16]. 研究表明, 由于其具有较高的迁移率, Oads在氧化反应中具有很高的活性[17]. 此外, 如表 1所示, Pd0.12V4/TiO2催化剂表面Oads/Olatt比例(53.70%)明显高于V4/TiO2催化剂(46.76%), 而其表面Oads/Olatt在活性测试后亦略有降低. 如图 4(c)所示, V 2p XPS光谱分为BE = 515.79和516.94 eV的两个特征峰, 分别归因于V4+和V5+[18]. 分析结果表明两款催化剂表面V5+/V4+比例变化不大, 均约为2.60. 如图 4(d)所示, Pd 3d5/2 XPS光谱也同样可以分为BE = 334.8和336.5 eV两个特征峰, 分别对应于Pd0和Pd2+[19]. 可以发现少量的Pd添加后催化剂活性大大提高, 这可能归因于引入0.12% Pd后吸附位点的增加.
|
图 4 V4/TiO2和Pd0.12V4/TiO2催化剂XPS图谱 Fig.4 XPS patterns of V4/TiO2 and Pd0.12V4/TiO2 catalysts |
| 表 1 V4/TiO2, Pd0.12V4/TiO2和Used Pd0.12V4/TiO2催化剂的XPS和BET测试结果 Table 1 XPS peak fitting and BET of V4/TiO2, Pd0.12V4/TiO2 and used Pd0.12V4/TiO2 catalysts |
通过H2-TPR表征方法研究了V4/TiO2和Pd0.12V4/TiO2催化剂的还原性能, 结果如图 5所示. 在V4/TiO2催化剂表面上发现了两个H2还原峰, 分别在398 ℃(peak Ⅰ)和459.4 ℃(peak Ⅱ)附近, 分别对应于V5+还原为V4+和Ti4+还原为Ti3+[20]. 相比于V4/TiO2催化剂, 在Pd0.12V4/TiO2催化剂表面获得了两个更低温度的还原峰(peak Ⅲ和Ⅳ), 其中peak Ⅲ可归因于Pd2+还原为Pd0[21], 而peak Ⅳ归因于PdOx的还原, 该PdOx位于另一种活性成分与载体之间的界面上(其与VOx和锐钛矿型TiO2产生强烈的相互作用)[22]. 因此, 还原峰的移动表明分散良好的两种活性成分(PdOx和VOx)和锐钛矿型TiO2之间的相互作用更强. 显然, Pd的添加有利于氧化还原反应的进行, 即2V4+(Ti3+)+Pd2+→2V5+(Ti4+)+ Pd0, 这与XPS测试分析结果一致.

|
图 5 V4/TiO2和Pd0.12V4/TiO2催化剂H2-TPR图 Fig.5 H2-TPR profiles of V4/TiO2 and Pd0.12V4/TiO2 catalysts |
实验对V4/TiO2和Pd0.12V4/TiO2两款催化剂进行O2-TPD表征分析, 测试结果如图 6所示. 一般来说, 物理吸附氧(O2(ad))和化学吸附氧(O2-/O-(ad))物种比晶格氧(O2-)物种更易于从催化剂表面解吸[23-24]. 由图 6可知, 约在270和340 ℃处可以观察到两个氧物种解吸峰. 其中, 在100~300 ℃范围内获得的解吸峰归属于化学吸附氧物种, 例如O2-和O-, 而另一个在300 ℃以上的峰归因于PdOx和VOx活性组分团簇中晶格氧物种的解吸[25-26]. 可以看出, 添加0.12%Pd会大大增加催化剂氧的种类, 特别是化学吸附氧的解吸量. 值得一提的是, 测得的催化剂O2解吸峰与其活性温度区间范围一致, 这表明Pd0.12V4/TiO2催化剂对NOx表现出的优异催化脱除活性可以归因于其丰富的表面氧种类和氧迁移率的提高.

|
图 6 V4/TiO2和Pd0.12V4/TiO2催化剂O2-TPD图 Fig.6 O2-TPD profiles of V4/TiO2 and Pd0.12V4/TiO2 catalysts |
NH3作为脱硝反应的还原剂, 其在催化剂表面的吸附量及吸附形态至关重要. 通过NH3-TPD实验对V4/TiO2和Pd0.12V4/TiO2催化剂表面的酸量进行表征, 结果如图 7所示. 可以发现, V4/TiO2和Pd0.12V4/TiO2催化剂的NH3解吸峰均在100~450 ℃范围内. 与V4/TiO2催化剂相比, Pd的加入使Pd0.12V4/TiO2催化剂表面酸量明显增加. 此外, Pd0.12V4/TiO2催化剂的NH3脱附面积最大. 最重要的是, NH3-TPD的结果与催化剂活性和温度范围一致.

|
图 7 V4/TiO2和Pd0.12V4/TiO2催化剂NH3-TPD图 Fig.7 NH3-TPD profiles of V4/TiO2 and Pd0.12V4/TiO2 catalysts |
锐钛矿型TiO2各晶面的稳定性顺序如下: (101) > (100) > (001). 此外, 从XRD测试结果可以发现(101)面同样也是出现频率最高的晶面. 两种活性成分(PdOx和VOx)负载于锐钛矿型TiO2(101)表面[27], 优化后所得催化剂结构如图 8所示. 在该催化剂结构表面上主要为Pd和V两个吸附位点.

|
图 8 优化后PdV/TiO2(101)催化剂结构的俯视图(a)和侧视图(b-c) Fig.8 Top view (a) and side view (b and c) of optimized PdV/TiO2 (101) catalyst structure |
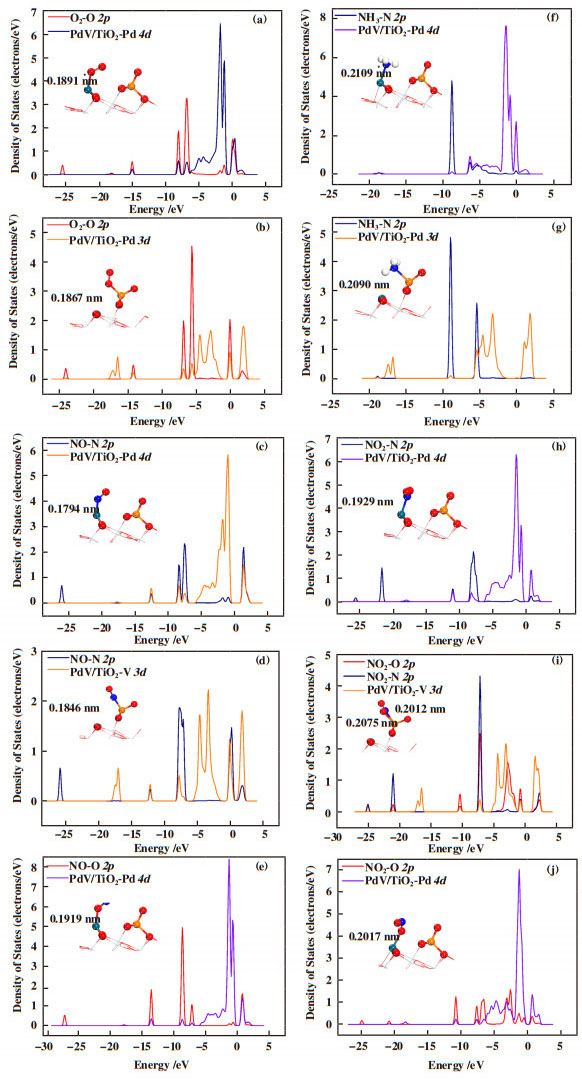
如图 9所示, PdV/TiO2催化剂表面的Pd和V位点是NH3-SCR各反应气体分子吸附的主要位点. 利用DFT计算评价了O2分子在PdV/TiO2催化剂表面的吸附情况. 如图 9(a-b)所示, O2分子既可以被吸附在Pd位点上也可以被吸附在V位点上, 且由吸附后的PDOS结果可以发现O 2p轨道和V 3d轨道(Pd的4d轨道)之间存在明显的杂化, 这表明两者之间存在化学相互作用, 生成的O-V(或O-Pd)键长为0.1867(或0.1.91)nm, 表现出的吸附能为-5.848(或-7.286)eV. NH3分子作为SCR反应中重要的气体分子, 同样通过DFT计算研究了NH3分子在催化剂表面的潜在吸附酸位点. 众所周知, NH3分子是呈现三角形金字塔结构, NH3分子中N原子的s轨道和p轨道不等sp3杂化形成4个轨道, 键角为107.8°. 优化后的NH3分子吸附构型如图 9(f-g)所示, NH3分子通过N端被吸附在催化剂表面Lewis酸(Pd和V)位上, 所生成的O-V(或O-Pd)键长为0.2090(或0.2109)nm, 相应的吸附能为-6.070(或-6.785)eV. PdV/TiO2催化剂表面对NOx(NO和NO2)气体分子的吸附捕集在NH3-SCR反应中同样重要, 优化后的NOx吸附构型如图 9(c-e和h-j)所示. NO分子可以分别通过O端和N端被吸附在PdV/TiO2催化剂表面Pd位点上, 而其仅能够通过N端被吸附在表面V位点上. 此外, NO在Pd位点上吸附(-8.447和-6.828 eV)的吸附能高于其在V位点上(-5.375 eV)的吸附能, 生成的对应化学键的键长分别为1.794(N-Pd)、1.919(O-Pd)和0.1846(N-V)nm. 对于NO2分子在V位点上的吸附, 其亦可分别通过N端和O端与PdV/TiO2催化剂表面的V位点结合, 且新形成的N-V和O-V键的长度分别为0.2012和0.2075 nm, 其吸附能为-6.262 eV, 优化后的构型被认为是螯合硝基化合物[25]. NO2分子可以通过N端和O端分别吸附在Pd位点上, 且NO2分子在PdV/TiO2催化剂表面与Pd位点结合分别为单齿配位亚硝酸盐(图 9j)和线性亚硝酸盐(图 9i)[26]. 这两种吸附构型对应的吸附能分别为-7.593和-7.068 eV. O2、NH3、NO和NO2气体分子在PdV/TiO2催化剂表面的吸附均为化学吸附, 且有新化学键形成. 各反应气体分子在催化剂表面的吸附构型中(非发生吸附的构型除外), 气体分子的最高占据分子轨道(HOMO)会与催化剂表面Pd和V位点的最低未占据分子轨道(LUMO)发生杂化. 因此, 可以得出的结论是NH3-SCR反应中各气体分子均可以被PdV/TiO2催化剂表面吸附并活化.
|
图 9 O2、NH3、NO和NO2气体分子在PdV/TiO2催化剂表面的吸附结构和PDOS Fig.9 Configurations and PDOS for O2, NH3, NO and NO2 gas molecules adsorption (a-n) on the PdV/TiO2 (101) catalyst surface |
| 表 2 NH3-SCR各反应气体分子在PdV/TiO2催化剂表面的成键信息与吸附能 Table 2 Adsorption energy and bonding information of NH3-SCR reaction gas molecules on PdV/TiO2 catalyst surface |
类似地, PdV/TiO2催化剂表面NO与O2、NH3气体分子的单独共吸附结果如图 10和表 3所示. NO和O2的共吸附构型如图 10(a)所示, 吸附能为-7.838 eV, 这可能有利于NO2(2NO + O2 = 2NO2)的生成, 促进了快速SCR的进行. NO和NH3的共吸附构型如图 10(b)所示, 吸附能为-9.109 eV, 这表明PdV/TiO2催化剂表面NH3-SCR过程遵循的L-H机理可顺利发生.

|
图 10 PdV/TiO2催化剂表面NO分别与O2、NH3气体分子的共吸附构型和PDOS(a-b) Fig.10 o-adsorption configurations and PDOS of NO with O2 and NH3 gas molecules on PdV/TiO2 catalyst surface (a-b), respectively |
| 表 3 PdV/TiO2催化剂表面NO分别与O2、NH3气体分子的共吸附能与成键信息 Table 3 Adsorption energy of NO with O2 and NH3 gas molecules on PdV/TiO2 catalyst surface |
原位红外漫反射实验测得的中间物种表明, Pd0.12V4/TiO2催化剂表面发生的NH3-SCR反应, 在原位红外测试中检测到的催化剂表面物种NH3分子将被吸附在Brønsted酸位点(-V-OH或-Ti-OH)和Lewis酸位点(Pd和V)上, 分别生成NH4+和NH3物种, 即① NH3(g)+ Brønsted→-O-NH4+. ② NH3free+M→M-NH3ad. -NH2(NH3物种氧化产生的反应中间体)的存在证明了在氧物种(包括Olatt和Oads)的氧化作用下, 被吸附的NH3物种中的N-H键被破坏, 解离的自由H原子被催化剂表面重新捕获并转化为Brønsted酸位. ③ NH3ad + O→-NH2ad + Brønsted. ④ -NH2ad + NO+O →-N = O+H2O. NH2ad、NH3ad物种发生H解离后的物种与气相或吸附态的NOx物种结合, 生成-N-N=O物种. 最后, 生成的-N-N=O物种进一步转化为无害的N2和H2O, 即, ⑤ -N-N=O + Brønsted→N2 + H2O[33]. 如图 11所示, 检测到的瞬时中间物种表明Pd0.12V4/TiO2催化剂表面发生的NH3-SCR反应过程中O2、NH3、NO和NO2分子处于竞争吸附状态.

|
图 11 250 ℃下Pd0.12V4/TiO2催化剂在SCR气氛吸附30 min的In situ DRIFT反应图谱 Fig.11 In situ DRIFT spectra of SCR on Pd0.12V4/TiO2 at temperature of 250 ℃ for 30 min (balanced by N2), respectively |
| 表 4 In situ DRIFT漫反射峰及其对应的物种 Table 4 In situ DRIFT spectra peaks and their corresponding species |
制备了一系列多活性位点催化剂(PdxVy/TiO2), 并对其NH3-SCR脱硝性能进行了测试分析, 该系列催化剂表现出优异的NOx催化脱除性能, 尤其是Pd0.12V4/TiO2催化剂, 其在250 ℃时可达到接近100%的NOx转化率和N2选择性. 结合一系列的表征和DFT计算分析, 考察了Pd0.12V4/TiO2催化剂表面NOx催化脱除机理分析. 催化剂表面对NH3、O2和NOx等反应气体分子表现出强烈的单吸附和共吸附性能, 且均为化学吸附. 催化剂中各组分(PdOx和VOx)在NOx的催化脱除中均发挥着不可或缺的作用, 其优越的NOx催化性能归功于催化剂表面存在的氧化还原循环(2V4+(Ti3+)+ Pd2+→2V5+(Ti4+)+Pd0), 催化剂表面同时存在E-R机理与L-H机理.
| [1] |
Li Ke-zhi(李柯志), Luo He(罗河), Zhao Ran(赵冉), et al. Regeneration treatment technology of deactivated vanadium tungsten and titanium denitration catalysts(具焙烧服役史钛白粉对新制脱硝催化剂活性影响机制研究)[J]. J Mol Catal (China)(分子催化), 2020, 34(5): 415-424.
|
| [2] |
Zhou Jin-hui (周锦晖), Li Guo-bo (李国波), Wu Peng(吴鹏), et al. The As poisoning mechanism over comm-ercial V2O5-WO3/TiO2 catalyst(商业V2O5-WO3/TiO2脱硝催化剂砷中毒机理)[J]. J Mol Catal(China)(分子催化), 2018, 32(5): 55-64.
|
| [3] |
Xie Wang-wang (谢旺旺), Zhou Guang-he (周广贺), Zhang Xiao-hong (张晓虹), et al. Research progress ofattapulgite application in flue gas SCR denitration catalytic reaction(凹凸棒石在烟气SCR脱硝催化反应中的应用研究进展)[J]. J Mol Catal (China)(分子催化), 2020, 34(6): 546-558.
|
| [4] |
Kong Ling-peng (孔令朋), Miao Jie (苗杰), Li Ming-hang (李明航), et al. Performances of selective catalytic reduction of NO with CO over CuMnCeLa-O/γ-Al2O3 catalyst (CuMnCeLa-O/γ-Al2O3催化剂助燃脱硝性能研究)[J]. J Mol Catal (China)(分子催化), 2018, 32(4): 295-304.
|
| [5] |
Zi Zhao-hui (訾朝辉), Zhu Bao-zhong (朱宝忠), Sun Yun-lan (孙运兰), et al. Low-Temperature selective cat-alytic reduction of NOx with ammonia over MnOx/Al2O3 catalysts(MnOx/Al2O3催化剂低温SCR脱硝性能)[J]. J Mol Catal (China) (分子催化), 2018, 32(3): 249-260.
|
| [6] |
Smirniotis P G, Pe a D A, Uphade B S. Low-temperature selective catalytic reduction (SCR) of NO with NH3 by using Mn, Cr, and Cu oxides supported on hombikat TiO2[J]. Angew Chem Int Ed, 2001, 40: 2479–2482.
DOI:10.1002/1521-3773(20010702)40:13<2479::AID-ANIE2479>3.0.CO;2-7 |
| [7] |
Boningari T, Pappas D K, Smirniotis P G. Metal oxideconfined interweaved titania nanotubes M/TNT (M = Mn, Cu, Ce, Fe, V, Cr, and Co) for the selective catalytic reduction of NOx in the presence of excess oxygen[J]. J Catal, 2018, 365: 320–333.
DOI:10.1016/j.jcat.2018.07.010 |
| [8] |
Zhao X, Mao L, Dong G. Mn-Ce-V-WOx/TiO2 SCR cat-alysts: Catalytic activity, stability and interaction among catalytic oxides[J]. Catalysts, 2018, 8(2): 76–84.
DOI:10.3390/catal8020076 |
| [9] |
Xin Y, Li H, Zhang N, et al. Molecular-level insight into selective catalytic reduction of NOx with NH3 to N2 over a highly efficient bifunctional V-MnOx catalyst at low temperature[J]. ACS Catal, 2018, 8(4): 937–949.
|
| [10] |
Lott P, Dolcet P, Casapu M, et al. The effect of pre-reduction on the performance of Pd/Al2O3 and Pd/CeO2catalysts during methane oxidation[J]. Ind Eng Chem Res, 2019, 58(28): 12561–12570.
DOI:10.1021/acs.iecr.9b01267 |
| [11] |
Sheng L P, Ma Z X, Chen S Y, et al. Mechanistic insight into N2O formation during NO reduction by NH3 over Pd/CeO2 catalyst in the absence of O2[J]. Chin J Catal, 2019, 40(7): 1070–1077.
DOI:10.1016/S1872-2067(19)63328-0 |
| [12] |
Liu Y, You X C, Sheng Z Y, et al. The promoting effect of noble metal (Rh, Ru, Pt, Pd) doping on the performances of MnOxCeO2/graphene catalysts for the selective catalytic reduction of NO with NH3 at low temperatures[J]. New J Chem, 2018, 42(14): 11673–11681.
DOI:10.1039/C8NJ01417E |
| [13] |
Hosokawa S, Tada R, Shibano T, et al. Promoter effect of Pd species on Mn oxide catalysts supported on rare earth iron mixed oxide[J]. Catal Sci Technol, 2016, 6(21): 7868–7874.
DOI:10.1039/C6CY01462C |
| [14] |
Liu Y, Li Y, Wang Y T, et al. Sonochemical synthesis and photocatalytic activity of meso- and macro-porous TiO2 for oxidation of toluene[J]. J Hazard Mater, 2019, 150(1): 153–175.
|
| [15] |
Wang Y F, Zhang C B, Yu Y B, et al. Ordered mesop-orous and bulk Co3O4 supported Pd catalysts for catalytic oxidation of o-xylene[J]. Catal Today, 2015, 242: 294–299.
DOI:10.1016/j.cattod.2014.06.032 |
| [16] |
Jin Qi-jie (金奇杰), Sui Guo-rong (眭国荣), Liu Qing (刘青), et al. Compatibility optimization of Mn-Mo-W-Ox catalyst for selective catalytic reduction of NO by NH3(Mn-Mo-W-Ox脱硝催化剂活性组分的配伍优化)[J]. J Mol Catal (China)(分子催化), 2017, 31(2): 159-168.
|
| [17] |
Tang Nan (唐南), Huang Yan (黄妍), Li Yuan-yuan (李元元), et al. Low temperature selective catalytic reduc-tion of NO with NH3 over Fe-Mn catalysts prepared by hydrothermal method(水热法制备铁锰催化剂脱硝性能及抗水抗硫性能研究)[J]. J Mol Catal(China)(分子催化), 2018, 32(3): 240-248.
|
| [18] |
Pei G X, Liu X Y, Yang X F, et al. Performance of Cu-Alloyed Pd Single-Atom catalyst for semihydrogenation of acetylene under simulated Front-End conditions[J]. ACS Catal, 2017, 7(2): 1491–1500.
DOI:10.1021/acscatal.6b03293 |
| [19] |
Busto M, Benítez V M, Vera C R, et al. Pt-Pd/WO3-ZrO2 catalysts for isomerization-cracking of long paraffins[J]. Appl Catal A Gen, 2008, 347(2): 117–125.
DOI:10.1016/j.apcata.2008.06.003 |
| [20] |
Shen Y, Wang L F, Wu Y B, et al. Facile solvothermal synthesis of MnFe2O4 hollow nanospheres and their photocatalytic degradation of benzene investigated by in situ FTIR[J]. Catal Commun, 2015, 68: 11–14.
DOI:10.1016/j.catcom.2015.04.025 |
| [21] |
Chen L, Li J H, Ge M F. Promotional effect of Ce-doped V2O5WO3/TiO2 with low vanadium loadings for selective catalytic reduction of NOx by NH3[J]. J Phys Chem C, 2009, 113(50): 21177–21184.
DOI:10.1021/jp907109e |
| [22] |
Bandara J, Mielczarski J A, Kiwi J. Adsorption mecha-nism of chlorophenols on iron oxides, titanium oxide and aluminum oxide as detected by infrared spectroscopy[J]. Appl Catal B Environ, 2001, 34(4): 307–320.
DOI:10.1016/S0926-3373(01)00224-7 |
| [23] |
Qiao Ming (乔明), Zhang Ji-yi (张继义), Zong Lu-yao (宗路遥), et al. Research progress in catalytic denitr-ification performance: The catalyst type, preparation methods and activity(催化脱硝技术研究进展—催化剂的种类、制备方法及催化活性)[J]. J Mol Catal(China)(分子催化), 2020, 34(2): 165-181.
|
| [24] |
Fang Qi-long (方祺隆), Zhu Bao-zhong (朱宝忠), Sun Yun-lan (孙运兰), et al. Study on the performance of lowtemperature De-NOx based on Mn-Fe/Al2O3 catalysts(Mn-Fe/Al2O3催化剂的低温脱硝性能研究)[J]. J Mol Catal(China)(分子催化), 2018, 32(4): 305-314.
|
| [25] |
Guo P, Guo X, Zheng C G. Roles of γ-Fe2O3 in fly ash formercury removal: Results of density functional theory study[J]. Appl Surf Sci, 2010, 256(23): 6991–6996.
DOI:10.1016/j.apsusc.2010.05.013 |
| [26] |
Abdulhamid H, Dawody J, Fridell E, et al. A combined transient in situ FTIR and flow reactor study of NOx stor-age and reduction over M/BaCO3/Al2O3 (Pd or Rh) catalysts[J]. J Catal, 2006, 244(2): 169–182.
DOI:10.1016/j.jcat.2006.09.003 |
| [27] |
Yun D, Wang Y, Herrera J E. Ethanol partial oxidation over VOx/TiO2 catalysts: The role of titania surface oxygen on the vanadia reoxidation in the Mars-van Krevelen mechanism[J]. ACS Catal, 2018, 8(5): 4681–4693.
DOI:10.1021/acscatal.7b03327 |
| [28] |
Zeng Y Q, Wang Y N, Zhang S L, et al. A study on the NH3-SCR performance and reaction mechanism of a cost effective and environment friendly black TiO2 catalyst[J]. Phys Chem Chem Phys, 2018, 20(35): 22744–22752.
DOI:10.1039/C8CP02270D |
| [29] |
Chen Z H, Yang Q, Hua L, et al. CrMnOx mixed oxide catalysts for selective catalytic reduction of NOx with NH3 at low temperature[J]. J Catal, 2012, 276(1/3): 56–65.
|
| [30] |
Ma Z R, Wu X D, Si Z C, et al. Impacts of niobia loading on active sites and surface acidity in NbOx/CeO2-ZrO2 NH3-SCR catalysts[J]. Appl Catal B Environ, 2015, 179: 380–394.
DOI:10.1016/j.apcatb.2015.05.038 |
| [31] |
Amores J G, Escribano V S, Ramis G, et al. An FTIR study of ammonia adsorption and oxidation over anatase supported metal oxides[J]. Appl Catal B Environ, 1997, 13(1): 45–58.
DOI:10.1016/S0926-3373(96)00092-6 |
| [32] |
Sun P F, Zhai S Y, Chen J K, et al. Development of a multi-active center catalyst in mediating the catalytic destruction of chloroaromatic pollutants: A combined experimental and theoretical study[J]. Appl Catal B Environ, 2020, 272: 119015–119024.
DOI:10.1016/j.apcatb.2020.119015 |
| [33] |
Liu J, Li X Y, Li R Y, et al. Facile synthesis of tube-shaped Mn-Ni-Ti solid solution and preferable Langmuir-Hinshelwood mechanism for selective catalytic reduction of NOx by NH3[J]. Appl Catal A Gen, 2018, 549: 289–301.
DOI:10.1016/j.apcata.2017.10.010 |
 2022, Vol. 36
2022, Vol. 36


